서 언
배추(Brassica rapa ssp. pekinensis)를 포함하여 배추과(Brassicaceae) 식물들은 아시아뿐만 아니라 전세계적으로 중요한 가치를 가지고 있는 식물로 구조 및 기능 유전체 연구가 진행되고 있다(The Rice Annotation Project, 2007; Yang et al., 2005). 이에 따라 특이적인 표현형을 바탕으로 이것을 유기한 미지의 유전자를 확인하는 역유전체학(reverse genetics)은 식물 기능 유전체 연구의 한 방향으로써, 다수의 돌연변이체 분석을 용이하게 해준다(Alonso and Ecker, 2006). 여기에는 유전자에 특정 DNA 조각을 삽입하여 그에 따른 기능의 획득 및 소실을 분석해 그 유전자의 기능을 확인하는 삽입돌연변이체 유기 분석법(insertional mutagenesis)이 다양한 생물에서 적용되고 있다(Amsterdam et al., 1997; Azpiroz-Leehan and Feldmann, 1997; Bechtold and Pelletier, 1998; Jeon et al., 2000; Martienssen, 1998). 그러나 삽입돌연변이체에서 단편의 삽입 위치 및 삽입으로 파괴된 유전자의 인접 염기서열(flanking DNA sequence) 정보를 확인하는 것은 고도의 기술을 요구한다.
인접 염기서열을 확인하는 방법으로는 Hamilton et al.(1991)에 의해 보고된 플라스미드 회수법(plasmid rescue)과 inverse PCR(Ochman et al., 1988), ligation-mediated PCR(Cottage et al., 2001; Rosenthal and Jones, 1990), thermal asymmetric interlaced(TAIL)-PCR(Liu and Whittier, 1995)과 같은 PCR방법을 응용한 다양한 방법들이 보고되었다. 특히 TAIL PCR법은 알고 있는 염기서열 정보를 바탕으로 특이적 nested primer와 16bp 정도의 변성 primer가 다중 단계의 온도 변화 단계를 적용한 반복 프로그램에 의하여 반응을 일으키는 것으로, 낮은 특이적 반응(low-stringency)과 높은 특이적 반응(high-stringency)이 반복적으로 이루어지면서 목적 DNA의 인접염기서열을 증폭시켜주는 방법으로 동물, 식물 및 곰팡이까지 널리 이용되고 있으며(Hirochika, 2001; Jeon et al., 2007; Pillai et al., 2008; Weld et al., 2006), microarray까지 적용되어 대량의 시료를 한번에 분석할 수 있게 되었다(Mahalingam and Fedoroff, 2001). 그러나 이러한 TAIL-PCR은 획득할 수 있는 산물의 크기가 0.3-4kb 정도로 제한적이며, 그 성공률도 20-40% 이다(Liu and Whittier, 1995). 이러한 효율의 제약을 극복하기 위하여 primer의 길이를 조절하는 high-efficiency TAIL PCR(Liu and Chen, 2007; Michiels et al., 2003)과 TAIL PCR을 기반으로 변성(arbitrary degenerate, AD) primer 없이 적용 가능한 single oligonucleotide nested (SON) PCR(Antal et al., 2004), multiple displacement amplification(MDA) 방법(Reddy et al., 2008) 등이 보고되었다.
본 연구에서는 T-DNA가 도입된 대량의 삽입돌연변이 배추 집단에서 T-DNA인접 염기서열 분석을 위하여 효율이 증가된 VA-TAIL PCR(Variable Argument - Thermal Asymmetric Interlaced PCR) 방법을 개발하였다. 개발된 방법은 고등 식물인 배추과에서 효과적으로 TAIL PCR을 적용하기 위하여 새로운 AD primer 제작하고, 인접염기서열의 PCR 증폭 효율을 높이기 위해 primer의 연쇄 반응 위치 부여(Antal et al., 2004) 및 autosegment(Mukai and Nakagawa, 1996), touch-up PCR(Ailenberg and Silverman, 2000) 방법을 응용한 가변적인 PCR 반응 프로그램을 적용하였다. 이에 따라 본 방법을 이용하면 T-DNA가 도입된 대량의 배추 집단에서 정확하고 효과적으로 T-DNA 인접 염기 서열을 분석할 수 있을 것으로 기대된다.
재료 및 방법
식물 재료
공시 재료로 사용한 형질전환 돌연변이체는 Agrobacterium tumefaciens(LBA4404)을 이용하여 플라스미드 회수 클로닝(plasmid rescue cloning)용 백터인 pRCV2(Kim et al., 2003)가 도입된 배추(B. rapa ssp. pekinensis var. Seoul)를 이용하였다. 도입된 pRCV2는 pCAMBIA 1301(CAMBIA, Canberra, Australia)과 pBluescript II KS(+)(Stratagene, CA, USA)이 결합된 14,730bp 크기의 벡터로 내부에 식물 선발 마커인 hpt(hygromycin resistance) 유전자와 플라스미드 회수 클로닝을 위한 ampicillin 저항성 유전자 및 origin이 포함되어 있다. 해당 pRCV2가 도입된 배추 돌연변이 집단을 구축하였으며(Lee et al., 2004), 본 연구에서는 VA-TAIL PCR의 효율성을 확인하기 위하여 플라스미드 회수 클로닝을 통해 인접 염기서열이 확인된 mutant line No. 346과 확인되지 않은 돌연변이 계통 14개를 임의로 선발하여 분석하였다.
식물 gDNA 추출
돌연변이 배추에서 gDNA를 추출하기 위해 McCouch et al.(1988)이 제시한 방법을 이용하였다. 공시 재료에서 선발된 T1 돌연변이 배추 종자 15계통을 파종 후 7주간 생육한 잎을 이용하여 gDNA를 추출하였다. 분리된 gDNA는 NanoDrop® UV-Vis Spectrophotometer(ND-1000; Thermo Scientific, MA, USA)를 이용하여 흡광도를 측정하고 A260/A280 비가 1.8이고, A260/A230비가 2.0으로 분석된 gDNA를 이용하여 VA-TAIL PCR을 진행하였다.
VA-TAIL PCR용 primer 작성
배추과에 효과적인 TAIL PCR 방법을 개발하기 위해 먼저 배추에 효과적으로 적용 가능한 배추 특이 AD primer를 작성하였다. 배추 특이 AD primer는 The European Molecular Biology Laboratory’s European Bioinformatics Institute (EMBL-EBI)의 Integr8(http://www.ebi.ac.uk/integr8) 데이터베이스와 National Center for Biotechnology Information (NCBI) GenBank 데이터베이스(http://www.ncbi.nlm.nih.gov)를 분석하여 작성하였다. 그 결과 총 6개의 배추 특이 AD primer를 작성하였으며, BrAD(Brassica rapa specific AD) primer 집단으로 명명하였다(Table 1). 또한 돌연변이 배추에 도입된 pRCV2 vector를 특이적으로 증폭하는 4개의 nested specific primer(SP)를 도입된 vector의 left border와 right border방향으로 각각 2sets 작성하였다. 각각의 primer는 single-step annealing-extension PCR 단계를 진행하기 위하여 annealing temperature를 65°C이상으로 작성하였으며, primer의 반응 효율을 증가시키기 위하여 Gibbs free energy(ΔG) > 0 되도록 구성하였다. 또한 반응의 특이성을 증가시키기 위하여 각각의 primer의 3′ 말단의 3-5bp를 다음 단계에 이용하는 primer의 5′ 말단과 일치하도록 구성하였다. 그 결과 T-DNA의 left border 방향의 LSP1, LSP2, LSP3, LSP4와 right border 방향의 RSP1, RSP2, RSP3, RSP4를 작성하였으며, primer의 일부 염기 서열의 연속 지역이 VA-TAIL PCR 결과에 미치는 영향을 분석하기 위하여 일부 염기 서열의 연속 지역이 없는 대조군으로 left border 방향의 LcSP4과 LcSP5를 추가로 작성하였다(Table 2 and Fig. 1). 각각의 primer가 가지는 dimer 및 hairpin 형성 관련 ΔG의 분석은 Vector NTI oligo-calculator(VectorNTI AdvanceTM, Invitrogen, Carlsbad, CA, USA)를 사용하였다.
Table 1. Identification of arbitrary degenerate (AD) primers for VA-TAIL PCR using the Integr8 proteome analysis server (http://www.ebi.ac.uk/integr8). |
Name | Target domain (Integr8 access number) | Primer sequence(5′→3′) | Variable argumenty |
BrAD1 | Zinc finger protein LSD1 (IPR005735) | GAM RTG NCT VAM WTT Gz | 192 |
BrAD2 | Zinc finger protein LSD1 (IPR005735) | DTA ASA TGN HNT TGC T | 288 |
BrAD3 | Serine/threonine protein kinase, threonine protein kinase (IPR008271) | ARY CAC YGY GAT MTH A | 96 |
BrAD4 | Leucine-rich repeat (LRR) protein (IPR012569) | C YTV ACY WSY TTG RAT | 192 |
BrAD5 | RNA recognition motif domain (IPR001890) | CAY AGR GAT WTD AAA G | 96 |
BrAD6 | RNA recognition motif domain (IPR001890) | VAY GTT RCY YRS TTT C | 192 |
zBrAD primers are degenerate primers. R = A/G; Y = C/T; S = G/C; W = A/T; M = A/C; D = A/G/T; H = A/C/T; V = A/C/G; N = any base. yThe number of unique primer combinations, or degeneracy, of the indicated AD primer. |
|
Table 2. Nested long gene-specific primers for VA-TAIL PCR. |
Primer | Sequence (5′→3′) | GC% | Tm (C) | Dimer ΔG (kcal/mol)y | Hairpin ΔG(kcal/mol) |
LSP1 | CTGTGTAGAAGTACTCGCCGATAGTGGAAAz | 46.7 | 68.2 | -0.2 | 3.6. |
LSP2 | GGAAACCGACGCCCCAGCAC | 70.0 | 68.4 | - | - |
LSP3 | AGCACTCGTCCGAGGGCAAAGAAATA | 50.0 | 69.9 | -1.8 | - |
LSP4 | GAAATAGAGTAGATGCCGACCGGATCTG | 50.0 | 68.3 | -1.7 | -0.4 |
| | | | | |
LcSP4 | CCAAAATCCAGTACTAAAATCCAGATCCC | 41.4 | 68.4 | -1.8 | 2.9 |
LcSP5 | AACGTCCGCAATGTGTTATTAAGTTGTCT | 37.9 | 68.2 | -1.3 | 3.6 |
| | | | | |
RSP1 | CAGGTATGGAATTTCGCCGATTTTG | 44.0 | 67.4 | -0.2 | 0.7 |
RSP2 | ATTTTGCGACCTCGCAAGGCAT | 50.0 | 67.1 | -0.1 | -0.5 |
RSP3 | GGCATATTGCGCGTTGGCG | 63.2 | 66.9 | -1.8 | -0.9 |
RSP4 | GGCGGTAACAAGAAAGGGATCTTCACT | 48.1 | 68.0 | -0.1 | -0.8 |
zUnderlined nucleotide sequences denote the overlapping sequence for each primer. yCalculation of the Gibbs free energy (ΔG) for dimer hybridization and hairpin formation during the annealing step using the Vector NTI oligo-calculator (VectorNTI AdvanceTM; Invitrogen, Carlsbad, CA, USA). |
VA-TAIL PCR을 이용한 T-DNA인접 염기서열 분석
VA-TAIL PCR은 pRCV2 vector로 형질전환되어 선발된 배추 돌연변이체를 대상으로 수행하였으며, 개발된 방법의 효율을 비교하기 위하여 기존의 Liu and Whittier(1995)의 TAIL PCR 프로그램을 대조 방법으로 이용하였다(Table 3). VA-TAIL PCR은 총 20µL의 PCR 반응혼합액에 5 unit Taq polymerase(cat#RR001B; TaKaRa Ex Taq®, Shiga, Japan), 2.5mM dNTP, 10× Taq polymerase buffer, 그리고 각 단계별로 0.2µM nested specific primer와 3.0µM BrAD 조합을 넣은 후 thermocycler(TGradient 96; Biometra, Goettingen, Germany)를 사용하여 실시하였다. 각각의 반응은 left border 방향의 경우 LSP1, LSP2, LSP3, LSP4 순서로 실시하였으며, right border 방향의 경우 RSP1, RSP2, RSP3, RSP4 순서로 단계별 반응을 실시하였다. 또한 primer의 연쇄가 TAIL PCR효율에 미치는 영향을 분석하기 위한 대조 방법의 경우 LSP1, LSP3, LcSP4, LcSP5 순서로 진행하였다. 한편 각 단계의 주형 DNA는 이전 단계의 반응된 주형을 1/100 희석하여 사용하였다. PCR 산물은 agarose gel(1.0%)에 전기영동하여 확인하며, 특이적 반응물을 효과적으로 선발하기 위해 3번째 TAIL PCR산물과 4번째 TAIL PCR산물을 동시에 전기영동하여 동일한 위치에 나타나는 산물을 선발하였다. 염기서열 분석은 선발된 PCR 산물을 gel elution kit(cat#YDF100; HiYieldTM Gel/PCR DNA mini Kit, Real Biotech Corporation, Banqiao, Taiwan)를 이용하여 분리 및 정제 후 TA cloning vector(cat#A1360; pGEM-T® easy vector; Promega, Madison, Wisconsin, USA)에 도입하여 Macrogen Co.(Seoul, Korea)에 의뢰하여 분석하였다. 분석 결과는 NCBI의 BLAST program(http://blast.ncbi.nlm.nih.gov/Blast.cgi)를 이용하여 증폭된 산물에 대한 정보를 분석하였으며, 배추 염색체 내 도입된 T-DNA의 위치를 확인하기 위하여 Flanking Sequence Tag Validator(FSTVAL; http://bioinfo.mju.ac.kr/fstval/)을 이용하였다(Kim et al., 2012). FSTVAL program을 이용한 분석은 해당 program에서 제공하는 배추 데이터베이스를 BLASTN 알고리즘(cutoff e-value < 1e-5)을 적용하여 염색체 번호(A01-A10)와 도입 형태(intergenic, exon, intron, 5′ upstream- 1000, 3′ downstream-300), 인접 유전자명을 분석하였다.
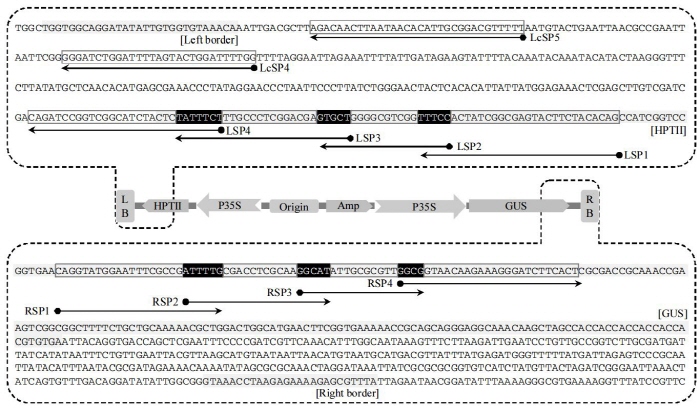
|
Fig. 1. Representation of strategies to design effective nested long gene-specific primers in plasmid pRCV2. The solid line, grey background, and black background indicate the primer binding sites, the overlapping sequence regions for each primer, and vector components, respectively. LSP1-4 are nested long gene-specific linked primers at the T-DNA left border; while LcSP4 and 5 are long gene-specific primers that are not linked; RSP1-4 are nested long gene-specific linked primers at the right border of the T-DNA; LB, left border; RB, right border; HPT II, hygromycin resistance gene; P35S, CaMV 35S promoter; Origin, origin of replication of CoIE1; Amp, ampicillin-resistance gene active in E. coli; GUS, β-glucuronidase reporter gene. |
|
Table 3. VA-TAIL PCR cycle conditions used in this study. |
Reaction | Number of cycles | Thermal settings |
Primary | 1 | 93°C 1 min, 95°C 5 min |
(ADz-SP1y) | 5 | 94°C 30 s, 71°C 3.5 min |
| 1 | 94°C 30 s, 25°C ramping to 72°C in 3 min, 72°C 2.5 min. |
| 15 | 94°C 20 s, 65°C 30 s (+ 0.5°C/cycle), 72°C 2 min (+ 1 s/cycle) |
| | 94°C 20 s, 65°C 30 s (+ 0.5°C/cycle), 72°C 2 min (+ 1 s/cycle) |
| | 94°C 20 s, 42°C 1 min, 72°C 2.5 min. |
| 1 | 72°C 5 min, 4°C hold |
Secondary | 12 | 94°C 20 s, 65°C 30 s (+ 0.5°C/cycle), 72°C 2 min (+ 1 s/cycle) |
(AD-SP2) | | 94°C 20 s, 65°C 30 s (+ 0.5°C/cycle), 72°C 2 min (+ 1 s/cycle) |
| | 94°C 20 s, 42°C 1 min, 72°C 2.5 min. |
| 1 | 72°C 5 min, 4°C hold |
Tertiary | 12 | 94°C 20 s, 65°C 30 s (+ 0.5°C/cycle), 72°C 2 min (+ 1 s/cycle) |
(AD-SP3) | 1 | 72°C 5 min, 4°C hold |
(AD-SP4) | | |
zAD, arbitrary degenerate primers. ySP, specific primers. |
결과 및 고찰
VA-TAIL PCR용 primer 작성 및 효율 분석
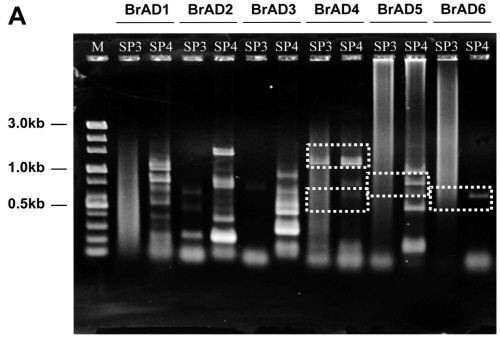
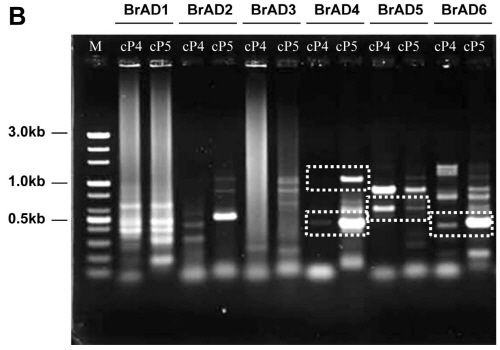
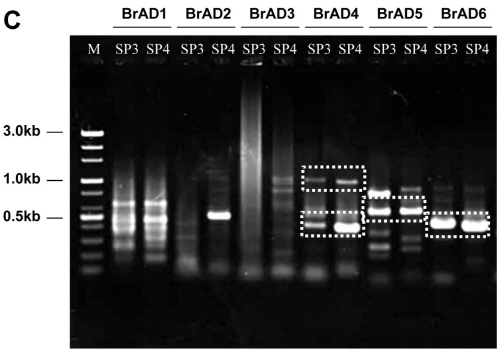
배추과에 효과적인 TAIL PCR 방법을 개발하기 위해 6개의 BrAD(Brassica rapa specific AD) primer를 작성하였다. 고등 식물에서 가장 높은 빈도로 존재하고 있는 단백질의 도메인을 선택하기 위하여, EMBL-EBI의 Integr8에서 제공하는 단백질체 분석 정보를 검색하였으며, 획득된 단백질 정보를 NCBI GenBank 데이터베이스의 protein BLAST로 분석하여 배추 속에서 가장 높은 일치율을 나타내는 염기서열을 수집하였다. 분석 결과 [Zinc finger protein LSD1; InterPro ID IPR005735], [Serine/threonine protein kinase; InterPro ID IPR008271], [Leucine-rich repeat (LRR) protein; IPR012569], [RNA recognition motif domain; InterPro ID IPR001890] 도메인(domain)을 선발하였다. 수집된 높은 빈도의 도메인 염기서열 가운데, 높은 상동성을 보이는 부분을 BLAST로 비교 분석하여 특이적 결합 비율을 180-300가지로 무작위성(degeneracy)을 제한함으로써 반응 특이성을 확보하였다(Table 1). 한편 게놈 크기가 283.9Mb인 배추와 같이 고등식물의 경우 PCR 효율의 극대화가 필수적인 요소이며, 이를 위해서는 single-step annealing-extension PCR 및 autosegment extension PCR 방법과 각각의 primer가 가지는 Gibbs free energy가 최소 -4kcal/mol 이상으로 작성하여 자발적인 반응이 일어나지 않도록 하는 방법 등이 있다(Lee et al., 2010; Mukai and Nakagawa, 1996; Ohler and Rose, 1992). 또한 Antal et al.(2004)은 TAIL PCR에 의한 비특이적 산물을 최소화하고, 반응의 특이성을 증진시키기 위하여 primer의 일부 염기 서열을 연쇄적으로 이어지게 구성하는 것이 효과적이라 보고하였다. 이에 따라 도입된 T-DNA를 특이적으로 증폭하기 위해 left border방향과 right border방향으로 각각 1set씩 작성된 nested specific primer는 PCR 효율을 증가시키기 위하여 ΔG > 0 되도록 구성하였으며, primer의 3′ 말단의 3-5bp를 다음 단계에 이용하는 primer의 5′ 말단과 일치하도록 구성되었다. 그리고 TAIL PCR의 효율을 최대화하기 위해서 single-step annealing-extension PCR를 위한 양방향의 nested specific primer를 Tm 68-70°C로 구성하고 touch-up PCR 방법을 동시에 적용하여 각 cycle마다 annealing 온도가 0.5°C씩 증가하도록 구축하고, autosegment extension PCR의 적용을 위하여 각 TAIL cycle마다 extension 시간을 1초씩 증가시켰으며, 각각의 특이적 primer의 결합위치를 3-5bp가 연쇄되도록 구축하였다(Tables 2 and 3). 위와 같은 방법으로 최적화된 VA-TAIL PCR 방법의 효율을 분석하기 위하여 Lee et al.(2010)의 보고에서 인접염기 서열이 확인된 mutant line No. 899의 left border 부분을 기존의 Liu and Whittier(1995)의 TAIL PCR 방법과 nested specific primer에 일부 염기 서열의 연속 지역이 없는 primer 조합(LSP1, LSP3, LcSP4, LcSP5)을 사용한 TAIL PCR 및 최적화된 VA-TAIL PCR을 실시하여 비교분석 하였다. 분석 결과 최적화된 VA-TAIL PCR 결과에서 BrAD4, BrAD5, BrAD6를 사용한 조합의 0.4-1.0kb사이에 특이적 산물이 확인되었다(Fig. 2C). 특히 특이적 primer인 SP3와 SP4의 경우 각각 7bp가 겹치게 구성되어 있으며 각각의 반응이 독립적으로 이루어졌기 때문에, 각각의 반응에서 동일한 위치의 PCR 산물을 특이적 산물로 판단할 수 있다. 그 결과 최적화된 VA-TAIL PCR 방법에서는 총 4개의 특이적 산물이 확인되었으나(Fig. 2C), 기존의 TAIL PCR 방법에서는 비특이적 산물의 양상만이 확인되었다(Fig. 2A). 또한 nested specific primer에 일부 염기 서열의 연속 지역이 없는 primer 조합을 이용한 경우에서도 전체적인 산물의 양상은 비슷해 졌으나, 특이적 산물의 증폭 효율이 낮았다(Fig. 2B). 즉, 본 연구에서 최적화된 VA-TAIL PCR 방법이 배추를 이용한 연구에서 기존의 TAIL PCR 방법보다 훨씬 효과적임을 확인할 수 있었으며, nested specific primer의 연쇄가 증폭 효율에 효과적임을 확인할 수 있었다.
|
Fig. 2. Comparison of electrophoretograms showing amplification efficiency of variable argument thermal asymmetric interlaced PCR (VA-TAIL PCR, C) with the normal TAIL PCR (A), and VA-TAIL PCR with unlinked primers (B) for identified T-DNA flanking sequences from T1 transgenic lines. Products from VA-TAIL PCR and normal TAIL PCR were obtained from a tertiary reaction. BrAD1-6, B. rapa arbitrary degenerate primers; SP3 and SP4, nested long gene-specific primers 3 and 4 with linked sequence strategy; cP3 and cP4, nested long gene-specific primers 3 and 4 without the linked sequence strategy; M, 100 bp DNA ladder; dashed box, comparison of PCR amplification efficiency. |
pRCV2 삽입 돌연변이 집단의 T-DNA 인접 염기서열 분석
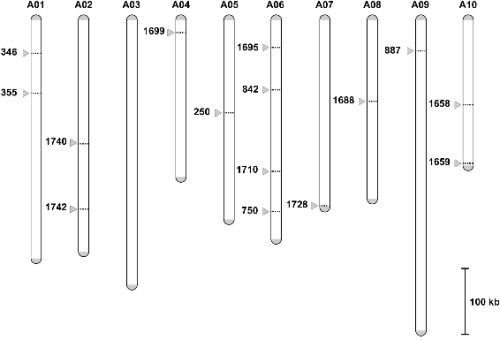
배추에서 최적화된 VA-TAIL PCR 방법을 이용하여 배추 돌연변이 집단 중 T-DNA 인접 염기서열이 확인되지 않은 돌연변이 계통 14개를 임의로 선발하여 분석하였다. 그 결과VA-TAIL PCR을 통하여 특이적인 산물을 확인할 수 있었으며, T-DNA 인접 염기서열이 유의성 있게 분석되었다(Table 4). 배추 염색체 상에 도입된 T-DNA의 위치 분석을 실시한 결과, 선행 연구에서 T-DNA의 도입위치를 확인한 mutant line No. 346를 포함한 총 15개 삽입 돌연변이체 중 intergenic 부분에 T-DNA가 도입된 계통이 8개(53%)이며, exon 지역 3개(20%), intron 지역 1개(7%), 5′ upstream-1000 지역 1개, 3′ downstream-500 지역 1개로 분석되었다. 또한 이러한 T-DNA는 염색체 A06에 4개(26.7%)가 도입되어 가장 많은 것으로 나타났으며, 다음으로는 염색체 A01, 염색체 A02, 염색체 A10에 각각 2개씩(13.3%)이 도입된 것을 확인하였다(Table 4 and Fig. 3). 플라스미드 회수 클로닝을 이용하여 배추 돌연변이 집단의 T-DNA 인접 염기서열을 분석한 연구 결과에서 mutant line No. 346의 경우 선행 연구와 동일하게 염색체 A1에 위치하는 것이 확인되었다(Yu et al., 2010). 또한 선행 연구에서는 T-DNA가 exon 지역에 40%, intron 지역에 23%, unknown 지역에 37%가 도입되었으며, 염색체 A3와 염색체 A9에 가장 많이 도입된 것으로 분석되어 본 연구 결과와 차이를 나타내는 데(Yu et al., 2010), 이는 분석된 시료 집단의 크기 차이에 기인한 것으로 본 연구의 VA-TAIL PCR을 이용하여 다수의 집단을 분석한다면 선행 연구와 동일한 결과가 나올 것으로 판단된다. 결론적으로 본 연구에서 최적화한 배추과에 효과적인 VA- TAIL PCR 방법과 6개의 BrAD primer 집단을 이용하면, 배추과 작물에서 T-DNA가 삽입된 인접 염기서열을 분석하거나, 미지의 영역을 분석 시에 효과적으로 사용될 수 있을 것으로 판단된다.
Table 4. T-DNA insertion sites and flanking sequences in the chromosome of transgenic lines. |
Line no. | Ch. no.z | Matching % (e-value) | T-DNAinsertion site | Gene IDy | Description |
250 | A05 | 89.76(5.00E-118) | Intron | Bra030425 | Protein phosphatase 2A 55 kDa regulatory subunit B alpha isoform |
346 | A01 | 98.08(4.00E-162) | Intergenic | Bra011066 | Xyloglucan endotransglucosylase/hydrolase 26 |
355 | A01 | 98.72(0.00) | Intergenic | Bra039772 | Unknown |
750 | A06 | 98.24(0.00) | 5′ Upstream-1000 | Bra025180 | Plastid-lipid associated protein PAP / fibrillin family protein |
842 | A06 | 98.16(1.00E-107) | Intergenic | Bra025846 | RING/U-box superfamily protein |
887 | A09 | 97.71(7.00E-156) | Intergenic | Bra037828 | Myb domain protein 68 |
1658 | A10 | 99.44(0.00) | Exon | Bra002337 | TCP-1/cpn60 chaperonin family protein |
1659 | A10 | 98.54(1.00E-66) | Intergenic | Bra001953 | Cold regulated 413 plasma membrane 1 |
1688 | A08 | 96.43(0.00) | Exon | Bra035281 | Phosphoenolpyruvate carboxylase family protein |
1690 | A04 | 97.92(6.00E-16) | Intergenic | Bra014600 | Tubulin binding cofactor C domain-containing protein |
1695 | A06 | 100.00(6.00E-153) | Intergenic | Bra019964 | Branched-chain amino acid transaminase 1 |
1710 | A06 | 89.82(1.00E-82) | Intergenic | Bra024282 | Dicarboxylate transport 2.1 |
1728 | A07 | 82.29(1.00E-10) | Intergenic | Bra035185 | Indole-3-acetic acid inducible 15 |
1740 | A02 | 98.88(4.00E-91) | Exon | Bra008337 | PHD finger family protein |
1742 | A02 | 87.00(1.00E-79) | 3′ Down-stream-300 | Bra036340 | Unknown |
zChromosome number in B. rapa ssp. pekinensis. yAccession code in Brassica database (http://brassicadb.org/brad/). |
|
Fig. 3. Genetic mapping with VA-TAIL PCR products from transgenic Chinese cabbage. In silico genetic map positions (gray arrows) of the chromosomes denote the T-DNA flanking regions from pRCV2-tagged transgenic Chinese cabbage lines using VA-TAIL PCR analysis. The chromosome positioning analysis was conducted using the web-based analysis program, FSTVAL (http://bioinfo.mju.ac.kr/fstval/). |
Acknowledgements
본 논문은 농촌진흥청 차세대바이오그린21사업(PJ01101601)의 지원에 의해 이루어진 것임.
References
Alonso, J.M. and J.R. Ecker. 2006. Moving forward in reverse: genetic technologies to enable genome-wide phenomic screens in Arabidopsis. Nat. Rev. Genet. 7:524-536.
Ailenberg, M. and M. Silverman. 2000. Controlled hot start and improved specificity in carrying out PCR utilizing Touch-Up and Loop Incorporated Primers (TULIPS). Biotechniques 29:1018-1024.
Amsterdam, A., C. Yoon, M. Allende, T. Becker, K. Kawakami, S. Burgess, N. Gaiano, and N. Hopkins. 1997. Retrovirus-mediated insertional mutagenesis in zebrafish and identification of a molecular marker for embryonic germ cells. Cold Spring Harb Symp. Quant. Biol. 62:437-450.
Antal, Z., C. Rascle, M. Fevre, and C. Bruel. 2004. Single oligonucleotide nested PCR: a rapid method for the isolation of genes and their flanking regions from expressed sequence tags. Curr. Genet. 46:240-246.
Azpiroz-Leehan, R. and K.A. Feldmann. 1997. T-DNA insertion mutagenesis in Arabidopsis: going back and forth. Trends Genet. 13:152-156.
Bechtold, N. and G. Pelletier. 1998. In planta Agrobacterium- mediated transformation of adult Arabidopsis thaliana plants by vacuum infiltration. Methods Mol. Biol. 82:259-266.
Cottage, A., A. Yang, H. Maunders, C. Lacy, and N. Ramsay. 2001. Identification of DNA sequences flanking T-DNA insertions by PCR-walking. Plant Mol. Biol. Rep. 19:321-327.
Hamilton, B.A., M.J. Palazzolo, J.H. Chang, K. VijayRaghavan, C.A. Mayeda, M.A. Whitney, and E.M. Meyerowitz. 1991. Large scale screen for transposon insertions into cloned genes. Proc. Natl. Acad. Sci. USA 88:2731-2735.
Hirochika H. 2001. Contribution of the Tos17 retrotransposon to rice functional genomics. Curr. Opin. Plant Biol. 4:118-122.
Jeon, J.S., S. Lee, K.H. Jung, S.H. Jun, D.H. Jeong, J. Lee, C. Kim, S. Jang, K. Yang, J. Nam, K. An, M.J. Han, R.J. Sung, H.S. Choi, J.H. Yu, J.H. Choi, S.Y. Cho, S.S. Cha, S.I. Kim, and G. An. 2000. T-DNA insertional mutagenesis for functional genomics in rice. Plant J. 22:561-570.
Jeon, J., S.Y. Park, M.H. Chi, J. Choi, J. Park, H.S. Rho, S. Kim, J. Goh, S. Yoo, J. Choi, J.Y. Park, M. Yi, S. Yang, M.J. Kwon, S.S. Han, B.R. Kim, C.H. Khang, B. Park, S.E. Lim, K. Jung, S. Kong, M. Karunakaran, H.S. Oh, H. Kim, S. Kim, J. Park, S. Kang, W.B. Choi, S. Kang, and Y.H. Lee. 2007. Genome-wide functional analysis of pathogenicity genes in the rice blast fungus. Nat. Genet. 39:561-565.
Kim, H.S., S.H. Kim, and Y.D. Park. 2003. Development of rescue cloning vector with phophinothricin resistant gene for effective T-DNA tagging. J. Kor. Soc. Hort. Sci. 44:407-411.
Kim, J.S., J. Kim, T.H. Lee, K.M. Jun, T.H. Kim, Y.H. Kim, H.M. Park, J.S. Jeon, G. An, U.H. Yoon, B.H. Nahm, and Y.K. Kim. 2012. FSTVAL: a new web tool to validate bulk flanking sequence tags. Plant Methods 8:19.
Lee, G.H., Y.J Kang, S.K. Yi, S.B. Lim, and Y.D. Park. 2010. Development of a highly effective T-DNA inserted mutant screening method in a Chinese cabbage (Brassica rapa L. spp. pekinensis) reverse genetics system. Plant Biotechnol. Rep. 4:201-211.
Lee, M.K., H.S. Kim, J.S. Kim, S.H. Kim, and Y.D. Park. 2004. Agrobacterium-mediated transformation system for large-scale production of transgenic Chinese cabbage (Brassica rapa L. ssp. pekinensis) plants for insertional mutagenesis. J. Plant Biol. 47:300-306.
Liu, Y.G. and Y. Chen. 2007. High-efficiency thermal asymmetric interlaced PCR for amplification of unknown flanking sequences. Biotechniques 43:649-656.
Liu, Y. and R. Whittier. 1995. Thermal asymmetric interlaced PCR: automatable amplification and sequencing of insert end fragments from P1 and YAC clones for chromosome walking. Genomics 25:674-681.
Mahalingam, R. and N. Fedoroff. 2001. Screening insertion libraries for mutations in many genes simultaneously using DNA microarrays. Proc. Natl. Acad. Sci. USA 98:7420-7425.
Martienssen, R.A. 1998. Functional genomics: probing plant gene function and expression with transposons. Proc. Natl. Acad. Sci. USA 95:2021-2026.
McCouch, S.R., G. Kochert, Z.H. Yu, Z.Y. Wang, G.S. Khush, W.R. Coffman, and S.D. Tanksley. 1988. Molecular mapping of rice chromosomes. Theor. Appl. Genet. 76:815-829.
Michiels, A., M. Tucker, W.V.D. Ende, and A.V. Laere. 2003. Chromosomal walking of flanking regions from short known sequences in GC-Rich plant genomic DNA. Plant Mol. Biol. Rep. 21:295-302.
Mukai, H. and T. Nakagawa. 1996. Long and accurate PCR (LA PCR). Jpn. J. Clin. Med. 54:917-922.
Ochman, H., A. Gerber, and D. Hartl. 1988. Genetic application of an inverse polymerase chain reaction. Genetics 120:621-623.
Ohler, L.D. and E.A. Rose. 1992. Optimization of long-distance PCR using a transposon-based model system. PCR Methods Appl. 2:51-59.
Pillai, M.M., G.M. Venkataraman, S. Kosak, and B. Torok-Storb. 2008. Integration site analysis in transgenic mice by thermal asymmetric interlaced (TAIL)-PCR: segregating multiple- integrant founder lines and determining zygosity. Transgenic Res. 17:749-754.
Reddy, P.S., S. Mahanty, T. Kaul, S. Nair, S.K. Sopory, and M.K. Reddy. 2008. A high-throughput genome-walking method and its use for cloning unknown flanking sequences. Anal. Biochem. 381:248-253.
Rosenthal, A. and D. Jones. 1990. Genomic walking and sequencing by oligo-cassette mediated polymerase chain reaction. Nucl. Acid. Res. 18:3095-3096.
The Rice Annotation Project. 2007. Curated genome annotation of Oryza sativa ssp. japonica and comparative genome analysis with Arabidopsis thaliana. Genome Res. 17:175-183.
Weld, R.J., K.M. Plummer, M.A. Carpenter, and H.J. Ridgway. 2006. Approaches to functional genomics in filamentous fungi. Cell Res. 16:31-44.
Yang, T.J., J.S. Kim, K.B. Lim, S.J. Kwon, J.A. Kim, M. Jin, J.Y. Park, M.H. Lim, H.I. Kim, S.H. Kim, Y.P. Lim, and B.S. Park. 2005. The Korea Brassica genome project: a glimpse of the Brassica genome based on comparative genome analysis with Arabidopsis. Comp. Funct. Genomics. 6:138-146.
Yu, J.G., G.H. Lee, J.S. Kim, E.J. Shim, and Y.D. Park. 2010. An insertional mutagenesis system for analyzing the Chinese cabbage genome using Agrobacterium T-DNA. Mol. Cells 29:267-275.







