서 언
재료 및 방법
분석용 연구 재료
DNA 추출
DNA barcode 부위의 증폭
염기서열 분석
계통유연관계 분석 및 종 판별용 marker nucleotide 탐색
결과 및 고찰
ITS 및 matK 부위의 특성
배추속 식물의 종간 유연관계 분석
종 감별용 marker nucleotide 발굴
서 언
배추과 식물은 338속, 약 3,709여 종으로 전세계에 분포하고 있으며, 경제적 가치가 매우 높은 작물에 속한다(Warwick and Sauder, 2005; Al-Shehbaz et al., 2006; Warwick et al., 2006). 그 중 갓(Brassica juncea (L.) Czern.)은 배추(B. rapa L., AA genome, 2n=2x=20)와 흑갓(B. nigra (L.) K.Koch, BB genome, 2n=2x=16)의 자연교잡 및 염색체배가로 생성된 복이배체(amphidiploid) 작물로 AABB
genome(2n=4x=36)을 가지고 있으며, 유채(B. napus L.)는 배추와 양배추(B. oleracea L., CC genome, 2n=2x=18)의 자연교잡 및 염색체배가로 생성된 복이배체 작물로 AACC genome(2n=4x=38)을 가지고 있다(Nagaharu, 1935; Johnston et al., 2005).
갓과 유채 각각의 종자는 개자(芥子), 운대자(蕓薹子)라는 한약재로 사용된다. 우리나라 대한민국약전외한약(생약)규격집(Korea Food & Drug Administration, 2012)에서 개자는 십자화과(Cruciferae = Brassicaceae)의 갓 또는 그 변종의 잘 익은 씨로 규정하고 있으며, 운대자는 유채의 잘 익은 씨로 규정하고 있다. 반면, 중국약전(China Pharmacopoeia Committee, 2010)에서는 십자화과 식물 백개(白芥, 백겨자; Sinapis alba L.) 또는 갓의 잘 익은 씨를 말린 것으로 전자를 흔히 ‘백개자(白芥子)’라고 부르며, 후자를 흔히 ‘황개자(黃芥子)’라고 부른다(Korea Institute of Oriental Medicine, 2017). 하지만 이들의 종자가 형태적으로 유사하여 유통되고 있는 한약재 개자와 운대자의 정확한 구별이 어렵다. 또한 같은 속의 배추, 양배추, 중국에서 정품 한약재 개자로 이용하는 백겨자, 그리고 흑개자(黑芥子)라는 명으로 이용되는 흑갓의 종자도 이와 같은 이유로 형태 구별이 매우 어렵다.
국내에서는 일반농가에서 다양한 갓 품종이 식용 목적으로 재배되고 있는데, 농지 단위가 작고, 좁은 지역에 다양한 근연종 배추과 작물을 재배하는 한국의 농업 특성 상, 화분을 통한 유전자 이동이 비교적 빈번하고, 이에 따라 근연종과의 교잡에 의한 교잡종의 발생 가능성이 더 높을 것으로 예상되고 있다(Lim et al., 2015). 실제로 배추속 종자는 종간, 종내 잡종에 의해 중간 형질이 많이 관찰되어 외부 형태적 형질에 기초하여 종을 동정하는데 어려움이 많기 때문에 객관적이고 정확한 동정법이 필요한 현실이다.
DNA barcode는 DNA의 짧은 표준 범위로부터 염기서열을 얻어 종간 비교를 통하여 빠르고 정확한 종 동정을 가능하게 해주는 DNA 상의 특정 유전자 또는 특정 부위로서, Hebert et al. (2003)에 의해 처음 용어가 고안된 이후로 생물학 전 범위에서 활발하게 사용되고 있다(Lee et al., 2015). 식물에서 주로 사용되는 범용성 DNA barcode 부위는 핵 내 45S ribosomal RNA gene(rDNA)에 존재하는 internal transcribed spacer(ITS) 부위와 엽록체 genome에 존재하는 matK, rbcL, psbA-trnH 등이 있는데, 국제생물바코드컨소시엄(CBOL, Consortium for Barcode of Life)에서는 고등식물의 core DNA barcode로 엽록체의 matK와 rbcL조합의 이용을 권고하였다(CBOL Plant Working Group, 2009). 약용식물 분야에서도 오동정으로 인한 약재의 오용을 막기 위해 형태적으로 종 감별이 어려운 종들과 그 근연종들에 대하여 DNA barcode 분석 및 barcode 데이터베이스 구축의 중요성이 대두되어, 최근 이를 통해 약재로 사용되는 기원식물의 종을 동정하고 계통분류학적 근연관계를 분석하는 연구가 활발하게 진행되고 있다(Zhang et al., 2015; Kim et al., 2016; Moon et al., 2016).
배추과에 속하는 배추와 양배추, 유채는 산업적 이용가치가 높아 다양한 산업분야에서 이용되고 있으며, 이에 따라 DNA barcode 및 유전체 연구가 활발히 진행 중이다(Cheng et al., 2014). 하지만 갓에 대한 연구는 최근에 시작되어 유전자와 유전체에 대한 연구가 상대적으로 미비하여(Yang et al., 2016a), 갓의 계통 유연관계 및 유전적 다양성에 대한 분석은 ITS 영역, SSR(simple sequence repeat), RAPD(random amplified polymorphic DNA) 및 AFLP(amplified fragment length polymorphism) marker를 이용한 소수의 연구만이 진행되었다(Srivastava et al., 2001; Kwon et al., 2007; Khan et al., 2008; Ramchiary et al., 2011; Chen et al., 2013; Yang et al., 2016b).
따라서 본 연구에서는 개자와 운대자로 사용되는 갓과 유채와 함께 이들과 혼·오용되거나 혼·오용 우려가 있는 배추과 식물인 흑갓, 양배추, 배추, 백겨자 6종을 대상으로, 핵 내 ITS 부위와 엽록체의 matK 유전자의 DNA barcode 부위로서의 적합성을 확인하고 종 감별을 위한 marker nucleotide를 발굴함으로써, DNA 바코드를 이용한 정확한 종 감별법을 제시하고자 한다.
재료 및 방법
분석용 연구 재료
본 연구에 사용한 갓(B. juncea), 유채(B. napus), 흑갓(B. nigra), 백겨자(Sinapis alba) 시료는 국립농업과학원 유전자원센터(National Agrobiodiversity Center)에서 분양 받은 종자를 파종하여 약 3개월 동안 생장상에서 키운 식물체와 국내 자생지에서 수집하여 -70°C 초저온 냉동고에 보관되어 있던 시료를 이용하였다(Table 1). 분양 받은 시료와 수집된 시료는 본초학, 생약학, 식물분류학 등의 전문가로 구성된 분류·동정 자문회의의 동정을 거쳐 그 종을 최종 확증하였다. 국립농업과학원 유전자원센터에서 분양 받은 시료는 분양 당시의 자원번호를 표기하였으며, 종자를 제외한 시료의 증거표본은 건조식물표본으로 제작하여 한국한의학연구원 한약표준표본관(Index Herbariorum code KIOM)에 표본번호를 부여하여 보관하였다(Table 1). 배추(B. rapa)와 양배추(B. oleracea) 시료는 동부팜흥농, 경신종묘주식회사, 성우종묘, 아시아종묘, 제일종묘농산에서 구입한 종자를 사용하였다(Table 1). 분석에 이용된 재료의 식물명과 학명은 The Plant List(http://www.theplantlist.org/)를 기준으로 정리하였다.
Table 1. Information of the 22 plant and seed samples used in this study 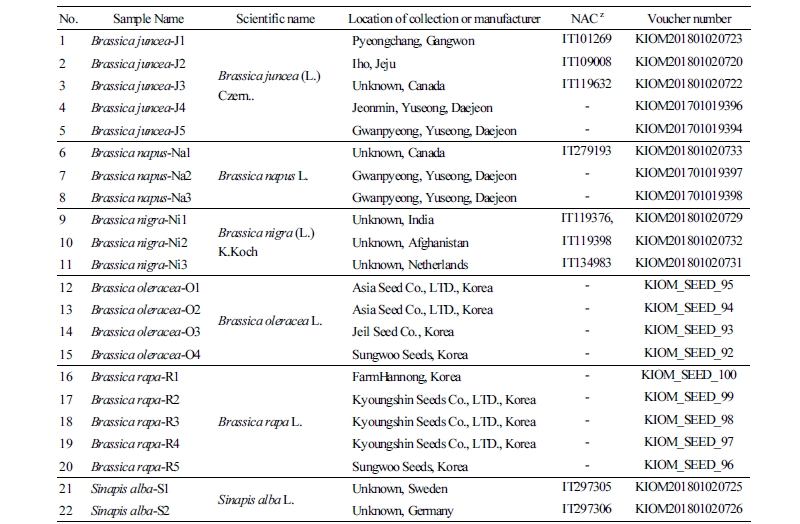 | |
zAccession number of National Agrobiodiversity Center. | |
DNA 추출
-70°C에 보관중인 기원식물 생체시료와 유통되고 있는 품종 종자 100 mg을 Lysing Matrix ATM tube(MP Biomedicals, USA)에 담아 PrecellysTM Grinder(Bertin Technologies, France)를 이용하여 5,500rpm으로 30초 동안 곱게 마쇄한 후, DNeasy Plant Mini Kit(QIAGEN, USA)을 이용하여 제작자가 제공한 protocol에 따라 추출 정제하였다. 정제된 DNA의 순도와 질을 확인하기 위하여 1.5% agarose gel에서 전기영동한 후, EcoDye™ Nucleic Acid Staining Solution(BIOFACT, Korea)로 염색하여 UV light 상에서 DNA band를 확인하였으며, UV spectrophotometer(Nanodrop DN-1000, Nanodrop, USA)를 이용하여 흡광도를 측정한 뒤, 최종 20mg·L-1로 희석하여 분석에 이용하였다.
DNA barcode 부위의 증폭
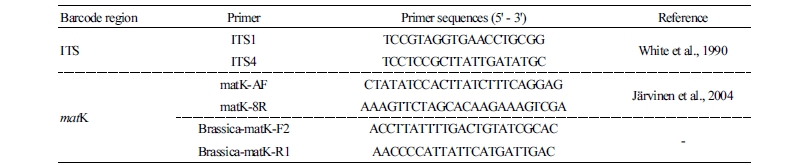
ITS 부위의 증폭을 위하여 약 20ng의 genomic DNA와 각 10pmole의 정방향의 ITS1과 역방향의 ITS4 primer를 이용하였으며(Table 2), 18S rRNA와 26S rRNA의 염기서열을 제외한 ITS1+5.8S rRNA+ITS2 구간을 각 시료의 ITS 부위로 정의하였다. 엽록체 genome에 존재하는 matK 유전자의 증폭을 위하여 matK-AF와 matK-8R의 primer set을 이용하였는데(Järvinen et al., 2004), 증폭이 원활하지 못한 문제가 있어 NCBI GenBank에 등록된 흑갓(NCBI accession no. AB354272.1)과 갓(NCBI accession no. AB354274.1)의 염기서열을 비교하여 primer(Brassica-matK-F2, Brassica-matK-R1)를 제작하여 증폭에 사용하였다(Table 2). 반응 조건은 ITS 부위와 matK 유전자에서 모두 95°C에서 2분간 pre-denaturation 한 후, 95°C에서 1분간 denaturation, 53°C에서 40초간 annealing, 72°C에서 2분간 extension을 총 35회 반복 수행하고 마지막으로 72°C에서 5분 동안 final-extension하여 해당 부위를 증폭하였다.
염기서열 분석
각 시료당 전체 40µL의 증폭산물을 EcoDye™ Nucleic Acid Staining Solution(BIOFACT, Korea)으로 염색한 1.5% agarose gel 상에서 100 bp DNA ladder(Solgent, Korea)와 함께 전기영동하여 증폭 여부를 확인한 후, 정확하게 증폭된 증폭산물을 agarose gel로부터 회수하여 Gel Extraction Kit(QIAGEN, USA)를 이용하여 정제하였다. 정제된 증폭산물을 pGEM-T Easy Vector Systems(Promega, USA)에 삽입하고, 증폭산물이 삽입된 vector를 JM109 competent cell(RBC, USA)에 형질전환한 뒤, 100mg·L-1 ampicillin, 40mg·L-1 X-gal, 그리고 0.5mM IPTG가 첨가된 LB agar 배지에 도말하여 약 18시간 배양하였다. 갓과 유채의 경우, 각각 AABB, AACC genome을 가지므로 두 가지 type의 염기서열이 존재할 수 있기 때문에, 두 가지 type의 염기서열 모두를 얻기 위하여 각 시료별로 5개 이상의 white colony를 취하여 분석에 사용하였다. 그리고 pGEM-T Easy vector의 T7과 SP6 primer를 이용한 colony PCR을 통해 예상된 크기로 증폭된 것을 확인한 clone을 sequencing 하였다. Sequencing 후, 두 가지 염기서열 type이 관찰되지 않은 경우는 white colony 5개를 추가적으로 분석하였다. 염기서열의 정확성과 신뢰성을 확립하기 위한 가이드라인에 따라(Nilsson et al., 2012), 4개의 clone으로부터 얻은 각각의 염기서열 정보를 비교분석하고 PCR 증폭과정에서의 오류를 판별한 후, NCBI GenBank BLAST 검색을 통해 키메라 유무를 판별하고 종을 확인하는 과정을 거쳐 각 시료의 최종 ITS 및 matK 바코드 염기서열을 확정하였다.
계통유연관계 분석 및 종 판별용 marker nucleotide 탐색
22개체의 시료로부터 확보한 ITS와 matK 유전자 최종 염기서열, 그리고 각 부위별로 NCBI GenBank에서 참조가 되는 염기서열을 추가하여 분석에 이용하였다(Table 3). 이들 염기서열을 각 DNA barcode 종류별로 MEGA version 7(Kumar et al., 2016) 프로그램의 ClustalW 정렬법을 이용하여 정렬하고, 동 프로그램에서 intra- 및 inter-specific distance를 계산하였다. ITS와 matK의 GC 비율은 DnaSP version 5.10.01(Librado and Rozas, 2009) 프로그램을 사용하여 계산하였다. ITS 부위의 경우, 갓과 유채의 genome이 각각 AABB, AACC로, 두 가지 type의 염기서열이 모두 검출되기 때문에, 이러한 경우에는 1차적으로 AA 염기서열과 BB 또는 CC 염기서열을 하나의 시료에서 얻은 두 가지 type으로 보고 각 염기서열을 독립된 데이터로 분석하였고, 2차적으로는 하나의 시료에서 얻은 두 가지 type의 염기서열을 AA 염기서열의 마지막 염기 뒤에 BB 염기서열 또는 CC 염기서열의 첫 번째 염기가 위치하도록 수평 직선상으로 배치하여 유합된 데이터로 계통유연관계 분석을 수행하였다. 이 경우에 나머지 이배체 종(배추, 양배추, 흑갓, 백겨자)의 ITS 염기서열은 해당 종의 염기서열의 copy를 위와 같은 방법으로 수평 직선상으로 배치하였다.
Table 3. GenBank accession numbers used in the marker nucleotide analyses and the phylogenetic analyses 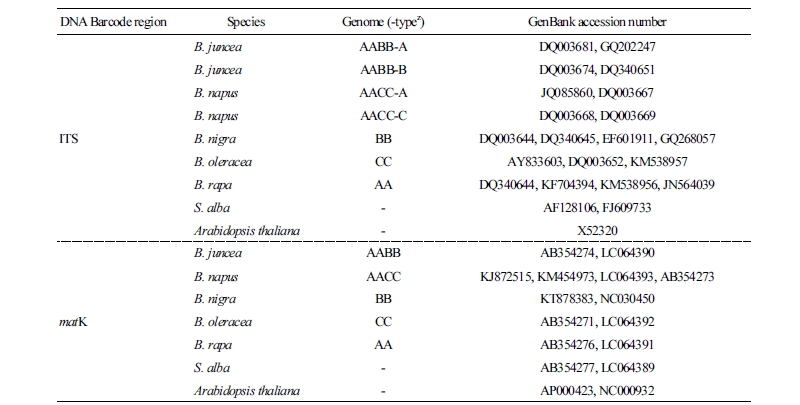 | |
zSequence type corresponding to the amphidiploid species. | |
분석대상 시료의 계통유연관계 분석을 위하여 MEGA version 7 프로그램을 이용하여 각 부위별로 model test를 수행하였고, ITS 부위는 K2+G(Kimura-2-parameter + Gamma), matK 유전자는 T92(Tamura 3-parameter)의 best fit model이 도출되었다. 동 프로그램 상에서 각 부위 염기서열의 best fit model을 적용한 Maximum Likelihood 계통추론방법으로 1,000회 bootstrapping을 통하여 계통수를 도출하였고, 이를 기반으로 분기군 형성 유무와 분기군 간의 근연관계를 비교·분석하였다. 도출된 계통수는 PowerPoint 2013(Microsoft, USA)에서 편집하였다. ITS 부위와 matK 유전자의 염기서열을 유합한 combined data의 적합성을 판단하기 위하여 PAUP version 4.0 (Swofford, 2002)에서 Incongruence Length Difference(ILD) test(Farris et al., 1994)를 수행하였다.
정렬된 matK와 ITS 염기서열의 종내 개체별 비교와 종별 비교를 통해 종 특이성을 갖는 염기(marker nucleotide)의 삽입(Insertions), 결실(Deletions) 및 치환(Substitutions)을 정렬된 위치별로 분석하여 정리하였으며, 이를 토대로 marker nucleotide를 탐색하였다.
결과 및 고찰
ITS 및 matK 부위의 특성
각 시료로부터 추출한 gDNA를 주형으로 하여 ITS1과 ITS4 primer 조합과 matK-AF와 matK-8R primer조합으로 증폭한 결과, 약 600 bp 크기의 ITS 증폭산물은 확인되었으나 약 1250 bp 크기의 matK 유전자의 증폭은 확인되지 않았다. Hollingsworth et al. (2011)과 Ghahramanzadeh et al. (2013)에서 matK 유전자의 변이율이 높아 matK 유전자 증폭 시에 universal primer로는 증폭이 어려운 경우가 많음을 보고하였는데, 본 연구에서도 matK universal primer가 Brassica속에서는 적합하지 않았던 것으로 판단된다. 이러한 이유로 본 연구에서 제작한 Brassica-matK-F2와 Brassica-matK-R1 primer 조합으로 matK 부위를 증폭하였으며, 그 결과 약 1.5 kb의 matK 유전자 절편을 증폭할 수 있었다.
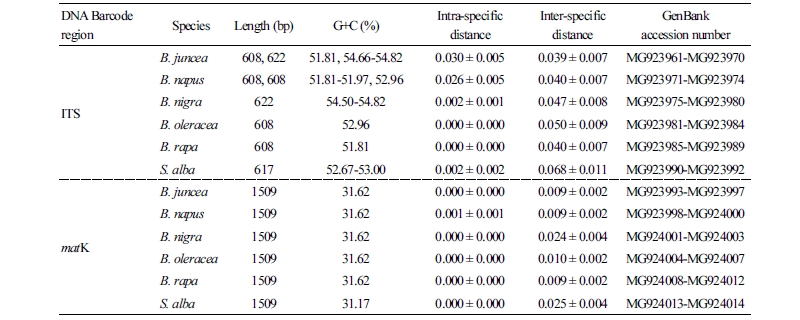
각 시료로부터 증폭된 ITS 염기서열을 분석한 결과, 갓과 유채는 두 가지 type의 염기서열이 나타났으며, 갓은 608 bp와 622 bp로 구성되었고, 유채는 608 bp의 서로 다른 두 가지 type의 염기서열로 구성되었다. 흑갓은 622 bp, 배추와 양배추는 608 bp, 백겨자는 617 bp로 구성되어 있음을 확인하였다. 갓과 유채에서 획득된 서로 다른 type의 염기서열이 sequencing 오류인지 확인하기 위해 NCBI GenBank BLAST 검색을 수행하였고, 각각 갓과 유채와 일치하는 염기서열이 존재하는 것을 확인하였다. 증폭산물의 G+C 비율은 전체적으로 51.81-54.82%로 나타났다. 본 연구를 통해 새로 제작한 primer 조합을 이용하여 증폭된 matK 유전자 염기서열을 분석한 결과, 모든 증폭산물은 1509 bp로 구성되어 있었고, G+C 비율은 31.17-31.62%로 확인되어 6종 모두 바코드 부위의 DNA 구조와 물리적 특성은 큰 차이를 보이지 않았다(Table 4).
종내 변이율을 분석한 결과, ITS 부위에서 가장 높은 종내 변이율을 보였으며, 갓, 유채, 흑갓, 양배추, 배추, 백겨자의 6종에 대한 종내 평균 변이율은 각각 0.030, 0.026, 0.002, 0.000, 0.000, 0.002으로 나타났다(Table 4). 갓과 유채에서 높은 종내 변이율이 나타난 것은 갓과 유채가 복이배체 식물로 두 가지 type의 염기서열이 존재하기 때문인 것으로 판단된다(Table 4 and 5). matK의 경우 유채에서 종내 평균 변이율이 0.001로 나타났지만, 나머지 6종은 종내 변이가 보이지 않았다. matK에서 유채의 종내 변이율이 0.001로 나타난 것은 유채의 AA genome 상에서 822 bp에서 T→A, 889 bp에서 C→A, 1132 bp에서 A→C로 바뀌는 3개의 염기치환이 있는 두 가지 type의 염기서열이 존재하기 때문인 것으로 판단된다(Table 6). 종간 변이율은 ITS에서 백겨자가 0.068로 가장 높았으며, 그 다음으로 양배추 0.050, 흑갓 0.047, 배추 0.040, 유채 0.040, 그리고 갓 0.039 순서였다. matK 유전자의 종간 변이율도 백겨자가 0.025로 가장 높았으며, 그 다음으로 흑갓 0.024, 양배추 0.010, 배추 0.009, 갓 0.009, 그리고 유채 0.009 순서였다. 획득된 염기서열은 NCBI GenBank에 업로드하였으며 각각의 accession number를 Table 4에 표기하였다.
배추속 식물의 종간 유연관계 분석
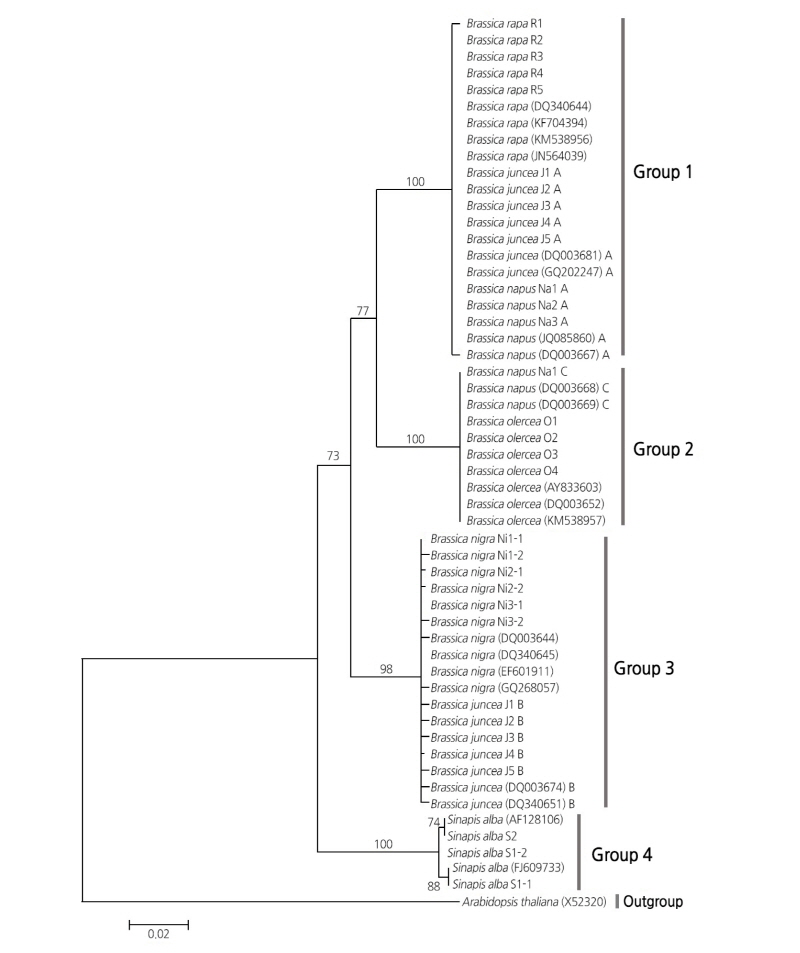
ITS 부위의 계통유연관계 분석 결과(Fig. 1), 독립적인 분기군을 형성한 백겨자와 Brassica속에 속하는 5종으로 크게 분기되었다. Brassica속은 genome type에 따라 분기군을 형성하였는데, 배추, 그리고 갓과 유채에서 분리된 AA genome이 하나의 분기군을 형성하였고(Group 1), 흑갓과 갓의 BB genome이 하나의 분기군을 형성하였으며(Group 3), 유채와 양배추의 CC genome이 또 하나의 분기군을 형성하여(Group 2) 총 3개의 group으로 나뉘었다. 그 중, AA와 CC genome이 BB genome보다는 더 가까운 유연관계에 있는 것으로 나타났다. 이는 핵 DNA의 CHS(chalcone synthase) 유전자를 이용하여 분석한 타 연구 결과와 일치한다(Chen et al., 2016). 그러나 종 별로 분기군이 형성되지 않고 각 genome type 별로 분기군이 형성되었기 때문에 Brassica속의 종 동정에는 적합하지 않은 것으로 판단된다.
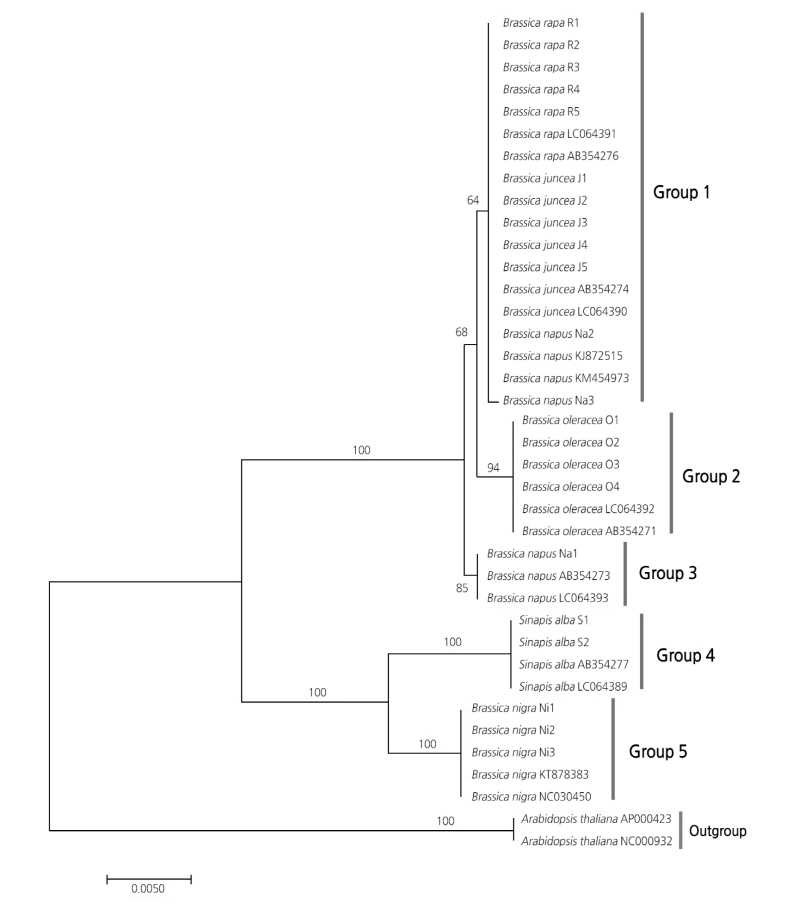
ITS 부위의 두 가지 type 및 copy를 수평 직선상에 배치하여 분석한 결과(Fig. 2), 총 6개의 group으로 분기군이 형성되었다. 각 분기군(Group 1-6)은 각각 단일종만으로 이루어져 있었으며, 그 중 백겨자는 기저에서 분지되어 독립적인 분기군을 형성하면서 Brassica속의 종들과 구분되는 형태를 보였다. 또한, Brassica속에서는 크게 두 개의 clade로 나뉘었는데, 첫번째 clade는 배추, 유채, 양배추로 구성되었고, 두번째 clade는 흑갓과 갓으로 구성되었다. AA genome과 CC genome이 BB genome보다 가까운 계통유연관계를 보이는 것은 ITS의 두 가지 type 부위를 수평 배치하지 않고 각각의 sequence로 작성한 계통수(Fig. 1)에서의 결과와 일치하였다. 그리고, 갓과 유채는 각각 AABB, AACC genome을 가지고 있으며 AA genome을 배추와 공유함에도 불구하고 갓, 유채, 배추는 분기군을 형성하지 않고 서로 paraphyly 관계에 있는 양상을 보였다. 반면에 BB genome을 공유하는 갓과 흑갓이 분기군을 형성하고 CC genome을 공유하는 유채와 양배추가 분기군을 형성하면서, BB genome간, CC genome간의 관계가 AA genome간의 관계보다는 좀 더 강한 유연관계에 있는 것으로 보인다(Fig. 2).
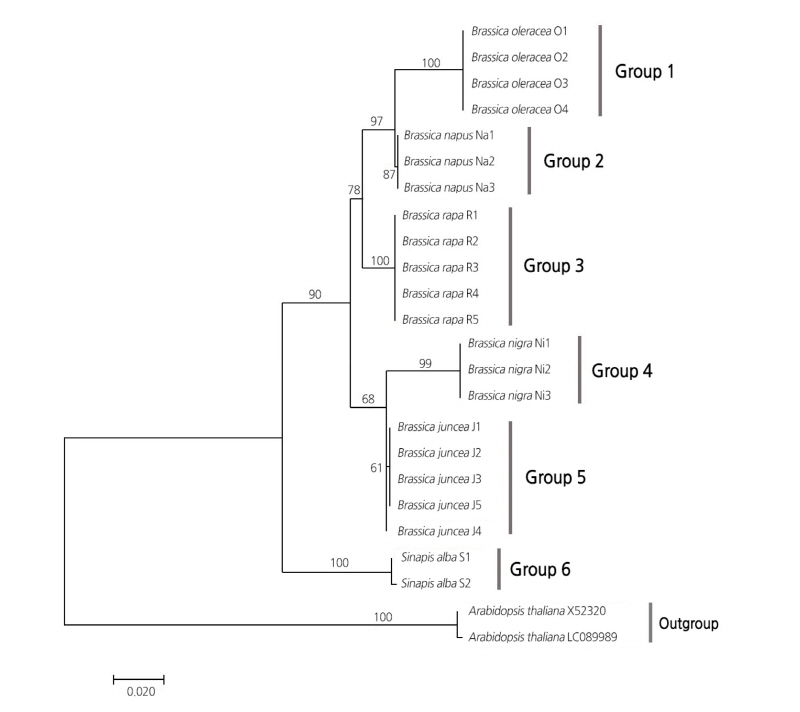
Fig. 2. Molecular phylogenetic tree inferred using the Maximum Likelihood method based on the Brassica ITS sequences arranged horizontally (the ITS sequence of the second genome type was situated right behind the final base of that of the first genome type). The numbers above branches indicate bootstrap values. Branches in less than 50% bootstrap values are collapsed.
matK 부위의 계통유연관계 분석 결과(Fig. 3), 백겨자를 포함하여 크게 두 개의 clade로 나뉘었다. 첫 번째 clade는 배추, 유채, 갓, 양배추로 구성되어 있었는데, 그 중 배추, 유채, 갓은 구분되지 않고 하나의 분기군(Group 1)을 형성하였으며 양배추만이 독립적인 분기군(Group 2)을 형성하였다. 그리고 유채 중 일부는 다른 분기군(Group 3)을 형성하는 결과를 보였다. 두번째 clade는 흑갓과 백겨자로 구성되어 있었다. 이러한 결과는 Li et al. (2017)이 보고한 Brassica속 식물의 전체 엽록체 genome 분석 결과, Lü et al. (2008)이 보고한 Raphanus 및 Brassica속 식물의 trnK/matK 염기서열을 이용한 Neighbor-joining tree 분석 결과, 그리고 Arias and Pires(2012)가 보고한 chloroplast genome 상의 intergenic Regions(rpl32-trnL, atpI-atpH, psbD-trnT, ycf6-psbM)의 분석 결과와 유사한 양상을 나타낸다. 따라서 배추과 식물의 chloroplast genome을 이용하여 유연관계를 분석한 여러 논문에서 보고된 바와 같이 배추, 양배추, 갓, 유채가 하나의 lineage를 이루고, 흑갓, 백겨자가 다른 lineage를 이루어 진화했기 때문에 chloroplast genome 상에서 갓, 유채, 배추 3종은 같은 분기군을 형성하는 것으로 판단된다. 또한, 이 결과로써 엽록체 유전자로는 배추, 유채, 갓의 뚜렷한 구분이 어렵다는 것을 확인하였다.
갓, 유채, 흑갓, 양배추, 배추와 백겨자 6종의 종간 유연관계 분석을 위하여 ITS와 matK 염기서열을 유합한 combined data의 적합성을 판단하고자 ILD test를 수행하였다. 그 결과, p-value가 0.03으로 ITS와 matK 부위가 homogeneous한 관계에 있다는 귀무가설을 기각하므로 combined data로서 적합하지 못한 것으로 판단되었다. 따라서 ITS와 matK 부위는 유합하여 분석하지 않았다.
종합적으로, ITS를 단순 분석한 것과 matK 유전자로는 분기군의 양상에서 Brassica 속 종들의 정확한 종 별 grouping이 어려웠으나, ITS 부위의 두 가지 type 및 copy를 수평 배치하여 분석했던 경우에서 Brassica 5종과 백겨자의 정확한 종 별 grouping이 가능하였다. 이로써 Brassica 5종과 백겨자의 정확한 종 동정과 종별 grouping을 위해서는 ITS 부위의 두 가지 type 및 copy를 수평배치하여 분석하는 것이 가장 바람직한 방법임을 확인하였다.
종 감별용 marker nucleotide 발굴
우리나라와 중국 약전의 개자 기원식물의 차이와 흑갓의 혼·오용 방지를 위한 종 감별용 marker로 활용할 수 있는 nucleotide 발굴을 위해, 본 연구에서 분석한 개자 및 운대자를 포함하는 6종 22개 시료로부터 증폭한 ITS, matK 염기서열과 NCBI GenBank의 기 보고된 갓, 유채, 흑갓, 양배추, 배추, 백겨자의 ITS, matK 염기서열을 확보하여 종내 비교와 종간 비교를 통해 종 특이적인 염기서열을 분석하였다.
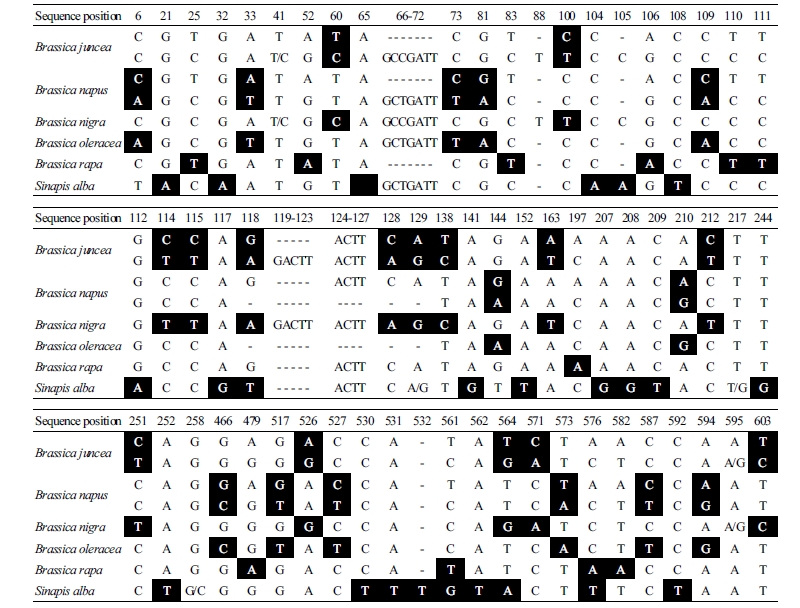
ITS 부위의 염기서열 분석 결과(Table 5), 백겨자 종 특이적인 염기삽입이 532 위치에서 확인되었으며, 염기치환이 26개 존재하였다. 배추속 식물인 나머지 5종은 종 특이적인 염기서열이 존재하지 않았으며, 총 3가지 type의 염기서열이 존재하였다.
배추(AA genome), 흑갓(BB genome), 양배추(CC genome)의 염기서열을 각각 A type, B type, C type으로 확정한 후 갓(AABB genome)과 유채(AACC genome)를 분석한 결과, 갓은 A와 B type, 유채는 A와 C type의 염기서열이 존재하였다. 각 type 별 특이적인 삽입/결실은 A type이 66-72위치, B type이 88, 119-123위치, C type이 124-127, 128, 129위치에 있었으며, 염기치환은 A type이 12개, B type이 17개, C type이 13개 존재하였다(Table 6).
종 특이적인 염기치환은 아니지만 Brassica속의 복이배체 종에서 두 가지 type의 염기의 조합으로 종을 동정할 수 있는 marker nucleotide를 탐색한 결과, 갓과 유채에서 각각 15개, 13개의 marker nucleotide가 확인되었다. 또한, 이배체 종들에서도 흑갓 15개, 양배추 13개, 배추 11개의 marker nucleotide가 확인되었다. 즉, ITS 부위 염기서열의 해당 위치의 염기 조합 정보를 이용하면 Brassica속을 종단위에서 동정할 수 있다는 결과를 얻었다.
본 연구 결과와는 다르게 Yang et al.(2016b)이 보고한 갓 품종 구분을 위한 ITS 분석 결과에서는 배추의 ITS 서열과 유사한 10품종과 흑갓의 ITS 서열과 유사한 5품종을 구분하였다. 이 연구 결과에서는 복이배체 식물의 두 가지 genome type 중 한 가지의 염기서열만이 나타나 있는데, sequencing sample의 수가 적어 각 genome이 가진 모든 ITS 염기서열이 확인되지 않은 것인지 여부를 추가적으로 확인해 볼 필요가 있다고 생각된다.
이와 관련하여 배추속 복이배체 식물인 갓, 유채, 그리고 에티오피아겨자(Brassica carinata)의 DNA 염기서열 분석 시에는 두 가지 type의 염기서열이 모두 관찰될 수 있기 때문에 cloning이 필수적이며, cloning 후에 PCR 증폭산물이 삽입된 white colony를 취할 때에도 충분한 수(7개-10개 이상)를 취하여 분석에 사용하는 것이 두 가지 type의 염기서열을 모두 얻기에 바람직한 방법으로 사료된다.
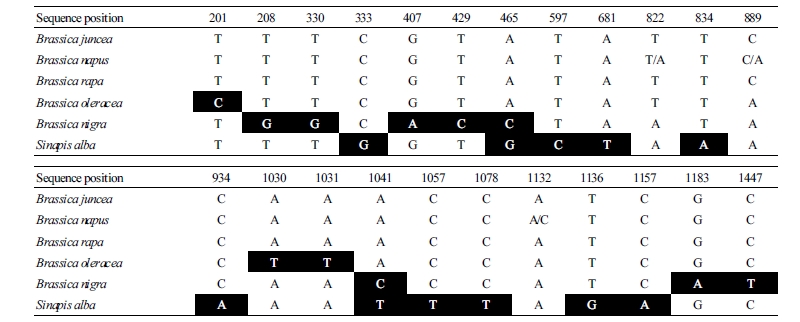
종 감별을 위한 matK 유전자의 염기서열 분석 결과(Table 6), 종 특이적인 삽입/결실은 없으며 백겨자, 흑갓, 양배추에서 염기치환이 각각 11개, 8개, 3개 존재하였다. 이 염기치환 부위를 marker nucleotide로 하여 백겨자, 흑갓, 양배추의 종 감별에 사용할 수는 있으나, 배추와 갓 그리고 일부 유채의 경우 염기서열상에 차이가 없어, 기 보고된 중국패모(Fritillaria thunbergii)와 달리 matK 유전자 염기서열만으로는 종 감별이 어려울 것으로 판단된다(Moon et al., 2018). 이것은 갓(AABB genome)과 유채(AACC genome)의 경우 모계 유전을 하는 chloroplast genome의 특성상 같은 모계, 즉 AA genome의 유전자를 획득하여 진화된 것으로 판단되며 기존에 보고된 다른 연구결과와 일치하였다(Li et al., 2017).
matK는 엽록체에 존재하는 유전자로 분자계통학적 연구에서는 상당히 높은 변이율을 보이나 PCR 증폭률이 낮은 어려움이 있어 rbcL과 결합하여 사용하길 추천하고 있다(CBOL Plant Working Group, 2009). 기존의 몇몇 연구에서 분류군에 따라 이들 두 조합만으로는 종 변별력이 떨어지는 문제점과 matK의 PCR 증폭의 어려움을 보고하며 추가적으로 다른 DNA barcode 부위의 필요성을 제기하였다(Hollingsworth et al., 2011; Ghahramanzadeh et al., 2013). 본 연구에서도 matK의 단일 바코드를 이용한 배추과의 종 감별은 어려운 것으로 판단되어, NCBI Genbank의 rbcL 유전자의 염기서열을 확인하였으나 matK 유전자 분석 결과와 같이 갓, 배추, 유채를 감별할 수 있는 변이가 나타나지 않았다(분석 결과 첨부 안함). 따라서 Brassica속 식물의 종을 감별하는 데 있어 matK +rbcL 조합의 DNA barcode는 적절치 않은 것으로 생각된다.
‘종의 합성’은 우장춘 박사가 배추와 양배추의 교배를 통해 기존에 존재하는 유채를 인공적으로 합성하여 종은 달라도 속이 같으면 새로운 식물을 만들 수 있다는 것을 최초로 증명한 것으로 흔히 ‘우장춘의 삼각형(U’s triangle)’이라 불린다(Nagaharu, 1935). 이 ‘우장춘의 삼각형’에 따르면 배추속에는 이배체 식물인 배추(AA genome), 흑갓(BB genome), 양배추(CC genome)가 있으며, 자연교잡에 의해 생성된 복이배체 식물인 갓(AABB genome), 유채(AACC genome), 에티오피아겨자(BBCC genome)가 있다. 복이배체 식물인 갓과 유채의 경우 자연교잡에 의해 서로 다른 genome에서 얻어진 ITS 염기서열이 존재하며 AA genome인 배추, BB genome인 흑갓, CC genome인 양배추의 3가지 염기서열 type을 비교해본 결과 우장춘의 삼각형을 따르는 결과를 얻었다.
따라서 ITS 부위는 배추속 식물의 우장춘의 삼각형을 설명할 수 있는 DNA barcode로, 복이배체 종의 ITS 부위에서 얻어지는 두 가지 type의 염기서열을 함께 분석한다면, chloroplast matK 유전자보다 정확하게 배추속 식물의 종 동정이 가능하기 때문에, 약재로 유통되는 갓과 유채의 종자인 개자와 운대자를 감별하는 데 효과적으로 이용할 수 있을 것으로 판단된다.