서 언
재료 및 방법
박테리아 생육환경 및 플라즈미드 벡터 구조
열 충격 형질전환 및 형질전환체 선발
Total RNA 추출 및 RT-PCR 분석
단백질 추출 및 Western blot 분석
결과 및 고찰
형질전환 및 형질전환체 선발
RT-PCR 분석을 통한 GFP 전사량 비교
Western blot 분석을 통한 GFP 단백질 발현량 비교
서 언
1970년 후반부터 유전자 재조합 기술을 이용하여 휴먼 인슐린(insulin) 생산을 시작으로 알부민(albumin), 아스파라기네이즈(asparaginase) 등 유용한 외래단백질들이 대장균(Escherichia coli)과 같은 박테리아 숙주세포에서 생산되어 왔다(Goeddel et al., 1979; Leader et al., 2008). 대장균은 다양한 벡터
(vector)를 이용한 형질전환 및 유전자조작이 간단하며 생장속도가 빨라 적은 비용으로 외래 단백질 생산이 가능하여 현재 가장 널리 사용되고 있는 숙주세포이다(Miroux and Walker, 1996; Šiurkus and Neubauer, 2011). 그러나 이와 같은 원핵세포에서는 진핵세포에서와 같은 복잡한 전이후변형과정(post-translational modification)이 일어나지 않고(Sambucetti et al., 1986), 페니실린 아실레이즈(penicillin acylase) 전구물질의 과발현으로 단백질이 불용화되기도 하며 폴딩(folding)이 되지 않아 재조합된 단백질이 정확한 생물학적 기능을 하지 못하는 단점이 있다(Xu et al., 2005).
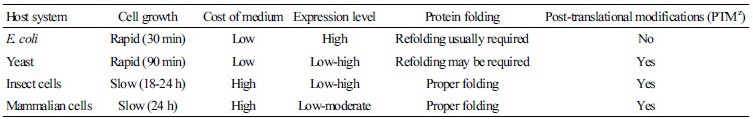
백신과 같은 인간 및 동물에게 유용한 의약품을 대량생산하기 위해서는 전이후변형과정이 가능한 숙주세포가 필요하며, 또한 복잡한 단백질 정제과정이 문제되어 왔다. 그래서, 1970년대 후반부터 진핵세포인 효모(Saccharomyces cerevisiae)를 숙주세포로 이용한 연구가 진행되어 왔고(Hinnen et al, 1978), 내독소가 없으며 대량생산체계가 쉽고 분비를 통한 단백질 분리 × 정제가 쉽다(Giga-Hama and Kumagai, 1999; Kumar and Singh, 2004)는 이점에도 불구하고, 효모의 세포벽 분해가 어렵고 벡터 선택의 폭이 좁은 단점 때문에 의약품에 사용되는 단백질 생산과 같은 특별한 목적이 아니면 숙주세포로 흔히 사용되고 있지 않다(Romanos et al., 1992). 최근에는 이를 극복하기 위하여 포유동물세포와 비슷한 전이후변형과정(post-translational modification)을 가지고 있으며 사람과의 종간 감염률이 극히 낮은 곤충세포를 숙주세포로 이용하고 베큘로바이러스(baculovirus)를 형질발현 벡터로 사용하여 외래단백질을 생산하고 있다(Smith et al., 1983; Jarvis, 2003). 하지만 본래의 단백질 활성과 가장 비슷한 재조합 단백질을 생산할 수 있는 포유동물세포는 생장속도가 느리고 비용이 많이 드는 것에 비해 외래단백질 발현율이 낮은 단점이 있다(Table 1).
단순한 일시적 외래유전자 과발현이라는 목적을 달성하기 위해서 적합한 숙주세포 선택과 형질전환방법, 형질전환율, 벡터 선택 등을 고려하여야 한다(Yin et al., 2007). 영구적 형질전환을 통해 연속적이고 안정된 생산을 위해 식물의 근두암종과 뿌리혹병을 일으키는 아그로박테리움(Agrobacterium tumefaciens)를 숙주세포로, 바이너리 벡터 시스템(binary vector system)을 이용하여 식물체의 영구적인 형질전환을 시작하였다(Bevan, 1984). 하지만 아그로박테리움은 생장속도가 느려 일반 벡터에 클로닝(cloning)하여 확인한 후, 다시 바이너리 벡터에 옮기는 과정을 거쳐야 하는 번거로움이 있다. 또한 카피(copy) 수가 적고 외래단백질 생산량이 낮다는 단점이 있다. 이를 극복하기 위해 Moon and Hefferon(2007)은 식물에 병을 유발하는 한 가닥의 원형 DNA로 된 콩황화오갈병 바이러스(bean yellow dwarf virus)를 벡터로 활용하여 형질발현율을 높이기도 하였다.
이렇게 여러 가지의 숙주세포가 개발되어 외래유전자 형질발현을 위해 많이 사용되고 있지만 여전히 특별한 목적을 완성하기 위해서는 더욱 다양한 숙주세포의 개발과 형질전환 방법의 개발 등은 의학, 생명공학산업 분야에서 요구가 높다. 그 첫 번째 이유가 경제적인 문제이다. 그 예로 가장 많이 시판되고 있는 대장균 DH5α(RH618, RBC, Taiwan)는 100µL(1 × 108) 10개 기준 십만 원 이상, 아그로박테리움 LBA4404(ElectroMAX, Invitrogen, USA)는 40µL(1 × 108) 5개 기준 오십만 원 수준으로 1회 형질전환용 숙주세포가 십만 원 이상으로 매우 비싸다. 이런 비싼 숙주세포를 대신할 수 있는 새로운 숙주세포의 개발이 필수불가결하게 되었다.
새로운 형질전환용 숙주세포가 되기 위한 특징은 외래단백질의 대량생산이 가능하고, 생육이 빠르며, 다루기 쉽고, 형질전환이 용이해야 한다. 이런 필요조건들을 고려해 볼 때 채소작물에 무름병을 야기하는 펙토박테리아(Pectobacterium caroto-vo-rum)가 주목을 받기 시작했다(Gallois et al., 1992; Hur et al., 2009; Abebe et al., 2016; Jayaraman et al., 2016). 펙토박테리아는 식물체 내에서 매우 빨리 자체증식하고 식물세포벽을 분해하여 단시간 내에 무름병징이 나타나는 특성을 가지고 있다(Gardan et al., 2003). 이는 짧은 시간 내에 쉽게 외래유전자의 대량 생산이 가능하고, 식물체 형질전환을 하기 위한 특별한 방법이 필요 없으며, 세포벽이 붕괴되어 있기 때문에 원심분리를 이용한 외래단백질의 분리가 매우 간편할 것으로 기대된다. 이런 새로운 형질전환용 숙주세포가 개발되어 상용화된다면 매우 큰 규모의 의학 및 생명공학산업 분야에서 보다 쉽게 저렴한 백신, 호르몬 및 유용한 단백질 등의 생산이 가능할 것으로 기대된다.
따라서 이 논문에서는 기존의 채소무름병을 유발하는 병원균의 병원성 관련 유전자의 분석 및 외래단백질의 단순한 형질발현의 유무가 아니라 Pectobacterium carotovorum subsp. carotovorum(Pcc21)의 새로운 형질전환용 숙주세포로써의 이용 가능성을 검증하기 위하여 대표적인 상용화 숙주세포(대장균 DH5α 및 아그로박테리움 LBA4404)와의 외래단백질 발현의 효율을 정량적으로 비교하였다. 이 연구에서는 프로모터와 인핸서 등의 벡터에 따른 발현 차이를 고려하지 않기 위해 제품화된 클론텍(Clontech, USA)의 pGFPuv(Lac::GFPuv) 벡터와 아그로박테리움 형질발현에 최적화된 pCAMBIA2300(35S::smGFP)을 이용하였다. 또한 total RNA와 단백질을 추출하여 RT-PCR과 Western blot 분석을 통해서 Pcc21과 가장 많이 이용되고 있는 DH5α 및 LBA4404 숙주세포 간의 GFP 발현 정도를 비교 × 분석하여 펙토박테리아의 새로운 숙주세포로써의 효율성을 확인하였다.
재료 및 방법
박테리아 생육환경 및 플라즈미드 벡터 구조
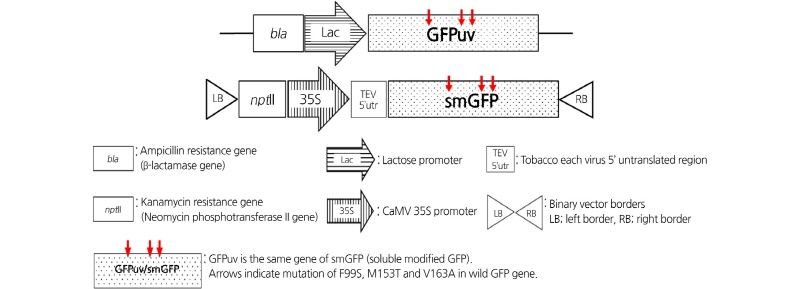
펙토박테리아(Pectobacterium carotovorum subsp. carotovorum) Pcc21(농촌진흥청 유해생물과 제공)의 형질전환용 숙주세포로써의 가능성을 평가하기 위해 현재 시판되고 있는 Escherichia coli인 DH5α(RBC, Taiwan)와 Agrobacterium tume-faciens인 LBA4404(Invitrogen, USA)를 pGFPuv(Clontech, USA)와 pCAMBIA2300(한국생명공학연구원 그린바이오연구센터 제공)을 형질발현 벡터로 사용하였다. pGFPuv는 락토즈 프로모터와 암피실린(ampicillin) 항생제 저항성 유전자 β-lacta-mase (bla) 유전자를 가지고 있으며, pCAMBIA2300은 콜리플라워 모자이크 바이러스(cauliflower mosaic virus) CaMV 35S 프로모터에 의해 조절되는 바이너리 벡터로 카나마이신(kanamycin) 항생제 저항성 유전자 neomycin phosphotransferase II(nptII) 유전자를 가지고 있다. GFPuv와 smGFP 유전자는 같은 유전자이고 Davis and Vierstra(1988)은 야생형 GFP가 애기장대와 같은 쌍자엽식물에서 이상한 스플라이싱(splicing)이 일어나 단백질이 불용성으로 되는 것을 해결하기위해 야생형 GFP 아미노산서열 중에서 99번의 페닐알라닌이 세린으로(F99S), 153번의 메티오닌이 트레오닌으로(M153T), 163번의 발린이 알라닌으로(V163A) 돌연변이하여 ‘soluble modified’ smGFP로 명명하였고 클론텍에서는 GFPuv로 명명하였으며 UV 조사 시 더 밝은 형광을 나타낸다(Davis and Vierstra, 1988).
RT-PCR 및 Western blot 분석 방법에 의한 GFP 형질발현 정도를 측정하기 위해 각 숙주세포의 특성을 고려해 최적 생장온도와 시간에서 배양하였다(Pcc21-27°C, 48시간; DH5α-37°C, 18시간; LBA4404-29°C, 72시간). 밀리리터당 콜로니 형성 단위(cfu·mL-1)는 적절한 항생제가 포함된 액체 LB배지에서 600nm에서의 광학밀도(optical density; OD)가 0.45가 될 때까지 진탕 배양한 후, 이 박테리아 현탁액 10µL를 각각 10,000, 20,000, 40,000배 희석하여 적절한 항생제가 포함된 고체 LB배지에 도말 후 배양하여 콜로니 수를 측정하였다. 10,000과 20,000배 희석 배지에서는 세포 수가 많아 박테리아 층(bacterial lawn)을 형성하여 콜로니 수를 측정할 수 없었으며, 40,000배 희석 배지에서 수를 측정하였다. Pcc21은 200개, DH5α는 220개, LBA4404는 260개의 콜로니가 생성되었다. 평균 10µL당 227개 콜로니가 형성되었으며 여기에 희석배수와 mL 단위로 환산한 결과 OD600nm = 0.45는 9 × 108cfu·mL-1와 비슷한 세포수로 예측하였다.
열 충격 형질전환 및 형질전환체 선발
대장균 DH5α(RBC, Taiwan)는 현재 시판되고 있는 열 충격 형질전환용 숙주세포(competent cell)를 사용하였고, Panja et al.(2006)의 방법 중 배지조성을 변형하여 Pcc21과 LBA4404(Invitrogen, USA)를 열 충격 형질전환 숙주세포로 제조하였다(Panja et al., 2006). 먼저 frozen cell stock에서 콜로니를 배양하여 1%의 2M Mg2+ stock(1M MgCl2, 1M MgSO4)이 포함된 LB 배지 2mL에 기초배양한 후 50mL에서 OD600nm = 0.6이 될 때까지 배양 후 얼음에서 차게 식힌 50mL 튜브에 넣어 4°C, 5,000rpm에서 5분간 원심분리하였다. 차가운 0.1M CaCl2로 두 번 씻어주었다. 1mL 0.1 M CaCl2에 다시 현탁하고 100µL씩 분주하여 액체질소로 급랭한 후 -70°C에 보관하였다. DH5α와 Pcc21에는 pGFPuv, LBA4404에는 pCAMBIA로 형질전환한 후 숙주세포의 형질전환 효율을 확인하였다.
온도 차이를 이용한 열 충격 형질전환 방법을 사용하였다(Yoshida and Sato, 2009). 형질전환용 숙주세포에 GFPuv 또는 CAMBIA2300의 1µg의 plasmid DNA(pDNA)를 넣고 얼음에 30분간 둔 후 42°C에서 30초간 열 충격을 가하였다. 다시 얼음에서 10분간 식혀준 후 액체 LB배지 1mL를 넣고 최적의 생육온도에서 2시간 동안 진탕배양하였다. 7,000rpm에서 1분간 원심분리하여 세포를 모은 후 멸균수 100µL를 넣고 다시 현탁하여 Pcc21과 DH5α는 암피실린(100µg·mL-1), LBA4404는 카나마이신(50µg·mL-1)을 함유한 고체 LB배지에 도말하여 배양하였다.
형질전환된 콜로니를 물에 희석한 후 4µL의 박테리아 현탁액을 주형으로 GFP 유전자 특이적 프라이머(primer)와 1X GO Taq® Green Master Mix(Promega, USA)로 PCR하였다. 반응 조건은 I단계 94°C-5분, II단계 25cycle; 94°C-30초/55°C-30초/ 72°C-30초, III단계 72°C-5분으로 실시하였다. 선발된 형질전환 콜로니는 pDNA 분리 후 제한효소(HindIII/EcoRI) 처리를 하여 형질전환체를 재확인하였다.
Total RNA 추출 및 RT-PCR 분석
형질전환 된 박테리아를 적절한 항생제가 포함된 액체 LB배지 20mL에 넣은 후 적당한 온도에서 250rpm으로 진탕배양하여 OD600nm = 0.45가 되면 박테리아를 수확한 후, 각 박테리아에서 GFP 전사율을 비교하기 위하여 total RNA를 추출하고 cDNA 합성을 하여 GFP 유전자 특이적 프라이머와 인터널 컨트롤로 사용하기 위한 16s rRNA 유전자 프라이머를 사용하여 PCR을 실시하였다. Total RNA는 Trizol® Reagent(Invitrogen, USA)를 사용하여 매뉴얼에 제시된 방법으로 추출 후 2µL(1U·µL-1)의 RNase free DNase(Promega, USA)로 30분간 처리한 후 total RNA에 gDNA가 없는 것을 PCR로 확인하였다. 분광분석기(S-3100, SCINCO, Korea)와 LabPro® Plus software로 total RNA를 정량 하였다. SuperScript™III first strand synthesis system(Invitrogen, USA)을 사용하여 cDNA를 합성하였다. 10µL의 RNA/프라이머 mix(1µg total RNA, 물, random hexa-mer, 0.5mM dNTPs mix)를 60°C에서 5분간 denaturation 후 4°C에서 2분간 반응시킨 후 10µL의 cDNA synthesis mix(1X buffer, 5mM MgCl2, 10mM DTT, 40 U RNaseOUT, 200 U SSIII-reverse transcriptase)를 넣고 25°C에서 5분, 50°C에서 60분 동안 cDNA합성을 하여, 70°C에서 15분 동안 종결반응이 이루어진 후 4°C에서 일시 보관하였다.
2µL cDNA를 주형으로 GFP 유전자 특이적 프라이머(GFPf; 5'-GAG GGT GAA GGT GAT GCA ACA TAC-3', GFPr; 5'-CTC ATC CAT GCC ATG TGT AAT CCC-3')를 이용하여 25 cycle(denaturation 94°C-2분, annealing 55°C-30초, exten-sion 72°C-30초)의 PCR(TP600, TAKARA, Japan)을 실시하였다. 16s rRNA는 인터널 컨트롤(internal control)로 이용하기 위하여 세 박테리아의 gDNA를 NCBI(National Center for Biotechnological Information)에서 Basic Local Alignment Search Tool(BLAST)을 이용하여 공통되는 부분을 찾은 후 프라이머를 제작하였다(16S rRNAf; 5'-TTA GAT ACC CTG GTA GTC CAC G-3', 16S rRNAr; 5'-GTA AGG GCC ATG ATG ACT TGA C-3'). 실험에 사용된 프라이머는 PrimerQuestsm(idtDNA, USA; www.idtdna.com) 소프트웨어를 사용하여 디자인하였다. PCR 후 1% 아가로오즈 젤에서 50V에서 50분간 전기영동(Mupid-EX, Advance, Japan)을 실시하였다. 이티디움브로마이드(ethidiumbromide, 1µg·mL-1)로 30분간 염색한 후 UV로 확인하였다. Image J software™를 사용하여 각각의 전사량을 노머라이즈(normalize)하였고 인터널 컨트롤을 이용하여 GFP 전사율을 비교 분석하였다.
단백질 추출 및 Western blot 분석
단백질 발현량을 비교하기 위해 Pcc21, DH5α 및 LBA4404가 OD600nm = 0.45일 때 수확하여 수용성 단백질을 추출하였다. 200µL의 셀 라이시스 버퍼(cell lysis buffer; 100mM NaCl, 25mM Tris·HCl pH 8.0)에 100U·mL-1 DNase, 200µg·mL-1 lysozyme을 넣고 섞어 준 후 얼음에서 20분간 두면서 vortex(15초 × 5회)를 한 후 12,000rpm, 4°C에서 5분간 원심분리하여 상징액을 새 튜브로 옮기고 브래드포드 시약(Bradford reagent, PIERCE, USA)을 이용해 변형된 Moon and Hefferon(2007) 방법으로 단백질을 정량하였다(Moon and Hefferon, 2007).
GFP 단백질 발현량을 비교하기 위해 Western blot 방법을 이용하였고, 20µg의 단백질에 5X sample buffer(50mM Tris·HCl pH 6.8, 100mM β–mercaptoethanol, 2% SDS, 0.1% bromophenol blue, 10% glycerol)를 넣은 후 85°C에서 10분간 디네츄레이션(denaturation)을 실시하였다. 12% 폴리아크릴아마이드 젤(polyacrylamide gel, 가로 × 세로; 10cm × 10.5cm)에서 20mA, 2시간 동안 전기영동(SE 260 Mighty Small II, Hoefer, USA)을 실시하였다. 젤에 있는 단백질을 1X 트랜스퍼 버퍼(transfer buffer; 39mM glycine, 48 mM Tris, 0.037% SDS, 20% methanol)를 이용하여 PVDF membrane에 blotting을 실시하였다(TE42, Hoefer, USA). 첫 번째 항체 Rabbit anti-GFP IgG(Thermo, USA)를 1:5,000, 두 번째 항체 Goat anti-Rabbit IgG (Thermo, USA)를 1:50,000으로 1% skim milk 용액에 희석하여 순차적으로 30분씩 처리를 하고, 처리가 끝날 때마다 PBST (PBS, 0.1% Tween20)로 씻어주었다(15분 × 3회). 기질은 SuperSignal® West Femto(Thermo, USA)를 이용하여 X-ray 필름(film)에 감광하였다. Image J software™를 이용하여 노머라이즈를 실시한 후 숙주세포에 따른 단백질 발현량을 비교 × 분석하였다.
결과 및 고찰
형질전환 및 형질전환체 선발
이 실험에 사용된 형질발현 벡터 구조는 Fig. 1에서 정리하였고, 펙토박테리아의 감자무름병징과 현미경에서 관찰된 구조는 Fig. 2A와 2B에서 볼 수 있다. pGFPuv(Clontech, USA) 벡터를 CaCl2 처리에 의해 제조된 형질전환용 숙주세포에 열 충격 방법으로 형질전환하여 적절한 항생제가 포함 된 고체 LB배지에서 배양하였다. 먼저 UV를 조사하여 GFP 특유의 녹색 형광을 띄는 콜로니를 확인하였다(Fig. 2C). 또한 PCR하여 612bp에서 밴드를 확인하였다. 확인된 콜로니는 Wizard Plus SV Minip-rep Kit(Promega, USA)를 사용하여 pDNA를 분리 후 HindIII와 EcoRI 제한효소 처리를 하여 최종 선발하였다(data not shown). 선별된 콜로니를 적정 항생제가 포함된 액체 LB배지에서 같은 세포수(OD600nm = 0.45 = 9 × 108cfu·mL-1)로 배양한 후 수확하여 -20°C에서 RT-PCR과 Western blot 실험을 실시하였다.
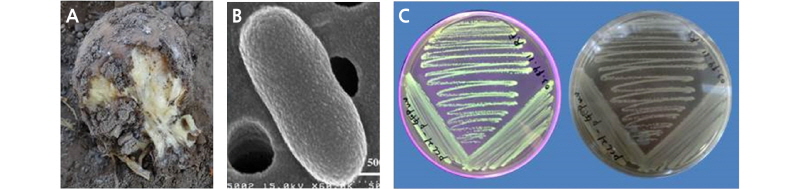
Fig. 2. Potato soft rot disease and Pectobacterium carotovorum. Erwinia carotovora was recently renamed to Pectobac-terium carotovorum. A. Symptoms of potato soft rot disease from ‘Disease and pest control of potatoes before and after harvest’ from National Institute of Crop Science, Rural Development Administration; B. Typical P. carotovorum from Moreau et al. (2007); C. pGFPuv-transformed Pcc21 under UV (left) and white light (right). Both A and B are reprinted with permission.
RT-PCR 분석을 통한 GFP 전사량 비교
pGFPuv 형질전환된 박테리아에서 total RNA를 추출하여 RT-PCR한 결과 예상하였던 612 bp에서 GFP 전사량(Fig. 3A upper)과 인터널 컨트롤로 사용한 16s rRNA 유전자의 전사량(Fig. 3A lower)을 확인하였다. Image J Software™를 사용하여 노머라이즈를 실시한 후 각 박테리아에서의 GFP 상대적 발현량을 비교하였다(Fig. 3B). GFP/16s rRNA를 보면 Pcc21은 1.12, DH5α는 1.06으로 Pcc21이 DH5α보다 0.06만큼 높게 나타났으며, LBA4404는 0.01로 다른 두 박테리아에 비해 매우 낮은 수치를 나타내는 것으로 보아 발현량이 매우 적었다. 또한 LBA4404는 최적 생장 온도가 DH5α보다 낮은 29°C에서 72시간 이상으로 배양함으로 생장속도가 매우 느렸다. 모두 그램 음성인 세 박테리아의 최적의 생육 온도와 충분한 시간으로 배양하여 같은 세포수(9 × 108cfu·mL-1)로 실험을 하였기 때문에 생장 속도의 문제이기보다 전사율이 낮은 것으로 판단된다. 이 결과를 통해서 Pcc21은 DH5α와 비슷한 수준으로 원하는 외래유전자를 발현시킬 수 있으며 LBA4404보다 생육 속도가 빠르고 발현율이 매우 높아 새로운 숙주세포로서의 활용 가능성을 확인하였다.
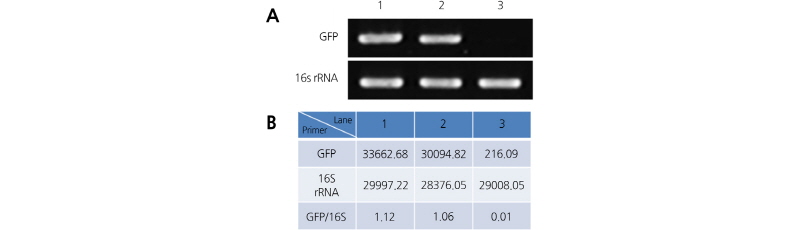
Fig. 3. Semi-quantitative comparison of transcription levels from Pcc21, DH5α and LBA4404 by RT-PCR. A. After cDNA was synthesized, GFP transcript was amplified using GFP gene-specific primers. 16s rRNA was used as the internal control. Lane 1: Pcc21, Lane 2: DH5α, Lane 3: LBA4404, B. The transcript signal for GFP was normalized using Image J SoftwareTM.
Western blot 분석을 통한 GFP 단백질 발현량 비교
일반적인 유전자 형질 발현에서 유전자 카피수가 많으면 mRNA가 많이 생성되고 단백질의 양도 많아질 것이라 기대된다. 하지만 너무 과도한 외래단백질의 발현은 유전자침묵(gene silencing)이 일어나 mRNA 양이 급감하고 결국 단백질량이 적어 형질이 발현되지 않는 것과 같은 경우와 유전자 카피수가 많아서 RNA량이 많음에도 불구하고 전이단계에서의 어떤 문제로 인해 단백질이 적은 경우가 있다는 보고가 있다(Moon and Hefferon, 2007). 따라서 이번 실험에서는 각 박테리아에서의 단백질 발현량을 알아보기 위해 Western blot 방법을 실시하였다.
박테리아 단백질을 SDS-PAGE 후 염색하여 정량의 단백질이 사용되었음을 확인하였으며(Fig. 4A upper), Western blot 방법으로 GFP 단백질 발현량을 비교하고(Fig. 4A lower), Image J Software™를 사용하여 노머라이즈하였다(Fig. 4B). RT-PCR에서 확인한 것과 마찬가지로 Pcc21은 23,663.87, DH5α는 16,629.51로 Pcc21에서 GFP 단백질은 DH5α보다 약 30% 높게 나타났다. 또한 LBA4404에서의 GFP는 거의 확인되지 않는 수준이었다. 이 결과는 Pcc21이 외래유전자의 mRNA 전사뿐만 아니라 단백질 발현에 있어 현재 많이 쓰이고 있는 숙주세포인 E. coli DH5α 만큼 효과적이고, 식물에 일시적·영구적 형질전환을 위한 숙주세포인 A. tumefaciens LBA4404에 비해 훨씬 좋다는 것을 확인하였다.
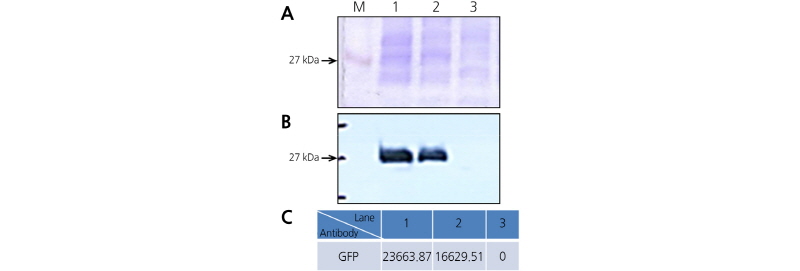
Fig. 4. Modified GFP protein expression was examined by immunoblot analysis. (A) Proteins (20 µg) were separated on 12% polyacrylamide gels and stained with Coomassie brilliant blue. M: protein marker, Lane 1: Pcc21, Lane 2: DH5α, Lane 3: LBA4404. (B) After transferring proteins, PVDF membranes were probed with Rabbit anti-GFP primary antibody (1: 5,000) and Goat anti-rabbit IgG secondary antibody (1:50,000). SuperSignal® West Femto Kit was used for chemi-lu-minescent detection. (C) The signal of GFP was normalized using Image J SoftwareTM.
LBA4404는 낮은 카피수의 숙주세포로 pDNA의 복제가 잘 되지 않고, 세포의 생장속도가 느린 것으로 알려져 있고(Shou et al. 2004; Moon and Hefferon 2008) 이번 실험결과와 일치한다. 또한 9 × 108 cfu·mL-1 (OD600nm = 0.45)에서 Pcc21은 27°C-48시간으로 식물에 접종할 수 있는 LBA4404(29°C-72시간)보다 생육 온도는 낮지만 생육 시간이 짧고, 전사·전이율이 훨씬 높았다. 따라서 이 실험의 결과 감자와 배추 등 채소류의 무름병을 유발하는 병원균인 펙토박테리아 Pcc21이 외래유전자의 발현을 위한 유용한 숙주세포 중 하나가 될 수 있다고 생각된다.