서언
재료 및 방법
실험 재료 및 저장 전처리
호흡률 및 에틸렌 발생률 측정
필름 포장 내 가스 농도 및 생체중 감소율 측정
경화 특성 분석
품질 분석
통계처리
결과 및 고찰
호흡률 및 에틸렌 발생률
필름 포장 내 가스 농도 및 생체중 감소율의 변화
경화 특성의 변화
품질 변화
서언
최근 아스파라거스(Asparagus officinalis L.)는 건강에 유익한 기능성 성분이 다량 함유되어 있어 국내 소비량이 증가하는 추세이다(Lee et al., 2015). 그러나 아스파라거스는 수확 이후 빠른 호흡 작용(Bhowmik and Matsui, 2003; Brash et al., 1995) 과 에틸렌 노출의 영향을 받게 되어 리그닌화 촉진(Liu and Jiang, 2006) 및 엽록소 감소(Wang et al., 1971) 등의 피해가 보고되 고 있다. 그리고 국내 유통 환경이 부적절하여 이로 인한 유통 중 손실이 발생하고 있어 수확 후 관리 기술이 필요하다고 판단 된다(Lee, 2015).
이러한 수확 후에 발생되는 품질 저하를 억제하기 위해 UV-C 조사, 열수 처리, CO2 처리, MA 저장 등과 같은 다양한 전처 리 기술이 보고되었다. UV-C 조사는 포도의 잿빛곰팡이병 발생을 경감시키고(Choi, 2012), 브로콜리에서는 엽록소 분해 효 소의 활성을 억제하여 황화 지연에 효과를 보였다(Costa et al., 2006). 열수 처리는 감에서 과피 흑변, 해충 사멸과 부패 억제 효 과를 보였고(Lee et al., 2010), 박피한 토란에서도 관능적 품질 유지와 갈변 억제 효과를 나타내었으며(Chang and Kim, 2015), 아스파라거스에서는 phenylalanine ammonia-lyase(PAL)와 peroxidase(POD) 활성을 억제하여 경화 지연의 효과가 보고된 바 있다(Chiu and Sung, 2013). CO2 처리는 복숭아에서 에틸렌의 생합성을 억제하여 부패 및 숙성을 억제하고(Choi et al., 2007), 딸기의 세포와 세포 사이의 응집력을 증가시켜 경도 유지에 효과가 있는 것으로 보고되었다(Harker et al., 2000). 그리 고 수확 후 유통 중 품질 저하를 억제할 수 있는 MA 저장 및 포장 기술이 여러 작물에 적용되었는데(Cho et al., 2009; Park et al., 2014), 아스파라거스는 MA 저장으로 색 변화와 수분 손실 등 품질 유지 효과가 보고된 바 있다Ga(riepy et al., 1991; Yoon et al., 2016). 그러나 MA 저장은 포장 내의 저장성을 향상시키는 고농도 CO2 및 저농도 O2 조건 이외에 품질 저하를 유도하는 에틸렌의 축적을 가져올 수 있다(Yun and Lee, 1996). 따라서 기존에 일반 저장 조건에서 그 효과가 입증된 여러 가지의 전처 리 기술이 MA 저장 조건에서는 상이한 결과를 가져올 수도 있을 것이다
이에 본 연구는 아스파라거스의 MA 저장 및 관행 저장 조건에서 몇 가지 전처리가 저장 중 경화 진행 및 품질 변화의 효과를 알아보기 위해 실시하였.
재료 및 방법
실험 재료 및 저장 전처리
본 실험에서 사용한 아스파라거스(‘Wellcome’, Asparagus officinalis L.)는 강원도 양구 지역에서 재배된 것으로 직경 1.5 ±1.1cm로 선별하였다. 저장 방법은 MA 저장을 위해 산소투과율이 10,000 cc·m-2·d-1·atm-1인 OTR 필름[PP(Polypropylene), Dae Ryung precision packaging industry Co., Ltd., Korea]을 사용하였고, 유공 필름(Ø 0.5cm, 4 holes/100cm-1)으로 포장한 관행 저장 방법을 두었다. 전처리는 열수 침지, UV-C 조사, CO2 전처리, CO2 주입, 그리고 대조구인 무처리를 두었는데, CO2 주입 처리의 경우 MA 저장에서만 시행하였다. UV-C 조사는 Costa et al.(2006)의 방법을 참고하여 15kJ·m-2로 실시하였다. 열수 침지 처리는 Chiu and Sung(2013)의 방법을 참고하여 48°C에서 4분 동안 실시하였다. CO2 전처리 및 주입의 처리 농도 는 Corrigan and Carpenter(1993) 방법을 참고하여 액화 CO2로 60%의 농도를 처리했고, CO2 전처리는 밀폐 용기에 2시간 동 안 처리한 후 포장했다. CO2 주입 처리는 OTR 필름으로 포장한 이후 액화 CO2를 60%의 농도로 주입하였다. 이들 실험구는 4°C와 상대습도 85% 조건에서 저장하였다.
호흡률 및 에틸렌 발생률 측정
호흡률 및 에틸렌 발생량은 무처리, UV-C, 그리고 열수 처리를 대상으로 측정하였다. 이들 처리는 각각 78mL 밀폐 용기에 아스파라거스를 담아 20°C에서 1시간 동안 두었다. 이후 호흡률은 infrared sensor(Checkmate, PBI, Denmark)로 에틸렌 발생 량은 gas chromatography(GC-2010, Shimadzu, Japan)로 측정하였다(Park et al., 2000).
필름 포장 내 가스 농도 및 생체중 감소율 측정
저장 중 필름 내 가스 농도 측정은 MA 저장에서만 시행하였고 CO2, O2, 그리고 에틸렌 농도를 측정하였다. CO2와 O2는 infrared sensor 그리고 에틸렌 농도는 gas chromatography로 측정하였다. 생체중 감소율은 초기 중량에서 감소하는 중량을 백 분율로 표현하였다.
경화 특성 분석
경도, 리그닌 함량, PAL과 POD 활성은 화두(상단부에서 5cm 아랫부분)와 줄기(하단부에서 8cm 윗부분)로 나누어 측정하 였다.t
경도의 prove는 No. 5(Ø 3mm)를 이용하여 rheometer(Model co-mpac-100, Japan)로 측정하였다. 리그닌 함량은 Liu and Jiang(2006) 방법을 수정하여 실시하였는데, 화두와 줄기 각 3.0g의 생체를 15mL의 95% ethanol에 넣고 균질화하여 원심분리 (12,000g, 4°C, 10분)하였다. 침전물은 ethanol과 hexane(1:2, v:v) 혼합액으로 세척한 다음 침전물에 acetyl bromide와 acetic acid(1:3, v:v) 혼합액을 넣어 상징액을 UV-VIS spectrophotometer(UV mini model 1240, Shimadzu, Japan)로 280nm에서 흡광도를 측정하여 Morrison(1972) 방법으로 정량분석하였다.
Phenylalanine ammonia-lyase(PAL) 활성을 측정하기 위해 화두와 줄기의 생체를 각각 3.0g씩 9.0mL의 boric acid buffer(pH 8.8, 0.2M boric acid, 1mM polyvinylpolypyrolidone(PVPP), 1mM EDTA, 그리고 5mM β-mercaptoethanol)에 넣어 균질화 하고 원심분리(15,000g, 4°C, 20분)하여 상징액을 채취하였다. PAL 활성은 상징액에 0.02M L-phenylalanine과 buffer 용액을 첨가하여 37°C 30분 동안 반응시킨 후 UV-VIS spectrophotometer를 이용하여 290nm에서 흡광도를 측정하여 ΔA290 ·g-1 FW/h 로 표현하였다(Koukol and Conn 1961; Liu and Jiang, 2006).
Peroxidase(POD) 활성은 Liu and Jiang(2006)의 방법을 수정하여 측정하였는데, phosphate buffer(pH 6.0, 50mM phosphate acid, 1mM PVPP, 1mM EDTA, 그리고 15mM β-mercaptoethanol) 9.0mL에 3.0g의 생체를 넣고 균질화하고 원심분리 (15,000g, 4°C, 20분)하여 상징액을 얻었다. POD 활성 값은 상징액에 25mM guaiacol과 0.1M H2O2 용액을 첨가하여 24°C에 서 2분 동안 반응시킨 후 UV-VIS spectrophotometer를 이용하여 470nm에서 흡광도를 측정하여 ΔA470·g-1 FW/h 로 표현하였 다(Liu and Jiang, 2006).
품질 분석
외관상 품질과 이취는 Jeong et al.(2010)의 방법을 참고하여 숙련된 5명의 패널에 의한 관능평가로 조사했고, 1부터 5까지 등급으로 평가하였다. 외관상 품질의 등급은 저장 전 가장 좋은 상태를 5점, 품질 유지 상태를 3점, 그리고 완전 폐기 상태를 1 점으로 하였다. 이취의 평가 등급은 이취가 매우 적을 경우 1점, 이취가 매우 심한 수준을 5점으로 하였다. 가용성 고형물 함량 은 굴절당도계(PAL-1, Atago, Japan)를 이용하여 측정하였으며 Brix로 나타내었다. 색도는 아스파라거스의 화두와 줄기 부분 을 색차계(CR-400, Minolta, Japan)를 이용하여 측정하였으며, hue angle 값으로 황화정도를 나타냈다. 아스파라거스 엽록소 함량은 화두와 줄기 부분을 각각 1.0g을 10.0mL methanol에 48시간 동안 4°C에서 침지시킨 후 UV-VIS spectrophotometer 를 이용하여 642.5nm와 660nm에서 흡광도를 측정하였다(AOAC, 1997; Baek et al., 2014).
통계처리
실험 결과의 통계분석은 Microsoft Excel 2013 program과 SAS Version 9.0(SAS institute Inc, Cary, NC, USA)를 이용하였다.
결과 및 고찰
호흡률 및 에틸렌 발생률
전처리 직후 아스파라거스의 호흡률 및 에틸렌 발생률은 무처리구와 UV-C처리구에 비해 열수처리구에서 가장 낮았다 (Figs. 1A and B). 이는 기존에 알려진 아스파라거스의 호흡률인 270mg·kg-1·hr-1(Kays and Paull, 2004)와 에틸렌 발생률 2.1-4.9μL·kg-1·h-1 (Haard et al., 1974)와 유사한 결과였다. 저장 전처리에 따른 호흡률 및 에틸렌 발생률은 열수 처리로 감소하 였는데, Tian et al.(1997)은 적절한 열수 처리는 브로콜리에서 에틸렌 receptor와 에틸렌 생합성과 관련된 효소의 손상으로 에 틸렌 발생과 호흡이 억제된다고 보고하였다.
필름 포장 내 가스 농도 및 생체중 감소율의 변화
MA 저장중 포장 내 CO2농도는 60% CO2 주입 처리구에서는 저장 1일차부터 5일차까지 점차 감소하여 8.0-11.0%까지 저 하되었다. 나머지 처리구는 저장 1일차에 급격히 증가하여 모든 처리구에서 CO2 주입 처리구와 유사한 8.0-11.0%의 농도를 보이며 저장 종료일까지 그 수준을 유지하였다(Fig. 2A). 모든 전처리구의 CO2 농도는 아스파라거스 MA 조건의 CO2 농도 범 위인 5.0-12.0%를 유지하였고(Kader, 2002), 무처리와 비교하였을 때 전처리에 따른 호흡량 변화에 영향을 미치지 않았던 것 으로 판단된다. 포장 내 O2 농도는 CO2 주입 처리에서 60%에 달하는 고농도 CO2 주입으로 인하여 저장 시작일에 6.0%를 보였 으나, 5일차 이후 증가하여 저장 중 15.0% 내외의 농도를 유지하였고, 나머지 처리는 저장 1일차에 7.0-9.0%까지 감소하였으 나, 5일차 이후 증가하여 15.0% 내외의 농도를 저장 종료일까지 유지하였다(Fig. 2B). 일반적으로 저장 중 아스파라거스의 최 소 O2 허용 농도는 5.0%인데(Kader, 2002), 본 실험에서 모든 처리가 저장 기간 중 6.0% 이상의 농도를 보여 저농도 O2 조건으 로 혐기적인 발효과정으로 인한 이취 발생에 영향을 미치지 않을 것으로 판단된다. 포장 내 에틸렌 농도는 CO2 주입 처리에서 저장 1일차에 13.5μL∙L-1까지 증가하였다가 이후 8.5μL∙L-1내외로 감소하였으나 처리 중 가장 높게 유지되었다. 열수 처리구 에서 에틸렌 농도는 저장 1일차에 급격히 증가하였으나, 이내 감소하여 4.0-6.5μL∙L-1의 농도를 보여 저장 종료일까지 가장 낮 게 유지하였다(Fig. 2C). 일반적으로 열수 처리는 에틸렌 receptor와 에틸렌 생합성과 관련된 효소에 영향을 주어 에틸렌 발생 을 억제한다고 하였는데(Tian et al., 1997), 본 실험에서도 열수 처리에서 저장 중 가장 낮은 에틸렌 농도를 보였다. 그러나 CO2 전처리 및 주입 처리는 저장 중 다소 높은 에틸렌 농도를 보였는데, 이는 본 실험에서 사용했던 공업용 액화 CO2가 원인이라 판 단된다. 일반적으로 공업용 액화 CO2는 에틸렌을 이용한 ethylene oxide/ethylene glycol(EO/EG) 공정 방식으로 제조되는데,이후 실험에서 액화 CO2의 농도별 에틸렌 측정 실험을 진행하였을 때, CO2 농도 60%일때 29.5μL∙L-1의 에틸렌이 검출되었다.
Fig. 1.
Respiration (A) and ethylene production rate (B) of asparagus spears treated with three different pretreatments (control, UV-C, and hot water dip) at 20°C for 1 hour. Vertical bars represent ± SE (n = 4).
아스파라거스의 저장 중 생체중 감소율은 저장 중 꾸준하게 증가하여 관행 저장한 모든 전처리구에서 저장 최종일에 5.0- 6.0%의 수준을 보였고(Fig. 3A). MA 저장은 CO2 주입에서 0.8% 내외로 가장 높았으며, 무처리, 열수 그리고 UV-C처리에서 0.4% 수준으로 낮았다(Fig. 3B). 관행 저장과 비교할 때 MA 저장에서 생체중 감소율이 매우 낮았는데, 이는 Cho et al.(2009) 이 제시한 것처럼 저농도 O2 및 고농도 CO2의 대기 조건이 효과적으로 호흡을 억제하였고, 포장 내 높은 상대습도가 증산을 억 제하였기 때문이라 판단된다. 일반적으로 저장 중 아스파라거스의 최대 허용 생체중 감소율이 8.0%인 것(Kays and Paull, 2004)으로 미루어 보아, 본 실험에서 저장 방법에 따른 수분 손실에 의한 품질저하는 상품성을 유지하는 수준으로 나타났다
경화 특성의 변화
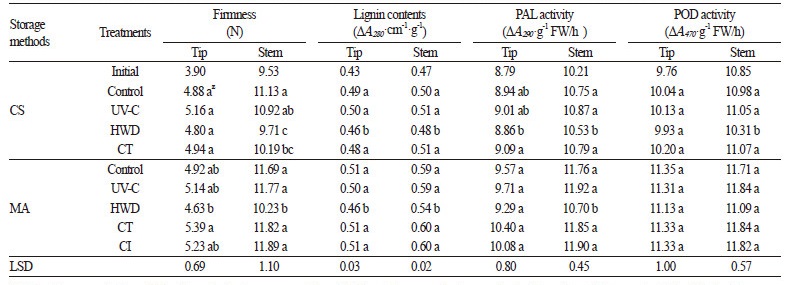
아스파라거스 품질 저하의 원인이 되는 경화를 분석하기 위해서 화두와 줄기의 경도, 리그닌 함량, 그리고 PAL과 POD의 활 성을 측정하였다(Table 1). 화두와 줄기의 경도는 모든 전처리구에서 초기값보다 증가하였고, 전처리 중 열수처리에서 가장 낮 았는데 MA 저장에서만 통계적 유의성이 인정되었다. 리그닌 함량도 화두와 줄기 모두 초기값보다 증가하였는데, 저장방법에
Fig. 2.
Changes in CO2 (A), O2 (B) and C2H4 (C) contents of asparagus spears in modified atmosphere (MA) storage for 35 days at 4°C. Vertical bars represent ± SE (n = 5).
Fig. 3.
Changes in fresh weight loss rate of asparagus spears in (A) conventional storage for 30 days or (B) modified atmosphere (MA) storage for 35 days, at 4°C. Vertical bars represent ± SE (n = 5).
관계없이 화두와 줄기 모두 열수 처리에서 가장 낮았고 특히 MA 저장처리구에서 무처리와 유의적인 차이를 보였다. PAL 활 성도 전처리 이후 화두와 줄기 모두 초기값보다 증가하였고, 저장 방법에 상관없이 열수 처리에서 가장 낮았으나, 줄기에서는 관행 및 MA 저장에서 무처리와의 차이가 통계적 유의성이 인정되었다. POD 활성 역시 화두와 줄기 모두에서 초기값보다 증 가하였고, 두 가지 저장 방법 모두에서 열수 처리가 낮았는데, 관행 저장의 줄기에서만 무처리와의 유의적인 차이를 보였다. 일 반적으로 원예산물은 수확 후 에틸렌 의해 조직의 연화가 촉진되지만(Kays and Paull, 2004), 아스파라거스는 저장 중에 에틸 렌에 의해 phenylalanine ammonia-lyase(PAL)와 peroxidase(POD) 활성을 증가시켜 리그닌화에 의해 경화가 촉진된다고 하 였다(Liu and Jiang, 2006). 본 실험에서도 리그닌 함량, PAL 및 POD 활성이 관행 저장보다 MA 저장에서 높은 경향을 보였는 데, 이는 저장 중 MA 포장 내 5.0-10.0μL∙L-1 농도를 보인 에틸렌이 원인인 것으로 생각된다. 전처리에 따른 경화 특성 변화 결 과를 비교해 볼 때, 열수 처리가 관행과 MA 저장 모두 경화 억제에 가장 큰 효과를 보였는데, 이는 리그닌 생합성에 관련된 효 소 활성 억제에 따른 결과라고 판단된다. 기존의 보고에 따르면 열처리는 엔디브에서 PAL의 합성을 억제하였고(Salman et al., 2008), 아스파라거스의 경도, 리그닌 함량의 증가 그리고 PAL 및 POD 활성을 억제했다고 하였다(Chiu and Sung, 2013). 특히 본 실험에서 열수 처리는 저장 중 포장 내 에틸렌 농도에 노출된 MA 저장 조건에서도 효과를 보였는데, 저장 중 다른 처리보다 낮은 에틸렌 농도를 꾸준히 유지하였고, 전처리에 따른 에틸렌 및 리그닌 생합성의 효소 활성을 효과적으로 억제했기 때문이 라 판단된다.
이러한 결과를 바탕으로 열수 처리는 기존의 MA 저장에서 에틸렌 농도 집적에 따른 리그닌화 진행의 문제점을 보완할 수 있었다.
품질 변화
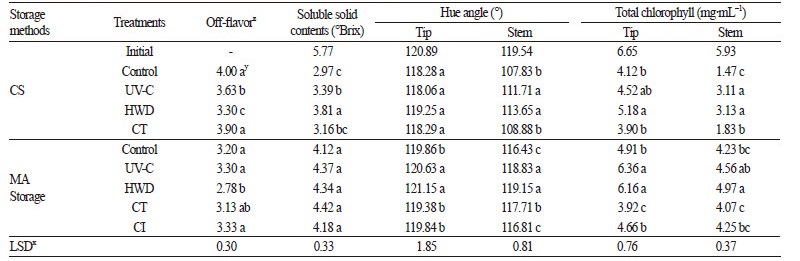
저장 최종일에 가용성 고형물 함량과 관능 조사를 통한 이취 및 외관을 비교하였고, 저장 중 황화 정도를 조사하기 위해 화두 와 줄기 부분을 나누어 hue angle값과 엽록소 함량을 측정하였다(Table 2 and Fig. 4).
관능평가로 조사된 이취는 저장 방법에 상관없이 열수 처리에서 가장 적었고, MA 저장한 모든 전처리구에서 관행 저장한 처리구보다 적게 발생하였다. 일반적으로 MA 저장의 경우 저장 동안의 이취 발생이 문제가 되는데(Kader, 2002), 2.5% 이하 의 산소 농도는 혐기성 호흡의 전환으로 인하여 acetaldehyde와 ethanol 생성으로 이취 등 여러 가지 피해가 나타난다고 하였 다(Park et al., 2015). 그러나 본 실험에서는 필름 포장 내 O2 농도가 최소 6.0% 이상을 유지하여 무기호흡(Kays and Paull, 2004)이 발생하지 않았던 것으로 보인다. 가용성 고형물 함량은 관행 저장에서 열수 처리가 가장 높았으나, MA 저장 시 모든 처리구간 통계적인 차이가 없었다(Table 2). 저장방법별로는 MA 저장한 아스파라거스의 가용성 고형물 함량은 관행 저장한 아스파라거스에 비해 높았는데, MA 저장에서 적정 MA 조건의 CO2 농도(5.0-12%)를 유지하면서 호흡이 억제되어 당 소모 가 적었기 때문이다. Hue angle 값은 관행 저장에서 화두 부분은 처리간 차이가 없었으나, 줄기 부분은 UV-C와 열수 처리에 서 높았고, MA 저장에서는 화두와 줄기 부분 모두 UV-C와 열수 처리에서 높게 유지되었다. 엽록소 함량은 저장 방법에 상관 없이 화두와 줄기 부분에서 UV-C와 열수 처리가 높게 유지되었다. 아스파라거스의 황화는 에틸렌에 의해 엽록소 감소가 촉 진되어 진행된다고 하였으나(Wang et al., 1971), 에틸렌 농도가 높았던 MA 저장 처리에서 관행 저장보다 높은 hue angle 값과 엽록소 함량을 보였는데, 이는 본 실험의 MA 저장에서 CO2 농도가 아스파라거스 저장의 적정 MA 조건을 만족했기 때문이라 판단된다. 일반적인 원예 산물은 10%의 고농도 CO2 조건에서 1.0μL∙L-1 에틸렌의 생화학적 활성을 억제하는 효과가 있는데,이는 CO2가 세포간극으로 축적되어 에틸렌의 생성 및 활성을 억제하는 기능을 보이기 때문이다(Yang 1985). 또한, Cho et al. (2009)도 브로콜리를 MA 저장 하였을 때 고농도 CO2 농도가 브로콜리 화뢰의 엽록소 분해 효소의 활성을 억제해 황화가 지연 되었다고 하였다. 전처리 기술에서 UV-C와 열수 처리 시 황화가 억제되는데, 브로콜리는 UV-C(Costa et al., 2006)와 열수 처 리(Funamoto et al., 2002)로 엽록소 분해 효소의 활성을 억제해 엽록소 감소율을 줄여 황화가 억제되는 효과를 보고하였다.
그러나 복숭아에서 에틸렌의 생합성을 억제한다고 알려진(Choi et al., 2007) 고농도 CO2 처리는 본 실험의 저장 전처리와 포 장 내 주입 처리 모두에서 hue angle값과 엽록소 감소 억제 효과를 나타내지 못했는데, 이는 본 실험에서 CO2 전처리에 이용되 었던 액화 CO2에 에틸렌 가스가 불순물로 포함되어 있었기 때문이라 판단되며, 실험에서 60% CO2 처리 기체에서 에틸렌이 29.5μL∙L-1의 농도로 검출되었다.
외관상 품질은 관행 저장구의 아스파라거스는 열수 처리 시 저장 종료일(30일)까지 가장 좋은 품질을 유지하였고(Fig. 4A), MA 저장구의 아스파라거스는 UV-C와 열수 처리에서 저장종료일(35일)까지 판매 가능 점수인 3점 이상을 유지하였다(Fig. 4B). 저장방법별로는 MA 저장한 아스파라거스가 관행 저장한 아스파라거스보다 높은 외관상 품질을 보였는데, 이는 MA 저 장구에서 나타난 1.0% 미만의 낮은 생체중 감소와 10% 수준을 보인 포장 내 CO2 농도에 의한 황화 억제가 원인이라 판단된다
이상의 결과를 종합하면 아스파라거스를 4°C에서 저장할 때 MA 저장 방법은 경화억제를 제외한 모든 품질 요소에 우수한 결과를 보였고, 전처리 중 열수 처리는 저장 방법에 상관없이 리그닌 생합성에 관련된 효소 활성과 황화 억제 등 품질 유지에 가 장 효과적이었다.
Fig. 4.
Changes in visual quality of asparagus spears in (A) conventional storage for 30 days or (B) modified atmosphere storage for 35 days (B), at 4°C. Vertical bars represent ± SE (n = 5)