서 언
재료 및 방법
실험 재료
가용성 고형물 함량, 건물 함량, 경도
Vitamin C
Lutein and β-carotene
시료의 추출
총 페놀 및 플라보노이드 함량
항산화 활성
아세틸콜린에스터라아제(AChE) 및 부티릴콜린에스터라아제(BChE) 저해 활성
통계 및 분석
결과 및 고찰
과실 특성
비타민 C, 루테인, 베타카로틴
총 페놀 및 플라보노이드 함량
항산화 활성
콜린에스터라아제 저해 활성
서언
키위(Actinidia spp.)는 호흡급등형 과일로 모체에 과실이 달리고 비대기를 거쳐 성숙 중에 1차 대사산물과 생리활성 물질의 합성이 이루어지며, 수확 전 뿐만 아니라 수확 후에도 대사작용으로 인해 물질의 생성과 분해, 조직 연화 등의 생화학적 및 물리적 변화를 겪는다(Ritenour et al., 1999; Tavarini et al., 2008). 키위, 파파야, 그리고 사과와 같은 호흡급등형 과일은 수확 후에도 활성물질의 변화가 계속된다(Matsumoto et al., 1983; Rivera-pastrana et al., 2010; Zhang et al., 2010).
키위는 수확 전 성숙 동안 과실 비대와 당도 증가, 엽록소 감소, 그리고 경도 감소가 이루어지며(Burdon et al., 2004; Jabbar et al., 2014; Montefiori et al., 2009), 수확 후에도 당도 증가와 산도 및 경도 감소, 생리활성 물질 변화가 진행된다(Matsumoto et al., 1983; Latocha et al., 2014). 골드키위(Actinidia chinensis)는 초록색 과육을 지닌 그린키위와 달리, 성숙 중에 색소 성분인 엽록소와 카로티노이드의 함량 변화로 인한 색 변화가 크게 나타난다(Minchin et al., 2003; Montefiori et al., 2009). 키위 과실의 수확 시 성숙도 또는 수확 후 저장에 따른 색소 성분의 변화와 항산화 활성이 많이 연구되어 있고(Ampomah-Dwamena et al., 2009; Pal et al., 2015; Tavarini et al., 2008), 키위 품종 간의 생리활성 물질과 항산화, 항염, 항치매 등의 기능성 활성이 연구된 바 있으나(Farr et al., 2007; Lim et al., 2014; Nishiyama et al., 2004), 수확 전 후 성숙 상태에 따른 물질 변화와 항산화 외 기능성 활성에 대한 연구는 미미하다.
기호성이 뛰어난 과일인 키위는 기후변화로 인해 국내 재배 면적이 증가하고 있으나, 국내에서 키위는 대부분 생과 형태로 소비되고 있으며, 이용 범위가 작아 농가 소득과 소비 증가에 제한이 되고 있다. 키위 재배 시, 과실 성숙 중에 다양한 환경 스트레스에 의해 완전히 성숙되기 전에 낙과되는 과실이 생기게 되며, 재배관리 시 많은 과실이 조기 적과되어 버려지고 있다. 후숙 과일의 경우 품질 평가나 수확 후 관리, 산업적 활용 등에 있어서 수확 시 성숙상태와 수확 후 저장기간 모두에 의해 영향을 받기 때문에 키위의 이용가치 증진을 위해 수확 전 후 성숙상태에 따른 생리활성 물질 및 기능성 활성 연구가 필요하다. 따라서 본 연구는 수확시기 별 수확 후 저장 동안 과실 특성과 생리활성 물질의 변화와 항산화 및 항치매 활성 변화를 분석하고자 실험을 수행하였다.
재료 및 방법
실험 재료
본 실험에 사용된 골드키위(A. chinensis)는 ‘Jecy Gold’(‘제시골드’) 품종으로 국립원예특작과학원 온난화대응농업연구소(Jeju, Korea)에서 비가림 재배하여 2015년 7~10월에 수확하였다. 수확시기 별 과실의 수확 후 저장에 따른 과실 특성과 물질 및 활성 변화 조사를 위해 수확 전 성숙 상태에 따라 만개 후 70~160일 동안 30일 간격으로 수확하였고, 수확한 키위 과실은 저장고(4°C, 상대습도 60%)에서 9주간 저장하여 3주 간격으로 조사를 실시하였다.
가용성 고형물 함량, 건물 함량, 경도
가용성 고형물 함량(°Brix)은 과육의 착즙액을 굴절당도계(Atago Co., Tokyo, Japan)로 측정하였고, 건물 함량은 껍질을 제거한 과육을 약 2mm 두께로 절편하여 65°C 에서 24시간 열풍건조 후, 건조 전 무게에 대한 백분율로 표시하였다. 경도(kg)는 과실의 껍질을 1mm 두께로 벗긴 후 과육 부분의 경도를 직경 5mm의 과실경도계(Takemura Denki Seisakusho Ltd., Tokyo, Japan)를 이용하여 측정하였다.
Vitamin C
Vitamin C 분석은 역상 HPLC(Waters 2695 Alliance HPLC, Waters, Milford, MA, USA)를 이용하여 Nishiyama et al. (2004)와 Nováková et al.(2008)의 방법을 변형하여 분석하였다. 시료 추출은 분쇄한 키위 과육 2g에 ice-cold 8% acetic acid 40mL를 첨가하여 90초간 vortexing 해준 후, 4°C, 10,000rpm에서 10분간 원심분리 후, 상징액을 0.45µm membrane filter (Syringe filter, Toyo Roshi Kaisha Ltd., Tokyo, Japan)로 여과 후 분석에 이용하였다. Column은 octadecylsilane column (Hypersil GOLD C18 column(5µm, 150 × 4.6mm), Thermo scientific, MA, USA)을 사용하였고, 이동상은 2%(v/v) formic acid가 포함된 water(A)와 2%(v/v) formic acid가 포함된 acetonitrile(B)을 사용하였다. 용매구배는 용매 B를 0%로 시작하여 1분까지 0%에서 5%로 증가시키고, 5분까지 9.4%로 증가시켰으며, 유속은 1.0mL·min-1로 분석하였다. Peak는 Waters 996 photodiode array detector(Waters Inc.)를 이용하여 254nm에서 측정하였다.
Lutein and β-carotene
Lutein과 β-carotene 분석은 Nishiyama et al.(2005)의 방법을 응용하여 분석하였다. Lutein과 β-carotene 추출은 키위 껍질 제거 후, 과육 100g 당 2g의 Na2CO3를 첨가하여 분쇄하였다. 분쇄한 키위 과육 5g에 80%(v/v) acetone 30mL을 첨가하여 1분 30초 동안 흔들어 준 후, 멸균거즈로 여과하였으며 3회 반복 추출하였다. 추출물은 4°C, 12,000rpm에서 2분간 원심분리 후, 상등액을 0.45µm membrane filter(Syringe filter, Toyo Roshi Kaisha Ltd., Tokyo, Japan)로 여과 후 분석에 이용하였다. Lutein 및 β-carotene 분석에 이용된 역상 HPLC는 Waters 2695 Alliance HPLC(Waters)를 사용하였다. Column은 octadecylsilane column[Prontosil 120-5-C18-ace-EPS(5µm, 250 × 4.6 mm), Bischoff, Leonberg, Germany]을 사용하였고, 이동상은 0.1%(v/v) formic acid가 포함된 water/acetonitrile(10:90, v/v)(A) 와 0.1%(v/v) formic acid가 포함된 ethyl acetate(B)를 사용하였다. 용매구배는 용매 B를 0%로 시작하여 10분까지 0%에서 60%로 증가시켜 15분간 유지하였다. Injection volume은 20µL로 하였고, 유속은 1.0mL·min-1로 분석하였다. 검출은 Waters 996 photodiode array detector(Waters Inc.)를 이용하여 445nm에서 측정하였다.
시료의 추출
시료는 분쇄한 키위 과육 50g에 80%(v/v) 에탄올을 250mL 첨가하여 상온에서 24시간씩 추출 후, Whatman No.1 여과지를 이용하여 여과하였다. 추출과정은 3회 반복 실시하여 추출물 혼합 후, 여과 및 감압 농축하여 사용하였다.
총 페놀 및 플라보노이드 함량
총 페놀 함량은 Singleton and Rossi(1965)의 방법을 변형하여 측정하였다. 증류수 2.6mL에 키위 추출물과 Folin-Ciocalteu’s phenol reagent(Sigma-Aldrich Co., St. Louis, MO, USA)를 0.2mL씩 혼합하였다. 혼합물은 6분간 반응시켜 7% Na2CO3를 2.0mL 가하여 상온에서 90분간 반응시킨 후 spectrophotometer(Scinco S-4100, Korea)를 이용하여 750nm에서 흡광도를 측정하였다. 총 페놀 함량은 gallic acid 표준검량곡선을 이용하여 정량하였다. 총 플라보노이드 함량은 Zhishen et al.(1999)의 방법을 응용하여 측정하였다. 함량 측정은 증류수 3.2mL와 키위 추출물 0.5mL을 혼합하고, 5% NaNO2 0.15mL, 10% AlCl3 0.15mL 및 1M NaOH 1.0mL를 가한 후 spectrophotometer(Scinco S-4100)를 이용하여 510nm에서 하였다. 총 플라보노이드 함량은 catechin 표준검량곡선을 이용하여 정량하였다.
항산화 활성
키위 추출물의 항산화 활성은 2,2-diphenyl-1-picrylhydrazyl(DPPH)와 2,2'-azino-bis(3-ethylbenzthiazoline-6-sulphonic acid)(ABTS) 자유라디컬 소거활성을 통해 측정하였다. DPPH 라디컬 소거활성은 Blois(1958)의 방법을 응용하여 측정하였다. 추출물 0.05mL에 0.06mM DPPH solution 2.95mL을 가한 후 암조건에서 30분간 반응시킨 후 spectrophotometer(Scinco S-4100)를 이용하여 517nm에서 흡광도를 측정하였다. ABTS 라디컬 소거활성은 Floegel et al.(2011)의 방법을 변형하여 측정하였다. ABTS 라디칼 용액은 2.5mM ABTS 용액에 1.0mM 2,2'-Azobis(2-amidinopropane) dihydrochloride를 혼합한 후 70°C에서 30분간 반응시켜 제조하였다. 제조된 ABTS 라디칼 용액은 상온에서 식힌 후 0.45µm membrane syringe filter로 여과하여 사용하였다. ABTS 라디칼 용액 0.98mL에 추출물 0.02mL를 가하여 10분간 반응시킨 후, 흡광도는 spectrophotometer (Scinco S-4100)를 이용하여 734nm에서 측정하였다. DPPH와 ABTS 자유라디컬 소거활성은 ascorbic acid 표준검량곡선을 이용하여 정량하였다.
아세틸콜린에스터라아제(AChE) 및 부티릴콜린에스터라아제(BChE) 저해 활성
키위 추출물의 항치매 활성은 Ellman et al.(1961)의 방법을 변형한 AChE 및 BChE 저해 활성 실험을 통해 측정하였다. AChE와 BChE 저해 활성 실험에서 acetylthiocholine iodide(ATCI)와 butyrylthiocholine chloride(BTCC)가 각각 기질로 사용되었고, 발색시약으로는 5,5'-dithiobis(2-nitrobenzoic acid)(DTNB)가 사용되었다(Sigma-Aldrich, St. Louis, MO, USA). 효소 반응은 다음과 같이 진행하였다. Incubation은 110µL의 100mM phosphate buffer에 추출물과 효소(0.2U/mL)를 20µL씩 가한 후, 37°C에서 5분간 하였다. 활성도는 10mM DTNB 30µL와 기질(15mM ATCI, 10mM BTCC)을 20µL 가하여 37°C에서 20분간 반응 후 415nm에서 microplate reader(model 680; Bio-Rad Laboratories Inc., Hercules, CA, USA)를 이용하여 흡광도를 측정하였다. 양성대조군은 tacrine을 농도별로 사용하였으며, 효소 저해 활성은 다음과 같이 계산하였다.
Cholinesterase inhibitory activity (%) = 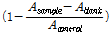 × 100
× 100
Asample : 시료, 효소, 기질 첨가군의 흡광도
Ablank : 시료 첨가, 효소 및 기질 무첨가군의 흡광도
Acontrol : 시료, 효소, 기질 무첨가군의 흡광도
통계 및 분석
통계 분석은 SAS 통계 프로그램(Enterprise guide 7.1 version, SAS Institute Inc., Cary, NC, USA)을 이용하여 Tukey’s studentized range(HSD) test 에 의해 유의적 차이(p < 0.05)를 검정하였다.
결과 및 고찰
과실 특성
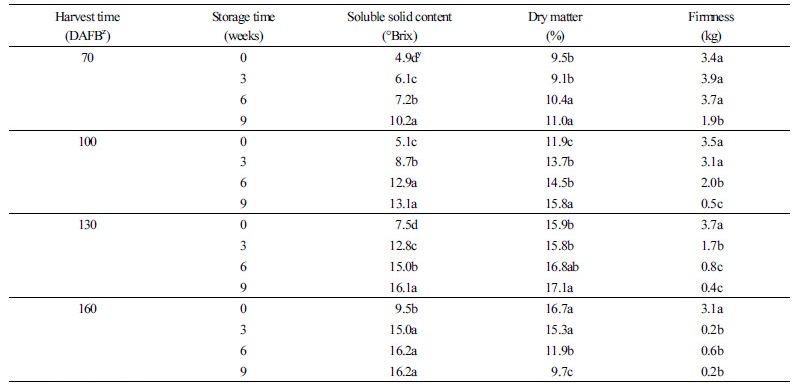
키위 과실의 가용성 고형물 함량은 수확시기 및 수확 후 저장기간에 따라 증가하는 것으로 나타났다(Table 1). 만개 후 70일에 4.9°Brix에서 160일에 9.5°Brix까지 계속 증가하였으며, 모든 수확시기에서 저온 저장 9주 동안 가용성 고형물 함량이 증가하였다. 만개 후 160일에서는 저장 3주차에 급격히 증가 후 함량을 15°Brix 이상 유지하였다. 당과 전분을 포함한 건물 함량은 후숙 과일에서 가용성 고형물과 상관관계가 큰 품질평가요소로서 수확기 결정과 수확 후 관리에 중요 요소로 여겨진다(Jordan et al., 2000; Richardson et al., 1997). 수확시기가 늦을수록 과실 비대 및 저장산물 축적으로 건물 함량도 증가하였으며, 만개 후 160일을 제외하고는 저장 동안에도 건물 함량이 증가하였다. 만개 후 160일에 수확한 과실은 수확 후 저장 9주 동안 16.7%에서 9.7%로 점진적으로 감소하였다. 이는 후숙 과정에서 과실의 호흡 대사작용으로 인해 저장산물이 소모되고, 과실 내 전분이 당으로 가수분해되어 건물 함량 감소와 함께 가용성 고형물 함량이 증가한 것으로 판단된다. 수확시기에 따른 경도의 변화는 유의적 차이가 없었으나, 모든 수확시기에서 저장기간이 길어질수록 감소하였으며, 수확시기가 늦을수록 경도 감소가 촉진되었고 감소율이 높게 나타났다. 이러한 물성변화는 수분 함량의 변화, 전분과 당, 단백질 등의 저장 산물의 변화 때문인 것으로 보인다. 수확 시 과실의 당도, 건물 함량 및 경도는 개화 전 낙엽시기에 따라 달라지며(Srisook et al., 2016), 수확 시 과실 성숙도가 수확 후 저장 중 당도 및 경도 변화에 큰 영향을 미치므로 과실 이용 용도에 따라 적엽시기와 과실 성숙도를 고려하여 수확 적기를 판단하는 것이 중요할 것으로 보인다.
비타민 C, 루테인, 베타카로틴
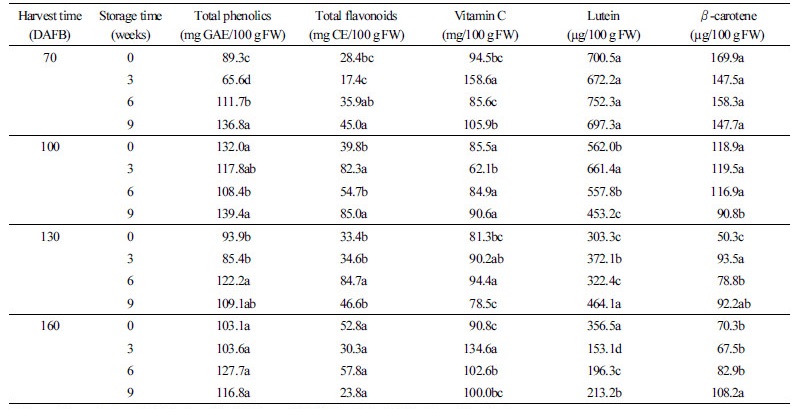
수확시기 및 후숙 기간에 따른 키위 과육 내 비타민 C 함량과 카로티노이드 함량은 Table 2에 나타내었다. 비타민 C 함량은 수확시기에 따른 유의적 차이를 보이지 않았으며, 저장 중에도 뚜렷한 경향을 보이지 않았다. Ferguson and MacRae(1991)의 Actinidia속 과실 내 비타민 C 함량은 수확 전후 성숙 동안 유의적인 변화가 없었다는 보고와 유사하였다. 키위 과실 내 주요 카로티노이드로 알려진 루테인과 베타카로틴(Cano, 1991)의 함량 변화를 수확시기 및 수확 후 저장기간에 따라 조사한 결과, 루테인과 베타카로틴 모두 수확시기가 늦을수록 함량이 감소하였으며, 만개 후 130일 이후에는 함량이 유지되었다. 만개 후 70일에 루테인과 베타카로틴은 각각 700.5, 169.9µg/100g fresh weight으로 함량 최고치를 보였으며, 수확시기에 상관없이 수확 후 저장 중에는 함량 변화에 크게 영향을 받지 않았다. Ampomah-Dwamena et al.(2009)에 의하면, A.chinensis의 세 품종에서 만개 후 20-150일 동안 루테인은 증가 후 감소하였으며, 베타카로틴은 만개 후 150일까지 꾸준히 증가하거나 만개 후 50일에 증가 후 함량을 유지하였다. 또한, 4°C에서 저장하였을 경우 20°C 저장에 비해 저장기간 동안 카로티노이드 함량이 크게 감소하였다고 보고하였다. Montefiori et al.(2009)은 만개 후 140-190일 동안 총 카로티노이드 함량은 유지되었으나 루테인과 베타카로틴 함량은 감소하였다고 보고하였다. 노란색을 갖는 루테인과 주황색을 갖는 베타카로틴 모두 성숙하지 않은 과실에 축적이 최대로 이루어졌으나 수확시기가 늦어질수록 녹색 과육에서 황색으로 색 변화가 일어났는데 이는 카로티노이드 함량 변화보다는 엽록소의 감소로 인한 것으로 알려져 있다(McGhie and Ainge, 2002). 또한 조기 수확 과실의 경우 수확 후 색 변화가 일어나지 않았으나, 만개 후 100일 이후 수확한 과실의 과육은 후숙 동안 녹색에서 황색으로 변했다(Fig. 1). 따라서, 키위 과실 내 카로티노이드 함량은 수확시기에 따라 변하며, 저장기간보다는 저장 온도가 더 큰 영향을 미치는 중요 요소로 판단된다.
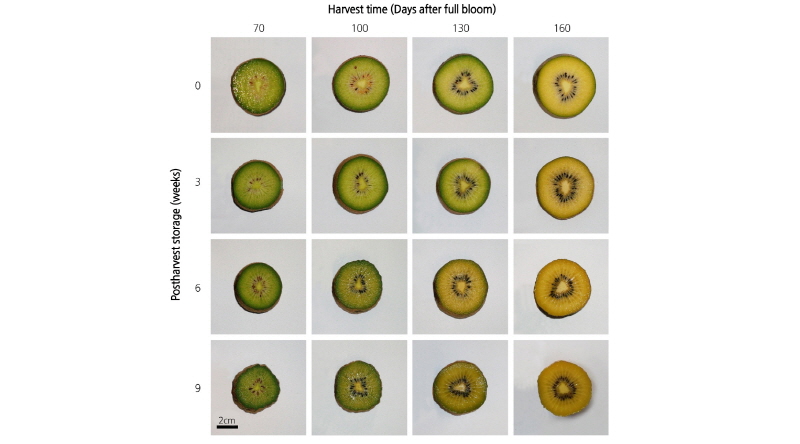
Fig. 1. Color changes in the flesh of ‘Jecy Gold’ kiwifruits at different harvest and postharvest storage times. ‘Jecy Gold’ fruits shown were cultivated by rain shield culture at the Research Institute of Climate Change and Agriculture in Jeju, Korea, and were harvested between July and October, 2015. Harvested fruits were stored at 4°C and 60% relative humidity for the duration of the experiment.
총 페놀 및 플라보노이드 함량
총 페놀 및 플라보노이드 함량은 수확시기의 과실 성숙기에 따라 일정한 변화 경향을 보이지 않았으나 만개 후 100일에 수확한 과실에서 총 페놀함량이 가장 높게 나타났다(Table 2). 조기 수확한 과실(만개 후 70일)은 저장 동안 과실 내 총 페놀 및 총 플라보노이드 함량이 증가하는 경향을 보였고, 만개 후 100일 이후 수확한 과실은 저장 중 총 페놀 및 플라보노이드 함량 변화가 일정한 경향을 나타내지 않았다. 총 플라보노이드 함량은 만개 후 100일과 130일에 수확한 과실의 수확 시 함량보다 저장하였을 때 높은 함량을 나타내었고, 만개 후 70일에 수확한 과육과 그 3주차 저장 그리고 만개 후 160일의 9 주차에서 17-28mg으로 낮은 함량을 보였다. 수확시기 별 총 페놀 및 플라보노이드 함량은 항산화 함량과 유사한 경향을 보여 수확 시 페놀성 물질과 플라보노이드 물질군이 항산화에 기여하는 것으로 판단된다. 반면 수확 후 저장 동안 총 페놀 및 플라보노이드 함량과 항산화 활성 간의 상관관계가 높지 않아 다른 2차대사산물의 영향이 있을 것으로 보인다.
항산화 활성
수확시기 및 수확 후 저장기간에 따른 키위 과실의 항산화 활성 측정 결과(Fig. 2), 키위 과실의 항산화 활성은 수확시기에는 크게 영향을 받지 않았다. DPPH 라디컬 소거활성의 경우, 만개 후 100일을 제외하고는 저장 3주차에 감소했다가 이 후 9주차까지 활성이 증가하였다. 만개 후 100일에 수확한 과실의 DPPH 라디컬 소거활성은 저장 3주 이후에 증가하다가 6주에 활성이 79.0mg VCE/100g fresh weight으로 정점을 보인 후 급격히 감소하였다. ABTS 라디컬 소거활성의 경우, 만개 후 70일에서는 DPPH 라디컬 소거활성과 유사하게 3주 이후 증가하였으나, 100일 이후 수확한 과실은 저장 동안 활성 변화가 없거나 감소하였다. DPPH와 ABTS 라디컬 소거활성은 만개 후 100일에 수확한 과실이 다른 시기에 수확한 과실보다 높았으며, 저장 6주까지 높게 유지되었다. 단 저장 9주차에는 만개 후 100일에 수확한 과실의 DPPH 라디컬 소거활성이 다른 수확시기의 과실보다 낮았으며, ABTS 라디컬 소거활성은 만개 후 70일에 수확한 과실이 급격히 증가하는 것으로 조사되었다. 키위 과실의 항산화 활성은 수확 시 가용성 고형물 함량에 따라 달라질 수 있으며(Ghasemnezhad et al., 2013), 항산화 물질인 비타민 C와 페놀성 화합물의 함량 변화가 항산화 활성에 영향을 미친 것으로 보인다.
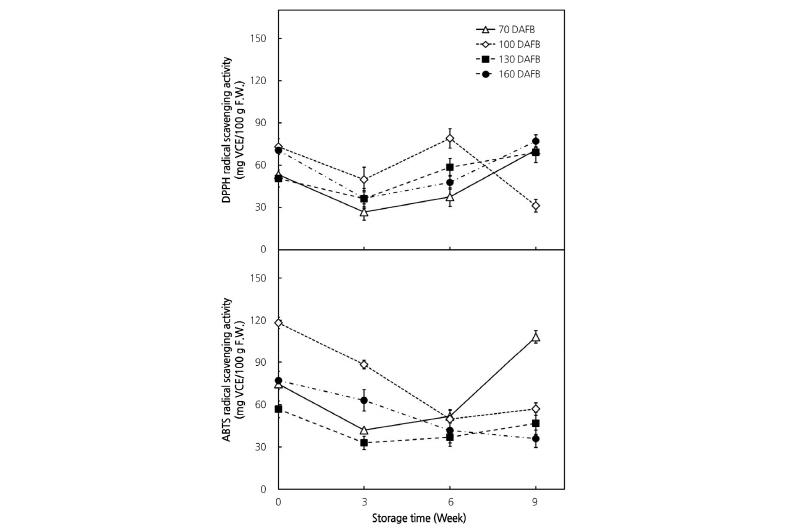
Fig. 2. Antioxidant activity of extracts from the flesh of ‘Jecy Gold’ kiwifruits at different harvest and postharvest storage times. Antioxidant activity was determined using 2,2-diphenyl-1-picrylhydrazyl (DPPH) and 2,2'-azino-bis (3-ethylbenzo-thiazoline-6-sulphonic acid (ABTS) free radical scavenging activity assays. ‘Jecy Gold’ fruits shown were cultivated by rain shield culture at the Research Institute of Climate Change and Agriculture in Jeju, Korea, and were harvested between July and October, 2015. Harvested fruits were stored at 4°C and 60% relative humidity for the duration of the experiment. DAFB, days after full bloom; FW, fresh weight; VCE, vitamin C equivalent.
콜린에스터라아제 저해 활성
알츠하이머성 치매는 신경전달물질인 아세틸콜린의 감소가 주원인이며, AChE와 BChE가 아세틸콜린 감소에 기여한다. 콜린에스터라아제의 활성을 저해시킴으로써 아세틸콜린의 기능을 유지시키는 것이 치매의 치료방안으로 연구되고 있으며, 따라서 수확시기 및 후숙기간을 달리한 키위 과실의 콜린에스터라아제 저해 활성을 측정하였다(Fig. 3). 수확시기에 따른 키위 과실의 콜린에스터라아제 저해 활성은 만개 후 130일 까지 70.44-79.34%로 유의적 차이가 없었으나, 만개 후 160일에 AChE와 BChE 저해 활성은 각각 56.24% 및 49.87%로 감소하였다. 모든 수확시기에서 수확 후 저장 중에 활성이 감소하였으며, 수확시기가 늦을수록 감소폭이 크게 나타났다. 만개 후 160일에 수확한 과실은 저장 3주부터 콜린에스터라아제 저해 활성이 나타나지 않았으며, 수확 전과 후 성숙과정에서 미성숙할 수록 콜린에스터라아제를 더욱 억제하는 것으로 나타났다. Eom and Reisch(2010)에 의하면 낮은 pH는 효소 활성에 부정적인 영향을 미치는데, 실제로 아세트산 pH 3.2 이하에서는 콜린에스터라아제의 활성이 현저하게 억제되었다(data not shown). 그러나 실험에 사용된 수확시기 및 수확 후 저장에 따른 키위 추출물의 pH는 3.3~3.4로 유의적 차이를 보이지 않았다. 수확 후 성숙과정에서 키위 과실의 pH는 뚜렷한 변동이 없으며(MacRae et al., 1989; Park et al., 2006), papaya, soursop, jackfruit 과 같은 후숙과일의 경우 성숙한 상태에서 pH가 더 낮게 조사된 것으로 보아(Corrêa et al., 2008; Márquez et al., 2011; Ong et al., 2006), 본 실험에서 키위의 pH는 콜린에스터라아제 활성과 상관관계가 없는 것으로 보인다. 콜린에스터라아제 억제에 기여하는 주요 물질군은 alkaloids, terpenoids, glycosides of terpenoids (Karimi et al., 2010; Mukherjee et al., 2007)로 알려져 있으며, 페놀성 유도체나 플라보노이드군이 cholinesterase 억제에 기여할 수 있다(Dall’Acqua et al., 2010; Lim et al., 2014).
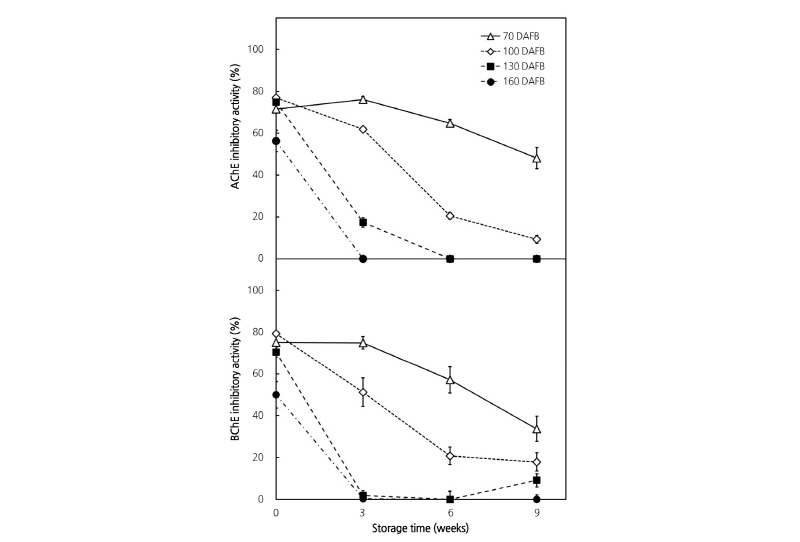
Fig. 3. Cholinesterase activity of extracts from the flesh of ‘Jecy Gold’ kiwifruits at different harvest and postharvest storage times. ‘Jecy Gold’ fruits shown were cultivated by rain shield culture at the Research Institute of Climate Change and Agriculture in Jeju, Korea, and were harvested between July and October, 2015. Harvested fruits were stored at 4°C and 60% relative humidity for the duration of the experiment. AChE, acetylcholinesterase; BChE, butylcholinesterase; DAFB, days after full bloom.