서 언
딸기(Fragaria × ananassa Duch.)는 1980년대부터 조직배양기술을 통해 무병묘를 보급하였으나 변이주의 발생으로 재배 시 많은 문제가 되고 있다. 그러나 최근 병배양(고체배양) 방법의 단점을 보완하기 위해 Lee et al.(2010)은 생물반응기 배양(액체배양)을 통해 증식율을 높고 변이주 발생이 적은 조직배양기술을 개발하였다. 그러나 생물반응기 배양은 생장점 배양묘가 액체배지에 잠겨있는 상태로 배양되기 때문에 고체배양에 비해 조직이 연하고 식물체의 초장이 길어지며, 잎과 줄기의 발달이 불안정하고, 식물 구조가 비정상적으로 발달한다(Sutter and Langhans, 1979; McClelland and Smith, 1990). 그래서 포장에서 자란 묘와 잎의 해부학적 구조, 기공의 기능 및 표피의 왁스의 양 등에서 차이를 보여(Wardle et al., 1983), 순화 시 외부의 건조한 공기를 접하면 수분손실이 많을 뿐만 아니라, 뿌리의 발달이 미약해 토양수분을 빠르게 흡수하지 못해 결국 고사율이 증가하는 단점을 가지고 있다(Lee et al., 2010).
|
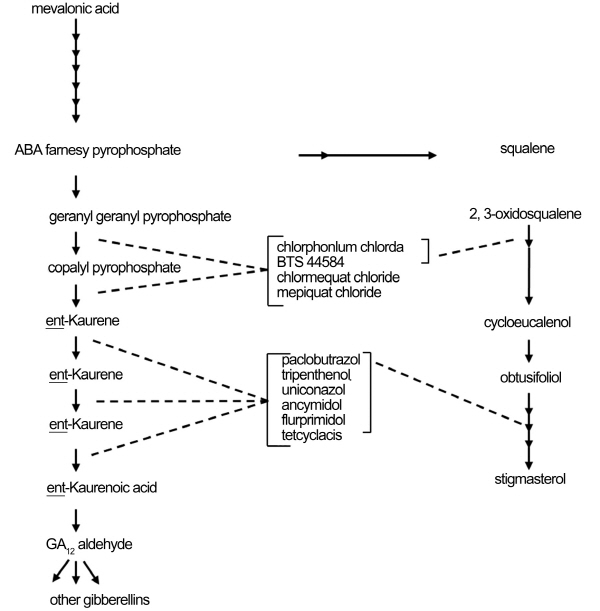
Fig. 1. Known points of inhibition on the isoprenoid pathway leading to gibberellins and sterols. |
식물생장억제제는 조직배양묘의 순화 시 발생되는 식물체의 고사 문제를 극복하기 위해 사용하는데, 기내(in vitro)에서 사용할 경우 시들음 증상을 감소시키고(Smith et al., 1991), 생체내(in vivo)에서 사용할 경우 키가 큰 식물의 절간을 짧게 하고, 잎의 크기 감소시키며, 잎을 진녹색으로 변화시켜 지상부를 튼튼하게 만들 뿐만 아니라 뿌리를 두껍게 하여 지하부도 단단하게 만든다(Graebe, 1987). 또한 수선화(Chen and Ziv, 2001a, b), 마늘(Kim et al., 2003), Colchicum autumnale(Ellington et al., 1997), 양파(Guen-Le Saos et al., 2002) 그리고 글라디올러스(Ziv, 1989, 1990) 등에서는 지하부의 발달을 촉진시키는 것으로 보고되고 있다. 이러한 생장억제제의 대표적인 계통은 트리아졸계통(paclobutrazol, triapenthenol, uniconazol)과 피리미딘계통(flurprimidol, ancy-midol)으로 나뉘며 대부분이 지베렐린 생합성을 억제하는데 관여한다(Fig. 1; Hazarika, 2003). 최근에 가장 많이 사용되는 트리아졸계통은 처리농도가 높아 유효성분이 주변환경에 더 많이 배출되어 토양 내 반감기가 182-365일로 다른 계통에 비해 63-246일이 더 길어 농업 생태계에 나쁜 영향을 미치기 때문에(Berruti and Scariot, 2013), 이를 대신할 새로운 계통의 식물생장억제제 탐색이 요구되고 있다.
따라서 본 연구는 생물반응기를 이용한 딸기조직배양 시 식물생장억제제로 피리미딘계통인 flurprimidol을 이용하여 기내배양 후 순화 생존율을 향상시키고자 실시하였다.
재료 및 방법
본 실험에 사용된 식물재료는 사계성 딸기 ‘고하’로, 생장점을 0.2-0.3mm 크기로 적출하여 Kim et al.(2011)의 방법에 따라 배양 및 유지하며 사용하였다.
기내 배양 중인 ‘고하’ 유식물체의 잎과 뿌리를 자르고 ‘Immersion’ 형식의 생물반응기에 처리별로 각 15주씩 넣었으며, 0.2vvm(air volume/medium volume/min)으로 공기를 주입하며 배양하였다. 액체배지는 1/2 MS 무기염에 30g・L-1의 sucrose를 넣어 완전히 녹이고 flurprimidol을 농도별로 첨가한 후 배지 pH를 5.6-6.6으로 조정하여 121°C, 1.5기압의 고압멸균기에서 15분간 멸균 후 사용하였다. Flurprimidol은 0(대조), 0.1, 0.5, 1.0 및 2.0mg・L-1의 농도로 처리하였으며, 각 처리당 15주씩 3반복으로 6주간 배양한 후 기내유식물체의 생육조사를 실시하였다. 초장은 기부로부터 식물체 전체 길이, 잎수는 주당 잎의 개수, 엽장 및 엽폭은 식물체의 잎 중 가장 큰 잎의 길이와 폭, 잎두께는 식물체의 잎 중 가장 큰 잎의 두께, 뿌리수는 주당 뿌리(주근)의 개수, 뿌리길이는 식물체의 뿌리 중 가장 긴 뿌리의 길이, 액아수는 주당 발생된 액아의 개수, 생체중은 잎과 뿌리를 모두 포함한 식물체의 무게로 나타내었다.
기내 생육조사 후 온실순화는 흑색비닐포트(480mm × 320mm, 24구)에 딸기전용상토(푸르미, ㈜서울바이오)를 충진한 후, 증식된 모든 유식물체를 한 개체씩 떼어 심었다. 관수는 상토 표면이 살짝 말랐을 때 지하수를 두상관수 하였다. 온실 내 기온은 10-25°C 범위로 유지하였으며, 순화 직후 투명비닐을 씌워 상대습도를 90%이상으로 유지하였고, 50% 차광망으로 약 일주일간 차광하였다. 그 후 자연광 하에서 생육을 유도하였고(Lee et al., 2012), 4주 후에 순화 식물체의 생육특성 및 생존율을 조사하였다. 순화 식물체의 생육조사는 기내유식물체의 생육조사와 동일한 기준으로 실시하였다.
결과 및 고찰
사계성 딸기 품종 ‘고하’의 생물반응기 배양 시 순화율 향상을 위해 flurprimidol을 농도 별로 처리한 결과는 Table 1 및 Fig. 2와 같다. Flurprimidol 처리 시 초장은 2.2-3.7cm 범위로 대조의 7.9cm에 비해 많이 왜화되는 것을 확인할 수 있었다. 잎수는 대조가 44.6개/주인 것에 비해 flurprimidol 0.1mg・L-1과 0.5mg・L-1 처리가 68.4개/주와 53.4개/주로 각각 더 많이 발생하였으나, 그 이상의 농도에서는 비슷하거나 적게 발생하였다. 잎의 크기는 대조에 비해 flurprimidol 0.5mg・L-1 이상 처리했을 경우 작아지는 경향을 보였으나, 잎의 두께는 flurprimidol 1.0mg・L-1 이상 처리했을 때 점점 두꺼워지는 경향을 보였다. 뿌리수는 대조가 51.8개/주인 것에 비해 flurprimidol 처리가 11.6-34.2개/주 범위로 17.6-40.2개/주가 더 감소하는 것을 확인할 수 있었고, 뿌리길이와 생체중도 같은 경향을 보였다. 액아수는 flurprimidol 2.0mg・L-1처리를 제외한 모든 처리에서 10.4-15.4개/주 범위로 대조의 8.6개/주에 비해 더 많이 발생하는 것을 확인할 수 있었다.

|
Fig. 2. Growth characteristics of plantlets according to concentration of flurprimidol in bioreactor culture of ever-bearing strawberry ‘Goha’ (A : 0 mg・L-1 of flurprimidol; B : 0.1 mg・L-1 of flurprimidol; C : 0.5 mg・L-1 of flurprimidol; D : 1.0 mg・L-1 of flurprimidol; E : 2.0 mg・L-1 of flurprimidol). |
|
Table 1. Comparison of in vitro growth of ever-bearing strawberry ‘Goha’ in the presence of different concentrations of flurprimidol in bioreactor culture. |
Concentration (mg・L-1) | Shoot length (cm) | No. of leaves (ea) | Leaflet length (cm) | Leaflet width (cm) | Leaflet thickness (mm) | No. of roots (ea) | Root length (cm) | No. of axillary shoots (ea) | Fresh weight (g) |
0 | 7.9 az | 44.6 b | 1.92 a | 1.44 a | 0.32 b | 51.8 a | 4.36 a | 8.6 c | 15.73 a |
0.1 | 3.7 b | 68.4 a | 1.22 a | 1.14 a | 0.35 b | 20.4 bc | 3.08 ab | 15.4 a | 3.01 b |
0.5 | 3.5 b | 53.4 ab | 1.02 a | 0.94 b | 0.37 b | 34.2 b | 2.40 b | 12.0 a | 2.77 b |
1.0 | 3.2 b | 44.8 b | 0.92 b | 0.86 b | 0.45 a | 13.8 c | 1.70 c | 10.4 b | 1.80 b |
2.0 | 2.2 b | 26.6 c | 0.90 b | 0.88 b | 0.59 a | 11.6 c | 0.88 c | 6.8 c | 1.77 b |
zDefferent letters within columns indicate significantly different values based on Duncan’s multiple range test (p ≤ 0.05). |
Ilczuk et al.(2005)는 Hippeastrum × chmielii Chm.의 기내 조직배양 시 고체 및 액체배양 모두 flurprimidol의 처리 시 유식물체의 초장이 줄어들었고, 특히 액체배양에서 왜화효과가 더 컸다고 보고하였다. 본 실험에서도 flurprimidol처리가 딸기 기내유식물체의 생육에 영향을 미쳐 초장이 대조에 비해 매우 감소한 것을 확인할 수 있었다. 일반적으로 생장억제제들은 구근성 작물에서 지베렐린 생합성을 저해하여 지상부 생육을 억제하는데 반해 구근 형성을 촉진하는 효과가 있었다고 보고하였는데(Kim et al., 2003; Guen-Le Saos et al., 2002), 본 실험에서 flurprimidol을 처리함으로써 정아의 발달을 막고 액아의 발달을 증가시킨 결과와 일치하였다.
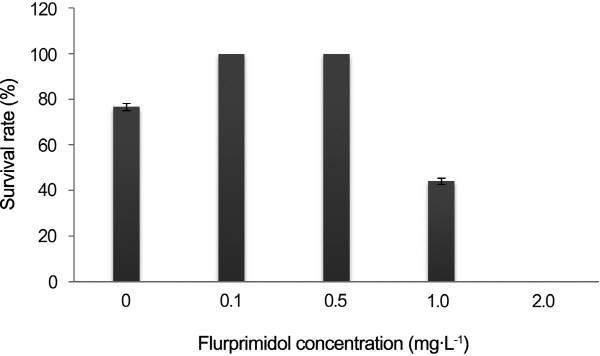
또한 대조의 순화 생존율은 76.7%로 전체의 23.3%가 고사하였다. 이는 순화 시 외부환경의 급격한 변화로 뿌리와 잎의 기능이 제대로 이뤄지지 않았기 때문이다. 그러나 flurprimidol 0.1mg・L-1와 0.5mg・L-1처리는 기내생육이 억제되고 잎의 두께가 두꺼워짐으로써 시들음이 감소되어 순화 생존율이 100%로 향상되었다. 반면에 flurprimidol 1.0mg・L-1처리는 44.2%, flurprimidol 2.0mg・L-1처리는 0%로 매우 낮았는데(Fig. 3), 이것은 flurprimidol 1.0mg・L-1이상의 농도에서는 기내 유식물체의 뿌리가 무르고 썩는 현상이 발생하였기 때문이다. Smith et al.(1991)은 국화 유식물체에 flurprimidol 3mg・L-1이상의 농도로 처리했을 때 시들음 감소 현상을 보였다고 하였으나 본 실험의 딸기에서는 flurprimidol 0.1-0.5mg・L-1범위의 저농도에서 시들음이 감소되어 순화 생존율이 향상되었고, 오히려 1.0mg・L-1 이상의 고농도에서 시들음은 감소되었으나 뿌리발달이 불량하였기 때문에 순화 생존율이 낮아진 것으로 판단된다.
|
Fig. 3. Survival rate of acclimated ever-bearing strawberry ‘Goha’ plantlets according to concentration of flurprimidol. |
온실에서 순화 과정을 거친 후의 생육특성(Table 2, Fig. 4)을 보면, 순화 후 대조의 초장은 13.2cm였으며 flurprimidol 0.1mg・L-1 처리는 10.4cm로 대조와 큰 차이를 보이지 않을 정도로 순화기간 동안 생육이 촉진되었다. 그러나 flurprimidol 0.5mg・L-1처리와 1.0mg・L-1처리는 각각 6.62cm와 5.32cm로 대조에 비해 생육이 저조하였다. 또한 잎수, 잎의 크기 및 뿌리길이도 초장과 같은 경향을 보였다. 뿌리수는 대조가 14.4개/주였으나 모든 flurprimidol 처리에서는 5.0-9.8개/주 범위로 유의적인 차이를 보였으며, 생체중도 같은 경향을 나타냈다. 그리고 순화 후 런너는 대조와 flurprimidol 0.1mg・L-1처리에서만 발생하였으며, 그 이상의 처리에서는 전혀 발생하지 않았다. 따라서 딸기 조직배양묘의 생물반응기 배양 시 flurprimidol 0.1mg・L-1 처리가 기내에서의 생육억제로 온실 내 순화 중 생육이 왕성하여 대조와 비슷하게 회복됨으로써 가장 적당한 처리농도로 판단되었다.

|
Fig. 4. Growth characteristics of ever-bearing strawberry ‘Goha’ plants acclimated for 4 weeks according to concentration of flurprimidol (A, E : 0 mg・L-1 flurprimidol; B, F : 0.1 mg・L-1 flurprimidol; C, G : 0.5 mg・L-1 flurprimidol; D, H : 1.0 mg・L-1 flurprimidol). |
Table 2. Growth characteristics of acclimated ever-bearing strawberry ‘Goha’ plants by concentration of flurprimidol. |
Concentration (mg・L-1) | Shoot length (cm) | No. of leaves (ea) | Leaf length (cm) | Leaf width (cm) | No. of roots (ea) | Root length (cm) | Fresh weight (g) | No. of runners (ea) |
0 | 13.2 az | 9.6 a | 4.90 a | 4.50 a | 14.4 a | 18.9 a | 17.0 a | 3.2 |
0.1 | 10.4 a | 7.2 a | 4.10 a | 3.62 ab | 9.8 b | 15.5 ab | 5.1 b | 3 |
0.5 | 6.62 b | 5.6 b | 2.78 b | 2.32 b | 5.2 c | 12.8 b | 1.8 c | 0 |
1.0 | 5.32 b | 6.2 b | 2.16 b | 1.64 b | 5.0 c | 12.1 b | 1.2 c | 0 |
2.0 | - | - | - | - | - | - | - | - |
zDefferent letters within columns indicate significantly different values based on Duncan’s multiple range test (p ≤ 0.05). |
그러나 딸기 조직배양묘 생산 시 호르몬을 처리하면 변이주가 발생될 수 있어(Sansavini et al., 1990) 정식 후 변이검정을 실시한 결과, flurprimidol 처리묘의 형태적 특징의 차이는 없었으며, 개화 특성에도 변이가 발생하지 않은 것을 확인할 수 있었다(Table 3). 그러나 유전적 변이검정기술이 없으므로 시급히 개발하여, 딸기 우량묘 생산보급체계를 확립할 필요가 있을 것으로 판단된다.
Table 3. Morphological characteristics of clonally propagated strawberry ‘Goha’ plants according to concentration of flurprimidol. |
Flurprimidol (mg・L-1) | Plant height (cm) | No. of leaves (per plant) | Leaf length (cm) | Leaf width (cm) | Appearance of floral bud | No. of crown (per plant) |
0 | 29.8 bz | 30.7 bc | 9.7 a | 7.6 a | continuously | 3.5 a |
0.1 | 27.6 b | 25.0 c | 9.6 a | 8.5 a | continuously | 2.3 a |
0.5 | 28.5 b | 37.8 b | 9.3 a | 7.4 a | continuously | 3.3 a |
1.0 | 37.1 a | 48.8 a | 10.3 a | 8.5 a | continuously | 4.0 a |
zDefferent letters within columns indicate significantly different values based on Duncan’s multiple range test (p ≤ 0.05). |
Acknowledgements
본 논문은 농촌진흥청 국립식량과학원 고령지농업연구센터의 ‘여름재배용 육성품종의 기본묘, 원원묘 생산 및 보급’ 연구과제비용으로 수행된 결과의 일부이며, 이에 감사를 드립니다.
References
Berruti, A. and V. Scariot. 2013. Efficacy of flurprimidol and peat alternatives on growth control of potted camellias. N. Z. J. Crop Hortic. Sci. 41:230-239.
Chen, J. and M. Ziv. 2001a. Ancymidol effect on oxidative stress and the regeneration potential of Narcissus leaves in liquid culture. Acta Hortic. 560:299-302.
Chen, J. and M. Ziv. 2001b. The effect of ancymidol on hyper-hydricity, regeneration, starch and antioxidant enzymatic activities in liquid-cultured Narcissus. Plant Cell Rep. 20:22-27.
Ellington, E., T. Adserias, A. Coma, J. Bastida, F. Viladomat, and C. Codina. 1997. Effect of paclobutrazol on in vitro culture of Colchicum autumnale corms. Acta hortic. 447:131-133.
Graebe, J.E. 1987. Gibberellin biosynthesis and control. Annu. Rev. Plant Physiol. 381:419-465.
Guen-Le Saos, F., A. Hourmant, F. Esnault, and J.E. Chauvin. 2002. In vitro bulb development in schaliot (Allium cepa L. Aggregatum Group): effects of anti-gibberellins, sucrose and light. Ann. Bot. 89:419-425.
Hazarika, B.N. 2003. Acclimatization of tissue -cultured plants. Current Sci. 85:1704-1712.
Ilczuk, A., T. Winkelmann, S. Richartz, M. Witomska, and A. Serek. 2005. In vitro propagation of Hippeastrum × chmielii Chm. - influence of flurprimidol and the culture in solid or liquid medium and in temporary immersion systems. Plant Cell, Tissue Organ Cult. 83:339-346.
Kim, E.K., E.J. Hahn, H.N. Murthy, and K.Y. Paek. 2003. High frequency of shoot multiplication and bulblet formation of garlic in liquid cultures. Plant Cell, Tissue Organ Cult. 73:231-236.
Kim, H.J., J.N. Lee, K.D. Kim, J.S. Im, H.T. Lim, and Y.R. Yeoung. 2011. Suitable hormone-free medium for in vitro mass propagation via bioreactor culture of ever-bearing strawberry. J. Plant Biotechnol. 38:221-227.
Lee, J.N., H.J. Kim, K.D. Kim, Y.S. Kwon, J.S. Im, H.K. Lim, and Y.R. Yeoung. 2010. In vitro mass propagation and economic effects of bioreactor culture in ever-bearing strawberry ‘Goha’. Kor. J. Hort. Sci. Technol. 28:845-849.
Lee, J.N., H.J. Kim, K.D. Kim, J.S. Im, H.T. Lim, and Y.R. Yeoung. 2012. Growth characteristics and economic efficiency of nursery plants production according to transplanting container for acclimatization of mass propagated plantlets via bioreactor culture of ever-bearing strawberry ‘Goha’. Kor. J. Hort. Sci. Technol. 30:437-441.
McClelland, M.T. and M.A.L. Smith. 1990. Vessel type, closure, and explants orientation influence in vitro performance of five woody species. Hortic. Sci. 25:797-800.
Sansavini, S. P. Rosati, D. Gaggioli, and M.F. Toshi. 1990. Inheritance and stability of somaclonal variation in micro-propagated strawberry. Acta Hortic. 280:375-384.
Smith, E.F., A.V. Roberts, J. Mottley, and S. Denness. 1991. The preparation in vitro of chrysanthemum for transplantation to soil. 4. The effect of eleven growth retardants on wilting. Plant Cell, Tissue Organ Cult. 27:309-313.
Sutter, E.G. 1988. Stomata and cuticular water loss from apple, cherry, and sweet-gum plants after removal from in vitro culture. J. Am. Soc. Hortic. Sci. 113:234-238.
Sutter, E.G. and R.W. Langhans. 1979. Epicuticular wax formation on Carnation plantlets regenerated from shoot-tip culture. J. Am. Soc. Hortic. Sci. 104:493-496.
Wardle, K., E.B. Dobbs, and K.L. Short. 1983. In vitro acclimati-zation of aseptically cultured plantlets to humidity. J. Am. Soc. Hortic. Sci. 108:386-389.
Ziv, M. 1989. Enhanced shoot and cormlet proliferation in liquid cultured Gladiolus buds by growth retardants. Plant Cell, Tissue Organ Cult. 17:101-110.
Ziv, M. 1990. The effect of growth retardants on shoot proliferation and morphogenesis in liquid cultured Gladiolus plants. Acta Hortic. 280:247-258.






