서 언
멜론(Cucumis melo L.)은 기원전 13세기에 고대 이집트의 사원벽화와 중국의 ‘이아(爾雅)’라는 책에 소개된 이후 지금까지 3천년 넘게 동서양에 걸쳐 널리 재배되고 있는 채소이다(Lee, 2013). 우리나라에서는 멜론은 주로 온실 내에서, 그리고 참외(Cucumis melo var. makuwa Makino)는 재배면적의 82.8%를
온실에서 연작하여 재배하고 있으며, 이로 인한 토양 전염성 병원균의 증가로 피해가 급증하고 있다(Park et al., 1996; MAFRA, 2016).
멜론(참외 포함) 재배에서 발생하는 주요 병해 중 하나인 덩굴쪼김병은 Fusarium oxysporum f. sp. melonis에 의해 발생하며, 전세계적으로 심각한 수량 손실을 일으킨다(Katan et al., 1994; Zitter, 1999). F. oxysporum f. sp. melonis는 멜론의 뿌리로 침입한 후, 기주의 도관에 정착하여 식물에 시들음 증상을 일으키고 결국 식물체를 고사시킨다. 또한 멜론 덩굴쪼김병균은 토양전염성 병원균이고 내구성이 우수한 후막포자를 생산하므로 토양에 한 번 유입되면 오래 동안 생존하여 연작장해를 일으킨다(Banihashemi and DeZeeuw, 1975).
멜론 덩굴쪼김병 방제를 위해서는 저항성 대목 품종을 이용한 접목 재배가 효과적인 방법으로 고려되고 있으나(Cohen et al., 2002; King et al., 2008), 시간과 노동력이 많이 요구되어 비용이 증가하는 문제점이 있다. 그리고 태양열 소독과 담수 등의 다양한 토양관리 방법이 있으나 기후에 영향을 많이 받는 등 실용적이지 못하다(Shlevin et al., 2004; Tamietti and Valentino, 2006). 또한 비기주 작물과의 윤작 방법이 있으나 여러 가지 이유로 용이하지 않다(Crino et al., 2007). 따라서 저항성 품종의 재배는 멜론의 덩굴쪼김병을 방제하기 위한 가장 효과적인 방법으로 알려져 있다(Freeman et al., 2002; Oumouloud et al., 2013; Kim et al., 2016).
멜론의 덩굴쪼김병 저항성 유전자는 Fom-1과 Fom-2가 알려져 있으며(Risser et al., 1976), 이들 저항성 유전자는 단인자 우성유전을 한다(Messiaen et al., 1962; Risser et al., 1976). 그리고 F. oxysporum f. sp. melonis의 race는 이들 저항성 유전자를 도입한 멜론 품종에 덩굴쪼김병을 일으킬 수 있는지에 따라 race 0, 1, 2, 그리고 1,2로 구분한다(Risser et al., 1976). 즉, race 0는 저항성 유전자가 없는 감수성 품종에만 병을 일으키는 균주이고, race 1은 감수성 품종과 Fom-1 저항성 유전자를 가지는 멜론 품종에 병을 일으키는 균주이며, race 2는 감수성 품종과 Fom-2 저항성 유전자가 도입된 저항성 품종에 병을 일으키는 균주이다. 그리고 race 1,2(race 3)는 Fom-1과 Fom-2 둘 다 가지는 품종에도 병을 일으키는 균주로 보고되어 있다. Race 1,2는 병징에 따라 식물이 고사되기 전에 황화증상이 나타나는 race 1,2y와 식물 고사되기 전에 황화증상 없이 시들음 증상이 나타나는 race 1,2w로 구분하기도 한다(Bouhot, 1981).
이와 같이 F. oxysporum f. sp. melonis는 4개의 race가 보고되었으나, 미국에서는 race 2가 우점하고 있으며, 유럽에서는 race 1이 가장 많이 분포하고 있다(Martyn and Gordon, 2017). 일본의 경우에는 race 0과 2가 광범위하게 분포하고 있고, race 1과 1,2y가 제한적인 지역에서 보고되고 있다(Namiki et al., 1998, 2000). Race 1,2에 대한 저항성 멜론 품종은 아직 개발된 적이 없으나, race 0, 1 그리고 2에 대한 저항성 멜론 품종은 미국, 일본, 프랑스 등에서 판매되고 있다(Zink, 1992; Matsumoto et al., 2011). 하지만 우리나라에서는 멜론 덩굴쪼김병균의 race에 대한 보고가 거의 없으며, 판매하고 있는 덩굴쪼김병 저항성 멜론 품종들도 무슨 race에 저항성인지 거의 알려져 있지 않다. 이와 같은 이유로 덩굴쪼김병 저항성으로 판매하고 있는 품종이 포장에서 종종 덩굴쪼김병이 발생하고 있어 혼란을 야기하고 있는 실정이다.
이 연구에서는 멜론 덩굴쪼김병균인 F. oxysporum f. sp. melonis 7개 균주들의 race를 동정하고, race 0, 1 및 2 균주를 사용하여 국내에서 시판 중인 멜론 22개 품종의 덩굴쪼김병균에 대한 저항성을 조사하였다.
재료 및 방법
덩굴쪼김병 균주
고령 지역에서 분리한 F. oxysporum f. sp. melonis GR 균주(Lee et al., 2015b), 농업유전자원센터(KACC)로부터 분양받은 F. oxysporum f. sp. melonis KACC 43205, 43206, 43207 균주, 그리고 ㈜농우바이오로부터 분양받은 F. oxysporum f. sp. melonis GR65, Fom10, Fom12 균주를 실험에 사용하였다.
식물체 준비
Race 판별용 멜론 품종 4종(‘Charentais-T’, ‘Charentais Fom-1’, ‘Charentais Fom-2’, ‘MR-1’)은 농업유전자원센터로부터 분양받아 증식하여 실험에 사용하였다(Risser et al., 1976). ‘Charentais-T’는 저항성 유전자가 없는 일반 품종, ‘Charentais Fom-1’와 ‘Charentais Fom-2’는 각각 Fom-1과 Fom-2 저항성 유전자가 도입된 멜론 품종, 그리고 ‘MR-1’은 Fom-1과 Fom-2 저항성 유전자를 모두 갖고 있는 멜론 품종이다(Zink and Thomas, 1990). 그리고 시판 중인 멜론 품종들의 F. oxysporum f. sp. melonis race 0, 1 및 2 균주들에 대한 저항성 조사를 위해서는 멜론 품종 22종을 시중에서 구입하여 실험에 사용하였다(Table 1).
멜론 품종들은 5 × 8 연결포트(포트 당 토양 70mL, Bumnong, Jeongup, Korea)에 원예용상토 5호(Punong, Gyeongju, Korea)를 넣고 종자를 1립씩 파종하여 온실(25 ± 5°C)에서 7일 동안 재배하여 실험에 사용하였다.
Table 1. List of the 22 commercial melon cultivars used in this study
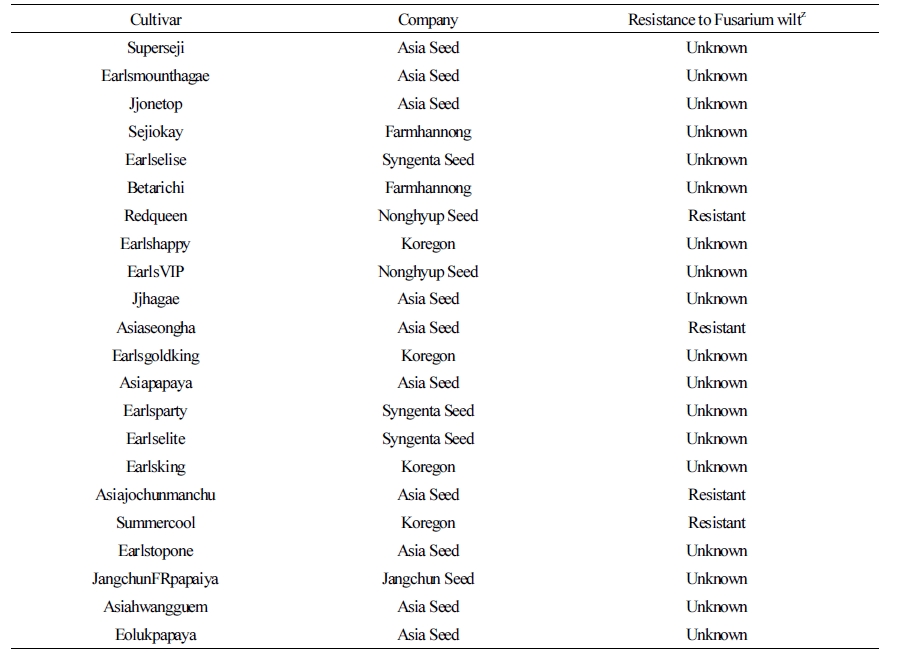 |
zThe disease resistance information of the melon cultivars was provided by the seed company. |
접종원 준비
Potato dextrose agar(PDA; Becton, Dickinson and Co., Sparks, MD, USA ) 배지에 F. oxysporum f. sp. melonis 균주를 접종하고 25°C에서 7일 동안 배양한 균총으로부터 균사 조각을 떼어 V8-juice broth(V8 juice(Campbell Soup Co., Camden, NJ, USA) 200 mL, CaCO3 3g(Samchun Chem. Co., Ltd., Pyeongtaek, Korea), distilled water 1L) 배지에 접종한 뒤 이를 25°C 암상태에서 7일 동안 150rpm으로 진탕배양하였다. 그리고 배양액을 4겹의 거즈로 걸러 균사를 제거하고 원심분리한(9,820g, 4°C, 10분; Beckman Coulter Inc., Brea, CA, USA) 후에 상징액(배양여액)은 버리고 침전물(포자)을 수확하였다. 여기에 멸균수를 붓고 잘 흔들어 포자를 현탁한 뒤에 광학현미경(Nikon Instruments Inc., Melville, NY, USA) 하에서 Paul Marienfeld GmbH & Co. KG, Lauda-Konighofen, Germany를 이용하여 포자의 농도를 조사하고, 멸균수로 희석하여 포자농도가 각각 3.3×105와 1.0×106conidia/mL인 포자현탁액을 준비하였다.
병원균 접종 및 발병
F. oxysporum f. sp. melonis의 race를 검정하기 위하여 뿌리침지법으로 접종하였다(Lee et al., 2015b). 재배하고 있던 포트로부터 멜론 유묘를 뽑고 뿌리를 물로 세척하여 흙을 제거한 후에 3.3×105conidia/mL 농도의 포자현탁액에 30분 동안 침지하여 접종하였다. 그리고 5×8 연결 포트(포트당 토양 80mL, 범농)에 원예용상토 5호(부농)를 넣고 접종한 멜론 유묘를 이식하였다. 멜론 유묘는 25°C 습실상에서 1일 동안 배양한 후에 25°C 생육실에서 하루에 12시간씩 광(55µmol·m-2·s-1)을 조사하면서 6일 동안 재배하고, 다시 28°C 생육실로 옮겨서 동일한 방법으로 재배하였다.
시판 멜론 품종의 덩굴쪼김병 저항성 검정은 scalpel 접종방법을 이용하여 실험하였다(Lee et al., 2015a). 멜론 식물체의 지제부에서 1cm 떨어진 곳에 45° 각도, 3cm 깊이로 scalpel을 삽입하여 뿌리에 상처를 준 뒤에 여기에 1.0×106conidia/mL 농도의 포자현탁액을 포트 당 10mL씩 관주하여 접종하였다. 접종한 멜론 유묘는 25°C 습실상에서 1일 동안 배양한 후에 25°C 생육실로 옮겨서 하루에 12시간씩 광(55µmol·m-2·s-1)을 조사하면서 재배하였다.
덩굴쪼김병 발병도 조사
접종 3주 후에 각 식물체의 덩굴쪼김병 발생 정도(disease severity)를 조사하였는데, Lee et al.(2015a)이 제시한 발병도(disease index) 사진을 참조하여 다음과 같은 기준으로 실시하였다. 0 = 건전, 1 = 도관이 갈변되고 생육이 약간 억제된 것, 2 = 도관이 갈변되고 생육이 억제된 것, 3 = 도관이 갈변되고 생육이 심하게 억제되고 황화된 것, 4 = 고사 등 5단계로 하였다. 저항성 판정은 평균 발병도가 1.0 이하인 경우에는 저항성, 1.1-2.5는 중도저항성, 2.6 이상은 감수성으로 하였다.
모든 실험은 처리 당 10개 식물체를 접종하였으며 실험은 2회 반복 수행하였다. 그리고 이 결과들은 SAS(SAS 9.1, SAS Institute Inc., Cary, NC) 프로그램을 이용하여 ANOVA 분석을 하고 처리 평균간 비교를 위하여 Duncan’s multiple range test(p = 0.05)를 실시하였다.
결과 및 고찰
멜론 덩굴쪼김병균 race 동정
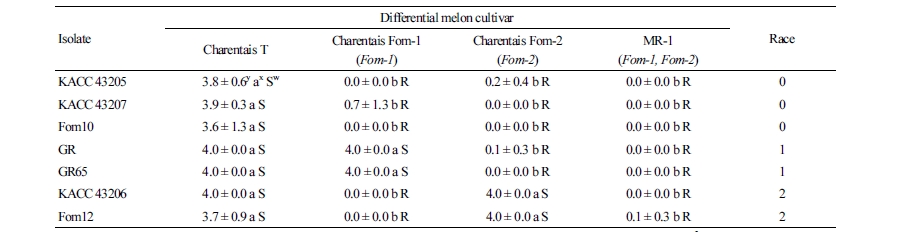
Risser et al.(1976)의 방법에 따라 F. oxysporum f. sp. melonis 7개 균주들의 race를 동정한 결과, race 0, 1, 2로 동정된 균주는 각각 3, 2, 2개였다(Table 2). KACC 43205와 43207 그리고 Fom10 균주는 실험한 4개 판병품종 중 ‘Charentais T’에만 발병도 3.6 이상의 심한 덩굴쪼김병을 일으키고 나머지 3개 품종에서는 0.7 이하의 낮은 발병도를 보여 race 0으로 동정하였다. 그리고 GR과 GR65 균주는 감수성 품종과 Fom-1 저항성 유전자가 도입된 ‘Charentais Fom-1’에서만 4.0의 높은 발병도를 보여 race 1로 동정하였다. 한편 KACC 43206과 Fom12는 감수성 품종과 Fom-2 유전자가 도입된 ‘Charentais Fom-2’에서만 3.7 이상의 높은 발병도를 보였고 나머지 품종에서는 저항성을 나타내어 이들 균주는 race 2로 동정하였다.
세계적으로 F. oxysporum f. sp. melonis는 4개의 race가 보고되어 있으며, 지역마다 우점하는 race가 서로 다르다. 미국에서는 race 2가, 그리고 유럽에서는 race 1이 가장 많이 분포하고 있다(Martyn and Gordon, 2017). 그리고 일본의 경우에는 race 0과 2가 광범위하게 분포하고 있다(Namiki et al., 1998, 2000). 하지만 우리나라에서는 멜론 덩굴쪼김병균의 race 분포에 대한 보고가 없어 우점하고 있는 race 또한 알 수 없는 실정이다.
본 연구에서도 기존에 보고된 바와 같이 Fom-1과 Fom-2가 도입된 품종들은 F. oxysporum f. sp. melonis에 대하여 중도저항성이 아닌 높은 감수성 혹은 저항성을 나타냈다(Table 2). 이는 Messiaen et al.(1962)이 보고한 바와 같이 Fom-1과 Fom-2 저항성 유전자가 단인자 우성유전을 하는 질적 저항성(qualitative resistance)이기 때문으로 생각되었다. 그리고 전 세계적으로 최근 race 1,2가 확산되고 있다고 보고되고 있는데(Veloso et al., 2000; Perchepied and Pitrat, 2004; Herman and Perl-Treves, 2007), 실험한 7개 균주 중에 race1,2로 동정된 균주는 없었지만 race 1,2 균주가 우리나라에 이미 존재하고 있을 가능성은 배제할 수 없다. 따라서 우리나라 멜론 재배지역에서 보다 많은 균주를 확보하여 race를 동정하는 것이 필요하다.
시판 품종의 저항성
Scalpel 접종법(Lee et al., 2015a)을 이용하여 세 가지 race, 즉 KACC 43207(race 0), GR(race 1), KACC 43206(race 2) 균주들에 대한 시판 중인 멜론 22개 품종의 저항성을 실험한 결과, 실험한 품종들은 모두 3.5 이상의 높은 발병도를 보이거나 1.0 이하의 낮은 발병도를 나타냈으며 중도저항성 반응을 나타내는 품종은 없었다(Fig. 1).
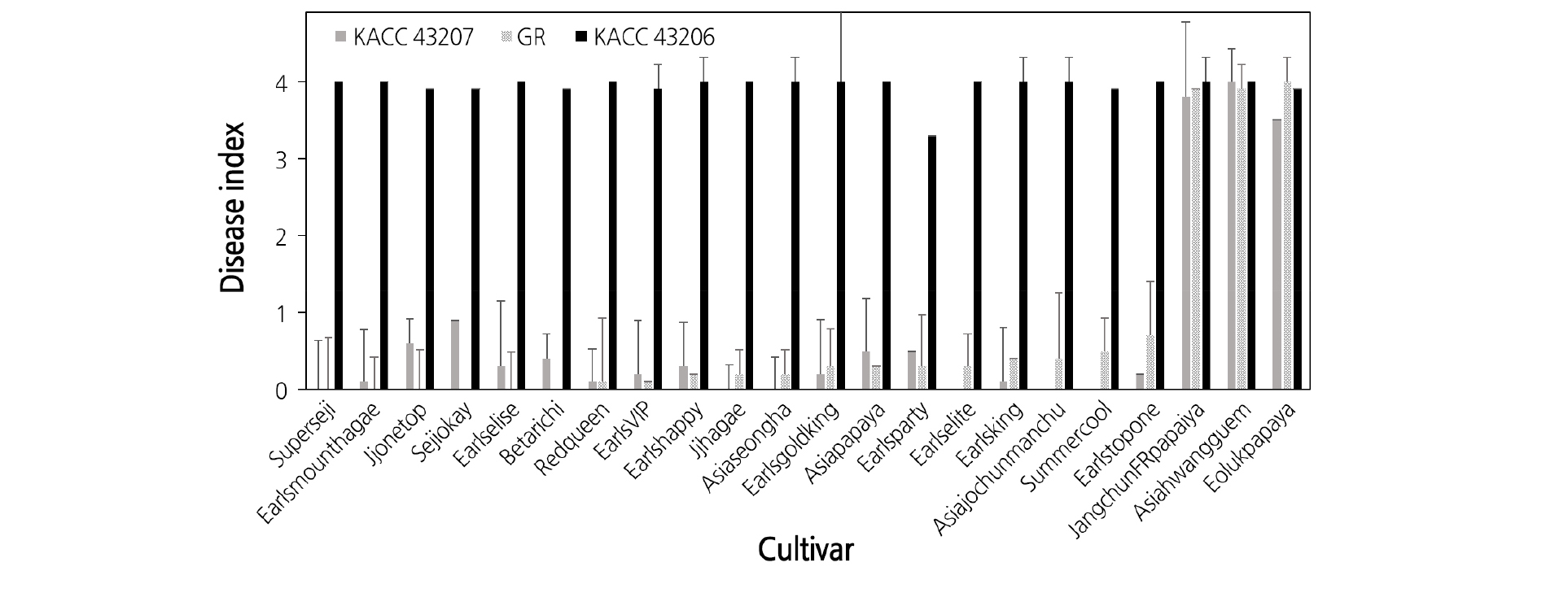
Fig. 1. Resistance of 22 commercial melon cultivars to 3 isolates of Fusarium oxysporum f. sp. melonis, KACC43207 (race 0), GR (race 1), and KACC43206 (race 2). Seven-day-old seedlings were inoculated with F. oxysporum f. sp. melonis by cutting the roots with a scalpel and then applying a 10-mL aliquot of the spore suspension (1.0× 106conidia/mL) on the soil. The inoculated plants were incubated in a dew chamber at 25˚C for 24 hours and then transferred to a growth room at 25˚C with 12 hour light a day. After 3 weeks, the disease severity of the seedlings was investigated on a scale of 0-4.
실험한 품종 중 ‘장춘FR파파이야’, ‘아시아황금’, ‘얼룩파파야’ 등 3개 품종은 실험한 모든 균주로 접종하였을 때 모두 3.5 이상의 높은 발병도를 보여 감수성 품종으로 생각되었다(Fig. 1) 그리고 이들 품종을 제외한 나머지 19개 품종은 race 1 균주인 GR 균주를 접종하였을 때에는 모두 1.0 이하의 낮은 발병도를 보여 이 품종들은 race 1 균주에 대한 높은 저항성을 나타내는 품종임을 알 수 있었다(Fig. 1). 그리고 race 2 균주인 KACC43206을 접종하였을 때에는 19개 품종 모두 3.9 이상의 높은 발병도를 보여 이들 품종은 race 2 균주에 대해 높은 감수성을 나타낸다는 것을 알 수 있었다.
양적저항성의 경우에는 접종 농도와 접종하는 식물의 생육 시기에 따라 저항성 반응이 다르게 나타나나(Barkadale et al., 1984; Kim et al., 1989; Jo et al., 2014; Jo et al., 2016; Park et al., 2016), 멜론의 덩굴쪼김병에 대한 저항성은 단인자 우성유전자인 Fom-1과 Fom-2에 의해 나타나므로 이론적으로는 중도저항성이 나타날 수 없다. 하지만 Lee et al.(2015b)에서 22개 멜론 품종을 root-dipping 방법으로 접종하였을 때 3개 품종은 감수성, 4개 품종은 저항성, 그리고 15개 품종은 중도저항성을 보였다고 하였다. Lee et al.(2015a)은 root-dipping 방법에서 멜론 품종들이 중도저항성을 보이는 원인을 병원균을 접종한 후에 이식한 멜론이 잘 활착하지 못하여 일어난 결과로 생각하고, 이를 개선하기 위한 scalpel로 상처를 내고 병원균을 관주접종하는 scalpel 접종방법을 개발하였으며, 이 방법으로 실험하면 멜론의 저항성과 감수성이 명확히 구분된다고 하였다. 본 연구에서도 22개 품종에 3가지 균주를 각각 접종하여 덩굴쪼김병 저항성을 조사하는 실험으로 실험하는 개체의 수가 많음에도 실험한 모든 품종은 중도저항성을 나타내는 품종 없이 모두 높은 저항성 혹은 감수성을 보여 scalpel 접종법이 멜론 덩굴쪼김병에 대한 병리검정에서 효과적인 접종 방법임을 알 수 있었다.
멜론의 덩굴쪼김병 저항성 유전자로 Fom-1과 Fom-2가 알려져 있으며, F. oxysporum f. sp. melonis의 race는 이들 저항성을 극복하느냐에 따라 race를 동정할 수 있다(Risser et al., 1976). 즉 Fom-1을 침해할 수 있으면 race 1, Fom-2를 극복할 수 있으면 race 2, 그리고 Fom-1과 Fom-2 모두를 극복할 수 있으면 race 1,2로 명명한다. 실험한 22개 품종 중 ‘장춘FR파파이야’, ‘아시아황금’, ‘얼룩파파야’의 3개 품종를 제외한 19개 품종은 race 0와 race 1에는 저항성을 나타내고 race 2에 대해서는 감수성을 나타냈다(Fig. 1). 따라서 이들 19개 멜론 품종은 ‘Fom-2’ 저항성 유전자가 도입된 품종이라고 생각되었다.
실험한 22개 멜론 품종들 중 종자회사에서 멜론 덩굴쪼김병균에 대한 저항성 품종으로 공시한 품종은 4개 품종이었지만, 종자회사에서 저항성 품종으로 공시하지 않은 품종 15개도 race 0와 race 1 균주에 대하여 높은 저항성을 나타냈다(Fig. 1). 병 저항성 품종이 고부가가치 종자임을 고려한다면 종자회사에서는 본 연구에서 사용한 scalpel 방법을 이용하여 멜론 덩굴쪼김병에 대한 병리검정을 수행하여 race에 대한 저항성이 규명된 저항성 품종을 판매하는 것이 바람직할 것으로 생각되었다.