서 언
재료 및 방법
실험 재료
물리화학적 특징 측정
시료 추출물의 제조
총 페놀성 화합물 함량 측정
FRAP법에 의한 항산화능 측정
DPPH Radical 소거능 측정
Flavonoid 함량 측정
통계처리
결과 및 고찰
유자의 물리적 특성
총 페놀함량
항산화활성
Flavonoid 함량
서 언
유자(Citrus junos Sieb. ex Tanaka)는 운향과 감귤속 후생감귤아속에 속하는 상록관목의 열매로 감귤, 오렌지, 자몽 등이 과육을 위주로 이용하는 것과는 달리 과피까지 이용할 수 있으며 중국, 일본, 우리나라에서 주로 재배되고 있는 과일이다. 우리나라에서는 전남 및 경남지역의 남해안 일대, 제주도에서 주로 재배되어지며, 유자는 감귤류 중 가장 추위에 강한 종으로 특유의 진한 향과 비타민 C가 다량 함유되어 있고 카로티노이드, 무기질, 구연산 등의 함량이 높아 건강식품의 이미지를 갖고 있어 그 활용범위가 광범위하다(Ji et al., 2008). 민간에서는 고미건위제, 진해거담제, 감기약으로 사용되는 등 그 효능이 이미 잘 알려져 있으며(Shin et al., 2009) 최근 논문에서 보면 질병을 억제하는 이러한 여러가지 약리 효과는 항산화 역할을 하는 비타민 C와 E 그리고 과일에 많이 들어있는 polyphenol과 flavonoids라는 물질으로 알려져 있다(Hertog et al., 1993; Vinson et al., 2001). 유자를 포함하는 감귤류의 과피에 많이 함유되어 있는 flavonoid류의 하나인 Naringin은 인체에 독성이 없고 콜레스테롤 억제효과와 백혈병 세포를 정상세포로 변화시키는 작용, 유방암 세포증식 저해작용이 있으며, 항산화 효과, 항염증, 천연 항균제로 알려져 있어 다양한 생리 기능성을 가진다(Chae et al., 2008; Lee et al., 2011; Yang and Eun, 2011). Hesperidin은 Naringin과 마찬가지로 감귤류의 과피에 다량 함유되어 있으며 혈중 콜레스테롤 농도 상승억제작용, 지방간 개선작용 및 간 종양세포 증식억제작용 등과 그 외 항산화 작용, 혈압강하작용, 항알러지작용 등의 생리활성 물질로 알려져 있다(Woo, 2000). 하지만 유자나무는 가시가 많아 과일에 상처가 많으며 기후에 의한 피해로 인해 폐과량이 40% 정도에 이르기도 하며 수확시기가 11월 12월로 한정되어 있어 유자의 부가가치 향상을 위해 가공방법이 사용되고 있으며 주로 설탕을 이용한 유자청이나 유자차 등의 음료로 가공이 되어져왔다. 또한 근래 들어서는 소스로 식품조리 및 목욕 미용용품에 많이 이용되고 있으며 분말이나 착즙액 형태로 첨가한 다양한 연구들이 진행되어 있다(Shin et al., 2009). 현재 감귤류에 대한 논문은 감귤류의 성분과 특성, 품종 및 수확시기별 품질특성과 이화학적 성분비교에 대한 연구가 보고 되어져 있으며(Yang et al., 2012) 유자에 대한 연구는 다른 분야에 비해 미흡한 실정이다. 이러한 이유는 수확시기가 한정되어 있어 저장과정 중 부패과의 발생, 향 손실 등으로 인해 장기보관이 힘들며 주로 가공식품으로서 사용되고 있고 재배지역이 전라남도 고흥, 남해, 완도, 제주 등 남부지방으로 한정되어 있기 때문인 것으로 사료된다. 본 연구에서는 현재 전라남도 고흥과 제주도에서 재배되고 있는 유자의 수확시기에 따른 플라보노이드의 함량 변화 및 항산화성을 탐색하여 산업적인 활용 및 기능성 구명을 위한 기초자료를 제공할 뿐 아니라 유자의 부가가치 증진을 도모하고자 수행하였다.
재료 및 방법
실험 재료
본 연구의 공시재료인 유자(Citrus junos Sieb. ex Tanaka)는 2012년 8월부터 12월까지 매월 1일을 기준으로 전라남도 ‘고흥’과 제주도 ‘서귀포시’에서 수확된 것을 농촌진흥청 감귤시험연구소로부터 제공받아 사용하였으며, 수확시기에 따라 Aug.(8월 1일 수확), Sep.(9월 1일 수확), Oct.(10월 1일 수확), Nov.(11월 1일 수확), Dec.(12월 1일 수확)으로 구분하여(Fig. 1), -70°C의 초저온냉동고에 보관한 후 실험재료로 사용하였다.
물리화학적 특징 측정
유자의 산지 및 수확시기에 따라 종경, 횡경, 과중, 당도, 구형지수, 수분함량의 물리화학적 특징을 측정하였다. 과중은 수확일에 각각 10개씩의 과실의 무게를 저울로 측정하여 평균 과중으로 표시하였고 종경과 횡경은 수확일에 각각 10개씩의 과실의 지름과 높이를 caliper(Digimatic caliper, Mitutoyo Corp., Japen)를 이용하여 지름은 과실의 폭을 과실의 높이의 중간지점을 기준으로 측정, 높이는 꼭지를 바닥에 놓고 수직으로 길이를 측정하였으며 과형지수는 높이 대비 지름값으로 계산하였다. 당도는 수확일에 각각 5개씩의 과실의 즙을 짜서 디지털당도계(Pocket refractometer PAL-1, Atago, Japan)를 사용하여 °Brix값을 측정하였다. 수분함량은 동결건조기(Lyophilizer 7754042, Labconco, USA)를 이용하여 샘플을 완전히 건조시킨 후 중량분석을 통해 수분 손실량을 측정하였다.
시료 추출물의 제조
수집된 유자는 수확시기에 따라 무작위로 5개의 구를 흐르는 물에 씻은 후 물기를 제거한 다음 잘게 썰은 시료 과실 20g에 99.5% ethanol 100mL을 가해 실온에서 100rpm의 속도로 균질화 하였으며, 25°C의 진탕배양기에서 5시간동안 150rpm으로 추출한 후 1시간동안 상온에 방치하여 3회 반복하여 추출하였다. 추출물은 Whatman No. 2 여과지로 감압여과한 후 회전식 감압농축기(EYELA Rotary evaporator N-1000, Tokyo aikakikai Co. LTD, Japan)를 사용하여 수조 온도를 30°C로 설정한 후 감압, 농축하여 0.2g・mL-1 농도로 제조하여 -70°C의 초저온 냉동고에 보관하며 실험에 이용하였다.
총 페놀성 화합물 함량 측정
총 페놀성 화합물 함량은 Singleton and Rossi(1965)의 Folin-Denis의 방법을 이용하여 측정하였으며, 추출물 100μL에 2.3mL의 증류수와 400μL Folin-Ciocalteau’s reagent를 차례로 가하고 7분동안 반응시킨 후, 1.2mL의 20% sodium carbonate를 첨가하여 vortex를 통해 잘 섞어 상온의 암실에서 1시간동안 정치한 후 UV spectrometer(UV-1201, SHIMADZU, Japen)를 통해 765nm의 파장에서 흡광도를 측정하였으며 gallic acid(Sigma-Aldrich, USA)를 표준물질로 사용하여 시료와 동일한 방법으로 분석하여 얻은 표준감량선을 이용하여 총페놀 함량을 산출하였다.
FRAP법에 의한 항산화능 측정
Ferric reducing antioxidant power(FRAP)법에 의한 항산화력은 Benzie and Strain(1996)의 방법을 변형하여 측정하였다. FRAP reagent는 1.87g의 sodium acetate를 acetic acid 16mL와 증류수 1L에 녹여 pH를 3.6으로 맞춘 300mmol・L-1의 buffer reagent와 0.1562g TPTZ를 40mM HCl 용액 50mL에 넣고 녹여만든 10mM의 TPTZ reagent, 0.2703g의 Iron chloride hexahydrate를 50mL 증류수에 녹여만든 20mM FeCl3・6H2O를 전처리 시약으로 준비해 두고 300mmol・L-1 buffer reagent 100mL, 10mM TPTZ 10mL, 20mM FeCl3・6H2O3 10mL을 각각 넣고 섞어 FRAP 시험용액으로 사용하였다. 각 시료 100μL에 증류수 300μL를 가한 후, 3mL의 FRAP 시험용액을 첨가하여 37°C에서 90분동안 정치한 다음 UV spectrometer(UV-1201, SHIMADZU, Japen)를 통해 593nm의 파장에서 흡광도를 측정하였으며 Trolox(Sigma- Aldrich, USA)를 표준물질로 사용하여 시료와 동일한 방법으로 분석하여 얻은 표준감량선으로부터 FRAP 함량을 산출하였다.
DPPH Radical 소거능 측정
1,1-diphenyl-2-picrylhydrazyl(DPPH) 라디칼 소거능은 Blois (1958)의 방법을 변형하여 측정하였으며, 1 × M의 DPPH를 만든 후 상온의 암실에서 12시간동안 교반시킨 후 사용하였다. 각 시료 0.25mL에 100% Ethaol 0.25mL, DPPH reagent 2.5mL를 순서대로 섞어 80분동안 상온의 암실에서 정치하여 UV spectrometer(UV-1201, SHIMADZU, Japen)를 통해 517nm의 파장에서 흡광도를 측정하였다. 대조군으로는 2.5mL DPPH와 0.5mL Ethanol을 순서대로 섞어 같은 전처리를 거쳐 같은 파장에서 흡광도를 측정하였으며 3반복으로 진행하였다. 이때 Trolox(Sigma-Aldrich, USA)를 표준물질로 사용하여 얻은 표준 감량선으로부터 DPPH 함량을 산출하였다.
Flavonoid 함량 측정
Naringin과 Hesperidin 함량은 Wang et al.(2008)의 방법을 변형하여 HPLC(Agilent 1100 series, Agilent Technologies, USA)로 측정하였으며 각 추출물을 0.45µm membrane filter로 통과시킨 것을 시료로 사용하였다. 분석에는 Atlantis C18 column(5μM, 4.6 × 250mm, Waters Corporation, USA)을 사용하였고, 용리액은 0.5% acetic acid(99%, Sigma Aldrich, USA)를 A용매로, acetonitrile(HPLC grade, Daejung, Korea)를 B용매로 하여 이동상으로 gradient를 주어 사용하였으며 유속은 1mL・min-1, 시료는 10μL를 injection하여 분석하였다. 이동상의 용매 구배는 A:95%, B:5%로 시작하여 10분에 A:90%, B:10%, 20분에 A:84%, B:16%, 40분에 A:80%, B:20%, 50분에 A:50%, B:50%로하여 55분까지 분석하였고 Binary pump(Agilent 1100 series-DE43618438, Agilent, USA)와 UV detector(Agilent 1100 series-DAD: G1315B, Agilent, USA)를 사용하여 280nm에서 측정하였다. 표준용액으로 Naringin(95%, Fluka Chemie AG, Buchs, Switzerland)과 Hesperidin(95%, Fluka Chemie AG, Buchs, Switzerland)을 Ethanol에 녹여 각각 1, 0.5, 0.2, 0.1, 0.05, 0.02mg・mL-1의 농도로 제조하여 peak면적을 구하고 회귀방정식을 이용한 검량선을 작성하여 정량하였다.
통계처리
본 실험은 3반복으로 실시한 결과를 통계분석 SAS프로그램(SAS, 9.2, Institute Inc., USA)를 이용하여 분산분석(ANOVA)을 하였으며 Duncan의 다중검정(DMRT; Duncan’s multiple range test)를 이용하여 p ≤ 0.05 수준에서 유의성을 검증하였다.
결과 및 고찰
유자의 물리적 특성
유자의 산지별 수확시기에 따른 물리적 특성으로 과실의 중량, 크기, 당도, 과형지수, 수분함량을 측정하여 Table 1에 나타내었으며, 8월부터 12월까지 수확한 유자의 외관특성은 Fig. 1에 나타내었다. 8월 수확한 유자는 진한 초록색으로 수확시기가 지날수록 점점 노란색으로 착색이 되는 양상을 보였다. 유자의 경우 과실의 중량은 9월 유자는 8월 유자의 2배에 가까웠으며, 그 이후로는 30일 간격으로 약 1.3배씩 증가하다가 수확 적기인 11월, 12월에는 비슷한 중량을 유지하였고 고흥과 제주도의 유자는 비슷한 양상을 보였다. 유자의 횡경은 수확시기에 따라 증가했으며, 수확 적기인 11월, 12월은 50mm이상의 크기를 유지하였고 종경 또한 수확시기가 지날수록 증가하였으며 횡경의 변화에 비해 증가되는 비율이 더 큰 경향을 보였다. 과실의 모양을 알 수 있는 과형지수(fruit shape index, Height/Diameter)는 8월 수확한 유자는 1에 가까웠으나 수확시기가 지날수록 감소하였고 이로부터 구형에서 수확시기가 지날수록 타원형의 형태를 유지하는 것을 확인하였다. 당도(°Brix)는 8월에 비해 9월 수확한 유자의 °Brix값이 약간 감소 하였으나 11월부터는 다시 증가하는 양상을 보였고, 수분함량은 86-97%로 나타났다.
총 페놀함량
산지별 유자의 수확시기에 따른 총 페놀함량을 분석한 결과는 Table 2와 같다. 식물체에는 교유의 색과 맛을 주는 페놀성 화합물이 존재 하며 식물계에 널리 분포되어 있는 2차 대사산물의 하나로 화학적으로 다양한 구조만큼이나 다양한 역할을 식물에서 수행한다. 식물 유래 페놀성 화합물은 phenol류, phenylpropanoid, phenolic acid, flavonoid류가 대부분으로 이는 항산화, 항균, 항알러지, 고지혈증등에 예방효과가 있는 대표적인 물질로 알려져있다(Azuma et al., 1999; Kim et al., 1999). 유자의 총 페놀 함량은 8월 1일 수확된 제주도 유자가 3.06 ± 0.18mg・g-1F.W(fresh weight)로 가장 높았고 8월 1일 수확된 고흥 유자 2.48 ± 0.05mg・g-1F.W가 그 다음으로 높았으며, 12월 1일 수확된 고흥 유자가 1.45 ± 0.01mg・g-1F.W, 제주도 유자가 1.41 ± 0.12mg・g-1F.W으로 수확시기가 늦어질수록 함량이 점차적으로 감소하는 경향을 보였다.
또한 산지별 총 페놀 함량은 제주도 유자가 고흥 유자에 비해 높은 함량을 보였으며 고흥과 제주도 유자 모두 수확 적기인 11월과 12월 수확된 유자는 비슷한 햠량을 유지하였다. 이는 지각, 당유자, 홍귤 진귤 등 감귤류에서 수확시기에 따라 총페놀함량이 점차 감소되었다는 보고(Kim et al., 2009)와 같이 본 연구에서도 수확시기가 지날수록 유자의 총페놀함량이 감소되었으며, 페놀화합물이 식물체의 과실색 발현에 영향을 준다는 보고(Treutter, 2010)처럼 유자 과실이 익어갈수록 과실색이 변하면서 페놀화합물의 작용으로 함량이 줄어드는 것을 알수 있었다. 이를 통해 페놀화합물이 항산화 활성을 가진 물질로서 본 연구에서 수확시기에 따른 유자 추출물의 polyphenol 함량변화의 경향을 분석한 결과 어린 숙기의 유자를 이용하였을 때 항산화 활성 등 기능성 작물로 활용할 수 있을 것으로 판단된다.
항산화활성
산지별 수확시기에 따른 유자추출물의 항산화능은 FRAP assay와 DPPH radical 소거능을 근거로 평가하였으며, 그 결과는 Table 2와 같다. Ferric reducing antioxidant power(FRAP)에 의한 환원력 실험은 산성 pH에서 환원제에 의해 ferric tripyridyltriazine 복합체가 ferrous tripyridyltriazine으로 전환되는 과정을 이용한 것으로 추출물의 총 항산화능을 측정하는 방법으로(Jeon et al., 2012) 8월 1일 수확된 고흥 유자는 3.29 ± 0.02mg・g-1F.W, 제주도 유자는 3.81 ± 0.07mg・g-1F.W으로 높은 환원력을 보였으며, 10월 1일 수확된 고흥 유자는 1.86 ± 0.08mg・g-1F.W, 제주도 유자는 2.07 ± 0.02mg・g-1F.W, 11월 1일 수확된 고흥 유자는 2.14 ± 0.03mg・g-1F.W, 제주도 유자는 1.99 ± 0.11mg・g-1F.W로 환원력이 다소 떨어지는 경향을 보였으나, 12월 1일 수확된 고흥유자는 2.22 ± 0.06 mg・g-1F.W, 제주도 유자는 2.85 ± 0.20mg・g-1F.W으로 다시 증가하였다.
DPPH radical 소거능은 비교적 간편하고 가격이 저렴하여 가장 널리 사용되는 항산화 시험법으로 DPPH radical 소거능 측정은 항산화 물질에 의한 전자공여에 의해 지질과산화 연쇄반응에 관여하는 산화성 free radical의 억제 정도를 측정하는 방법이다. 산지별 수확시기에 따른 유자추출물에서 전자가 DPPH로부터 이탈하여 항산화 물질과 결합하는 원리를 이용하여 가사의 활성산소가 소거되었음을 나타내는 DPPH 전자공여능의 변화를 측정하였다. 8월 1일 수확된 고흥 유자는 0.4 ± 0.02mg・g-1F.W, 제주도 유자는 0.48 ± 0.04mg・g-1F.W였으며 9월 1일 수확된 고흥 유자는 0.25 ± 0.03mg・g-1F.W, 제주도 유자는 0.30 ± 0.01mg・g-1F.W으로 다소 떨어지는 경향을 보였으나 10월 1일 수확된 고흥 유자는 0.31 ± 0.01mg・g-1F.W, 제주도 유자는 0.37 ± 0.06mg・g-1F.W, 12월 1일 수확된 고흥 유자는 0.45 ± 0.04mg・g-1F.W, 제주도 유자는 0.41 ± 0.05mg・g-1F.W으로 10월 이후로 수확시기가 지날수록 점차적으로 증가하는 경향을 보였다. 이는 9월 하순에서 1월 하순까지 전자공여능이 증가되었다고 보고(Kim et al., 2009)된 결과와 비슷한 경향을 보였으며 DPPH 라디컬 소거능이 과숙성 유자에서 높았다는 보고(Yoo and Hwang., 2004)의 결과와도 비슷한 경향이었다.
FRAP법으로 측정한 것과 DPPH법으로 측정한 값의 유의적인 차이는 크게 나타나지 않았으며, 미숙과의 경우 항산화 활성이 유의적으로 가장 높았고 제주도에서 수확한 유자가 고흥산 유자보다 높은 활성을 보였으며, 수확시기가 지날수록 항산화 활성이 다소 떨어지는 경향을 보였다. 총 페놀 함량과 항산화능의 상관관계에서 총 페놀 함량이 높은 수확시기에서 DPPH와 FRAP 측정값이 가장 높았으며, 수확시기에 따른 총페놀 함량과 항산화능의 변화는 비슷한 경향을 보였다. 이는 DPPH 자유기 소거능이 총 페놀화합물의 함량과 높은 상관관계를 나타낸다는 보고(Ji et al., 2008)와 유사한 결과로 이 사실로부터 FRAP법과 DPPH법에 의한 항산화 활성은 총 페놀성 화합물과 관련이 있는 것으로 사료되며 유자의 미숙과는 식물체에 존재하는 많은 페놀성 물질과 항산화능을 보유하여 다양한 활용을 통해 여러 질병들로부터의 보호효과와 다양한 생리활성을 기대할 수 있다.
Flavonoid 함량
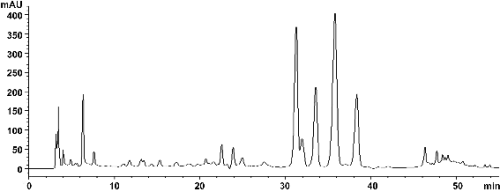
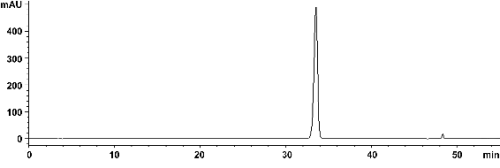
플라보노이드는 가장 방대한 식물 페놀성 화합물 중에 하나로 기본적으로 2개의 방향성 고리 구조를 가지는 15개의 탄소를 포함하는 구조를 포함하며 담황색 또는 노란색 계통의 색소화합물로서 안토시아닌, 플라본, 플라보놀, 이소플라본이 이에 속하며 실제로 많은 플라보노이드는 자연계에서 배당체로 존재한다(Böhm et al., 1998). 유자의 유효성분 중 항산화 활성이 있다고 생각되는 주요 flavonoid 성분을 정량 분석하기 위해 HPLC를 이용하였으며, 감귤류에 가장 많이 존재하는 플라보노이드 화합물로서 Naringin과 Hesperidin이 분석한 결과 확인되었다(Fig. 2A). Naringin과 Hesperidin은 Flavonon류에 속하며, 특히 과육보다 과피에 다량 함유되어 있고 세포독성을 감소시킴과 동시에 세포증식을 촉진시킨다고 보고되어 있다(Eun et al., 1996; Sohn and Kim, 1998). Naringin은 감귤류의 외피나 내피에 함유된 정유나 배당체의 일종으로 가열이나 공기와의 접촉에 의해 변질되어 품질저하를 일으키고 과실의 쓴맛성분으로 항균작용이 있다고 보고되어 있다(Shin et al., 2008). HPLC 분석결과, 확인된 Naringin은 표준물질을 농도별로 제조하여 표준곡선을 그려본 결과 R2 = 0.999임을 확인할 수 있었으며, 32.98분에 chromatogram을 얻을 수 있었다(Fig. 2B). 8월 1일 수확된 고흥 유자의 Naringin 함량은 1.18 ± 0.02mg・g-1F.W, 제주도 유자의 Naringin 함량은 1.48 ± 0.08mg・g-1F.W으로 가장 높은 함량을 보였으며, 9월 1일 수확된 고흥 유자는 0.56 ± 0.01mg・g-1F.W, 제주도 유자는 0.68 ± 0.01mg・g-1F.W으로 2배이상 감소하였고 11월 1일 수확된 고흥 유자는 0.33 ± 0.01mg・g-1F.W, 제주도 유자는 0.36 ± 0.05mg・g-1F.W로 유의적으로 감소했으며, 12월 1일 수확된 고흥 유자는 0.33 ± 0.02mg・g-1F.W로 일정하게 유지되었으나, 제주도 유자는 0.39 ± 0.15mg・g-1F.W로 약간 증가하는 경향을 보였다(Table 3). 이는 감귤류의 flavonoid 함량이 수확시기가 늦어질수록 대부분 감소하는 경향을 보이나, 품종에 따라 과숙이 될수록 함량이 다시 증가하는 품종도 있다는 보고(Kim et al., 2009)와 유사한 경향을 보였다.
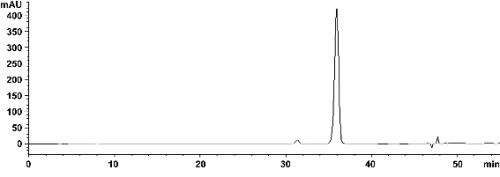
Hesperidin은 연한 노란색~연한 갈황백색의 결정 또는 결정성 가루로 무색, 무미의 치상결정을 형성하여 감귤류의 백탁 원인물질로 혈중 콜레스테롤 농도 상승억제작용, 항산화작용, 지방간 개선작용등의 작용을 나타내는 것으로 보고되어 있으며(Cha et al., 1999), HPLC를 이용하여 Hesperidin의 표준물질을 농도별로 제조하여 표준곡선을 그려본 결과 R2 = 0.999임을 확인할 수 있었으며 34.87분에 chromatogram을 얻을 수 있었다(Fig. 2C). 8월 1일 수확된 고흥 유자의 Hesperidin 함량은 1.49 ± 0.10mg・g-1F.W, 제주도 유자는 1.84 ± 0.06mg・g-1F.로 가장 높았으며, 10월 1일 수확된 고흥 유자는 0.88 ± 0.13mg・g-1F.W, 제주도 유자는 1.26 ± 0.27mg・g-1F.W, 11월 1일 수확된 고흥 유자는 0.67 ± 0.01 mg・g-1F.W, 제주도 유자는 0.68 ± 0.04mg・g-1F.W로 성숙단계가 진행될수록 유의적으로 감소하는 경향을 보였으나, 12월 1일 수확된 고흥 유자는 0.69 ± 0.07mg・g-1F.W, 제주도 유자는 0.76 ± 0.19mg・g-1F.W로 다시 증가하는 경향을 보였다(Table 3).
이로써 유자의 주요 Flavonoids성분인 Hesperidin과 Naringin의 함량은 Hesperidin이 Naringin보다 많으며, 산지별 수확시기에 따른 함량은 Naringin과 Hesperidin 모두 고흥산 유자보다 제주산 유자가 더 높은 함량을 보였고, 특히 미숙과 유자의 Hesperidin과 Naringin 함량은 수확적기 유자에 비해 월등히 높았고 수확시기가 늦어질수록 함량이 큰폭으로 감소하였다가 산지에 따라 11월 이후 다시 서서히 증가하는 경향을 보였다. 일반적으로 감귤의 수확시기별 flavonoids함량은 수확시기가 늦어질수록 감소하는 것으로 보고되어 있으며(Kim et al., 2001; Rhyu et al., 2002) 산지에 따라 다시 함량이 증가하는 것은 재배연도나 기후조건 등에 따라 나타날 수 있는 차이로 추정된다.
|
(A) Yuzu extract |
|
(B) Naringin |
|
(C) Hesperidin |
Fig. 2. HPLC profiles of ethanol extract of yuzu (Citrus junos Sieb. ex Tanaka) (A) and standards of naringin (B), hesperidin (C) detected at 280 nm. |