서 언
재료 및 방법
시험 재료
시약 및 기구
GC-ECD/MS 기기분석 조건
표준검량선 및 분석정량한계(Limit of quantitation, LOQ)
시료의 추출 및 분배
Florisil 흡착 크로마토그래피
대표 원예작물에 대한 fluazinam의 회수율 시험
결과 및 고찰
GC-ECD 분석조건의 확립
시료 추출 및 분배과정의 확립
Florisil 흡착 크로마토그래피 정제조건의 최적화
대표 원예작물에 대한 fluazinam의 분석 정량한계 및 회수율
GC/MS를 이용한 잔류분의 재확인
서 언
최근 농약은 현대농업에 있어 품질유지 및 향상을 위한 필수농업자재로써 농산물의 생산성 제고 및 품질향상에 크게 기여하 여 오늘날 풍요로운 먹거리의 공급이 가능하도록 하였을 뿐만 아니라 농산물의 생력화를 통해 노동력과 농업 생산비 절감에 중요한 역할을 함으로써 농업인의 삶 향상에 큰 공헌을 하였다(Jang et al., 2010). 농약은 농산물의 재배를 위한 필수자재이기 때문에 국가에서 사용을 허가하고 있으나, 농약의 오남용을 방지하여 국민건강에 피해를 주지 않도록 각 농약별 사용량, 사용 횟수, 수확기에 따른 살포 횟수 및 시기 등에 관한 농약안전사용기준과 농약의 최대잔류허용기준을 설정하여 사용방법과 사용 량을 엄격히 규제하고 있다(Kim et al., 2007).
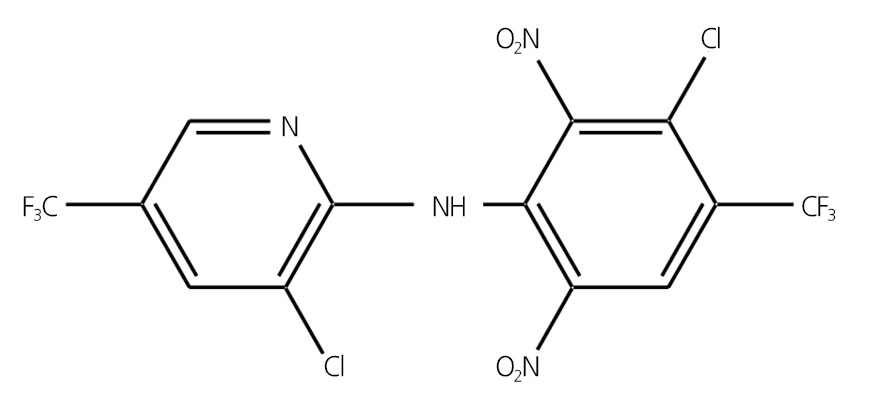
Fluazinam[3-chloro-N-(3-chloro-2,6-dinitro-4-trifluoromethylphenyl)-5-trifluoro-methyl-2-pyridinamine]은 dinitroaniline계 살균제로써 1990년에 일본 이시하라 산업에 의해 개발 및 상용화가 시작된 이후, 세계적으로 58개의 다양한 국가에서 유통 및 판매된 농약이다(Krieger, 2001).
Fluazinam은 진균류의 미토콘드리아 내막에서 ATP synthetase와 결합하여 ATP 합성을 저해하는 작용을 함으로써 진균류 에 대한 방제효과가 있으며(Guo et al., 1991), 작물체의 생장 중 포자에 의한 감염을 억제하는 데 사용되는 살균제로(Ulrich et al., 2012), 전 세계적으로 감자의 괴경 감염 예방에 효과적으로 작용하여 감자의 역병을 억제하는 데 주로 사용되고 있다(Ulrich et al., 2012).
국내에서는 배, 복숭아, 사과, 감, 감귤, 자두 및 포도 등의 과수류와 고추, 배추, 양파, 인삼 및 감자 등 다양한 원예작물의 재배 시에 발생하는 탄저병, 뿌리혹병, 뿌리마름병, 더뎅이병, 잿빛무늬병, 점무늬병, 갈색무늬병, 역병 등을 방제하는 데 사용되고 있으며, 2015년 3월 현재 입제와 분제, 수화제, 액상수화제 등이 시판되고 있다K(orea Crop Protection Association, 2015). Fluazinam의 물리화학적 특성을 살펴보면(Fig. 1), n-octanol/water 분배계수(Log Pow)가 4.0인 비극성의 중성화합물로써 녹는점은 119°C이고, 분자량은 465.09(C13H4Cl2F6N4O4)인 노란색 분말 형태의 화합물이다(United States Environmental Protection Agency. 2001). 다양한 유기용매에 잘 녹으며(acetone 645g, dichloromethane 485g, ethyl acetate 624g, methanol 162g, n-hexane 6.7gㆍL-1), 물에 대한 용해도는 극히 낮아 0.071mgㆍL-1에 불과하다(United States Environmental Protection Agency, 2001).
Dinitroaniline계 살균제인 fluazinam은 국내 농약잔류허용기준(Maximum Residue Limits; MRL)이 0.05-10mgㆍkg-1 범위 로 설정되어 있다(Ministry of Food and Drug Safety, 2014). 현재 국내 식품의약품안전처에서 발간한 식품공전에 수록된 잔류 농약분석법 4.1.2.2(Ministry of Food and Drug Safety, 2012)에 SPE(Solid phase extraction) 정제 후 GC-ECD(Gas chromatography-electron capture detector)로 분석하는 방법이 수재되어 있으나, 다성분 분석 및 SPE 정제로 인해 재현성 및 정제도가 불량하고, 또한 기존에 GC-ECD나 LC/MS를 이용하여 분석한 바 있으나(Hu et al., 1997; Kim et al., 2010), 대상농 약을 검출하기 위한 검출기의 최적화가 이루어지지 않았다고 판단되며, 실제 원예작물을 대상으로 fluazinam의 분석조건 확 립 및 회수율 등이 검토된 결과는 전무한 실정이다
최근 우리나라는 다양한 국가와 FTA 협상타결로 국경 없는 경쟁 체제에 돌입하였으며, 이와 같은 국제 여건에 능동적으로 대응하고 우리 농산물의 수출 촉진 및 안전성이 확보된 외국 농산물의 수입을 위해서는 잔류농약의 안전성 평가가 핵심적 요 구사항이 되었다
그러나 각 나라마다 재배환경의 차이로 동일 작물이라 할지라도 발생되는 병해충과 방제에 사용되는 농약의 종류가 상이하 고, 또한 국민의 식습관도 다르기 때문에 잔류허용 기준과 규제 성분에서도 큰 차이가 있으며, 각 나라마다 자국 농업보호와 안 정성 확보를 위하여 수입 농산물에 대한 검역을 강화하고 이를 기술장벽으로 활용, 농산물 수입을 제한하는 수단으로 활용하 고 있으므로 농약사용이 극히 제한될 수 밖에 없고, 아울러 정밀한 공정 잔류농약 분석법의 개발을 통해 수출입 농산물의 안전 성을 확보하여야 할 것이다.
따라서, 본 연구는 현행 국내 식품공전 상에 수록된 광범위 살균제 fluazinam의 분석법을 개선하여 정확성 및 정밀성이 확보 된 효율적인 분석방법을 개발함으로써 국내 및 수출입 원예작물의 일상적 잔류농약 검사에 활용 가능한 공정 분석법을 확립하 고자 하였다.
재료 및 방법
시험 재료
국내 식품 농약잔류허용기준(Ministry of Food and Drug Safety, 2014) 중 fluazinam의 사용이 등록되어 있는 원예작물 중 에서 Codex Alimentarius Commission(Codex)의 잔류분석법 대상 대표 농산물군(Codex, 2003), 국내 소비량 및 해외수출을 진행하고 있는 원예작물을 고려하여 채소류에서는 ‘청양고추’(Capsicum annuum L. cv. Chungyang, 수확일 : 7월 30일)와 결 구배추인 ‘CR-불암플러스’(Brassica rapa ssp. Pekinesis cv. CR-Bulamplus, 수확일 : 10월 25일)를, 과일류에서는 사과 ‘후 지’(Malus domestica Borkh cv. Fuji, 수확일 : 10월 25일)와 감귤 ‘흥진조생’(Citrus unshiu Marcow cv. Okitsuwase, 수확일 : 12월 18일)을 시료로 선정하였다. ‘청양고추’와 ‘CR-불암플러스’ 배추는 대구광역시 북구에 소재한 경북대학교 유리온실에서 포트에 종자를 파종하여 관행재배법에 준하여 재배하였고, ‘후지’ 사과도 경북대학교 사과시험포장에서 관행재배법에 따라 재 배한 과실의 사용하였다. 그리고 ‘흥진조생’ 감귤은 제주특별자치도 서귀포시 남원읍에 소재한 감귤연구소 포장 하우스에 재 식된 나무에서 관행재배법에 준하여 재배한 과실을 사용하였으며, 본 시험에 사용된 작물들은 무농약으로 재배하였다. 이들 시 료 분석을 위하여 ‘청양고추’, ‘후지’ 사과 및 ‘흥진조생’ 감귤은 과경을 제외한 과피와 과육 전체를, ‘CR-불암플러스’ 배추는 뿌 리와 가장 외엽을 제거한 전체를 시료로 사용하였다. 시료 분석은 국내 식품공전 상 검체의 처리방법(Ministry of Food and Drug Safety, 2014)에 따라 세절 및 전처리하여 사용하였다. 4종의 원예작물 시료는 잔류농약 검사를 실시하여 무농약 시료임 을 확인하고 대조구로 사용하였다.
시약 및 기구
본 연구에 사용한 fluazinam은 순도 98.5% 이상의 분석용 표준품을 Sigma-aldrich(St. Louis, MO, USA)로부터 구입하여 n-hexane에 녹여 1,000mgㆍL-1의 농도로 조제하고 -20°C의 냉동고에서 보관하면서 필요 시 마다 n-hexane으로 희석하여 사 용하였고, 분석 정량한계(LOQ), 정량한계의 10, 50, 및 100배에 해당하는 농도로 희석한 후 4종의 대표시료에 처리하여 분석 시료로 사용하였다. Florisil(60-100mesh)은 J. T. Baker(Phillipsburg, NJ, USA)로 부터 구입하여 130°C에서 하룻밤 이상 가 열, 활성화하여 사용하였다. n-Hexane, dichloromethane, acetone 및 ethyl acetate는 잔류분석용을, deionized water는 HPLC 용을 J. T. Baker에서 구입하여 사용하였다. 기타 유기용매 및 무기시약은 시약특급 또는 잔류분석용을 사용하였다. 농축기는 NE-1000SW(Eyela Co., Tokyo, Japan)를 사용하였고, 시료의 마쇄 및 균질화는 고속 균질기인 Ultra-Turrax T-25(IKA Co., Wilmington, NC, USA)를 이용하였다.
GC-ECD/MS 기기분석 조건
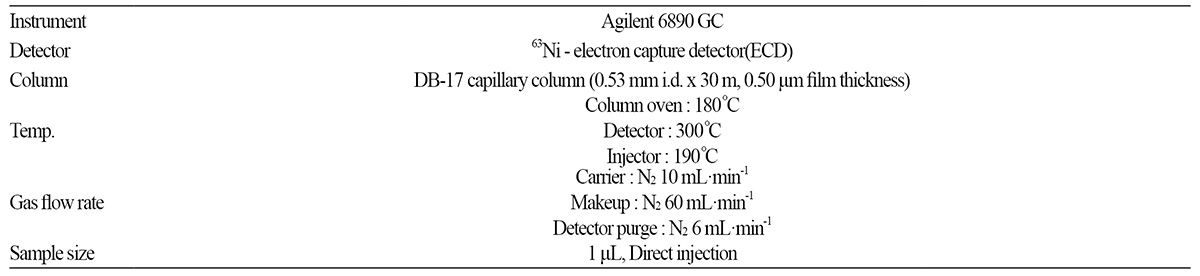
Fluazinam은 분자구조 내에 chlorine 2개, fluorine 6개 및 nitro기 4개를 함유하고 있어 GC-ECD 혹은 NPD 분석이 모두 가 능하다. 이들 검출기 중 분자구조 내에 함유된 다량의 할로겐 화합물에 의해 고감도 분석이 가능한 ECD를 fluazinam의 분석 검출기로 선정하였다. ECD를 장착한 Agilent(Wilmington, DE, USA) 6890 GC에서 분리용 column은 내경이 0.53mm인 capillary column을 사용하여 180°C의 등온조건에서 분석하였다. 재확인을 위한 GC/MS 분석에는 Agilent 7890/7000 GC/ MSD Triple Quad를 사용하였으며, 각각의 자세한 분석조건을 표시하였다(Table 1 and 2).
표준검량선 및 분석정량한계(Limit of quantitation, LOQ)
Fluazinam의 stock solution을 희석하여 0.001-1.0mgㆍL-1의 농도가 되도록 농도별 표준용액을 조제하고, 각 1μL를 GCECD에 주입하여 분석된 peak의 면적을 기준으로 표준검량선을 작성하였다. 또한, 분석기기의 재현성(reproducibility)을 검증 하기 위해 0.50mgㆍL-1의 fluazinam 표준용액을 GC-ECD에 15번 연속 주입, 크로마토그램 상의 retention time(Rt.) 및 peak area의 변이를 비교 평가하였다. 분석법의 정량한계는 무농약 농산물 시료에서 간섭물질이 존재하지 않음을 확인한 후, 분석기 기의 정량한계와 시료량 그리고 분석과정 중의 농축배율을 계산하여 아래의 계산식에 의해 산출하였으며 동일 수준으로 fluazinam을 처리한 회수율 시험으로 재확인하였다(Ahn et al., 2015).
LOQ(mgㆍkg-1) = [기기 정량한계(ng)/주입량(μL)]×[시료용액(mL)/시료량(g)]
시료의 추출 및 분배
세절 또는 분쇄한 시료 25g에 acetone 100mL를 가하고 균질기상에서 2분간 고속마쇄(12,000rpm) 추출하였다. 추출물을 여 과지(Toyo No. 6, Japan)가 장착된 Buchner funnel 상에서 흡인 여과하고 잔류물의 시료 및 호모게나이저 컵을 여분의 acetone 50mL로 씻어 앞서의 여과액과 합하였다. 합친 추출액을 1L 용량의 분액여두에 옮기고 포화식염수 50mL와 증류수 450mL를 첨가한 뒤 n-hexane 100mL로 분배 추출하였다. 분배 후 n-hexane 추출액만을 취해 sodium sulfate 15g에 통과시켜 탈수한 뒤 40°C에서 감압 농축, 건고하였으며, 잔류물은 n-hexane/dichloromethane 혼합용액(95/5, v/v) 10mL에 재용해하였다.
Florisil 흡착 크로마토그래피
내경 1.5cm, 길이 40cm의 유리칼럼에 활성화시킨 florisil 10g을 건식 충전한 후, 3g의 무수 sodium sulfate를 그 위에 첨가하 였다. 칼럼에 n-hexane/dichloromethane 혼합용액(95/5, v/v) 50mL를 가하여 상단에 소량의 n-hexane/dichloromethane 혼 합용액(95/5, v/v)이 남을 정도로 유출시켜 버린 후 n-hexane/dichloromethane 혼합용액(95/5, v/v) 10mL에 녹인 시료 용액 을 가하여 약 3mL/min의 유속으로 유출시켰다. 충전제 표면이 노출되기 직전 n-hexane/dichloromethane 혼합용액(85/15, v/v) 100mL를 용출시 켜 버린 후 재차 n-hexane/ethyl acetate 혼합용액(65/35, v/v) 150 mL를 용출시켜 받았다. Fluazinam 이 용출된 분획은 40°C에서 감압 농축, 건고하고 잔류물을 n-hexane 10mL에 재용해하여 GC-ECD로 분석하였다.
대표 원예작물에 대한 fluazinam의 회수율 시험
본 연구에서 확립한 살균제 fluazinam 잔류분석법의 효율 및 신뢰성을 검증하기 위해 실제 대표 원예작물의 시료에 대한 회 수율 시험을 수행하였다. 즉, 마쇄한 각 대표 무농약 시료 25g에 LOQ, LOQ의 10, 50, 및 100배에 해당하는 fluazinam 표준용 액을 각각 3반복으로 처리한 다음 상기 분석과정을 수행하여 회수율과 분석오차를 측정하였다.
결과 및 고찰
GC-ECD 분석조건의 확립
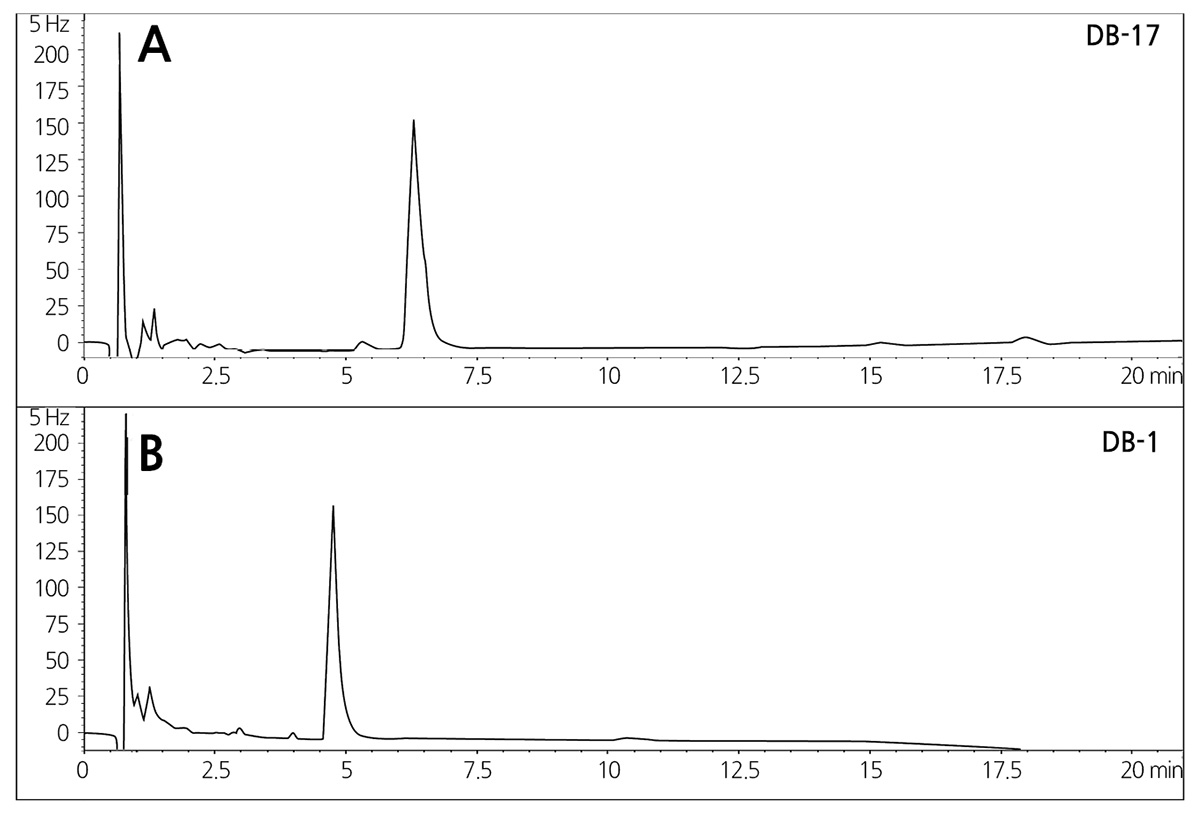
GC-ECD를 이용하여 fluazinam 분석의 최적 column을 선정하기 위하여 column의 극성별로 분리양상을 조사하였다. Phenylsiloxane/methylsiloxane 함량별로 극성을 달리하여 분리능을 조사한 결과, methylsiloxane 함유량이 100%인 DB-1 비극성 capillary column 보다 phenylsiloxane이 50% 함유된 비교적 극성인 DB-17 capillary column에서 fluazinam의 감도 및 분리능이 우수하였고, DB-1 칼럼에 비해 머무름 시간이 다소 지연되는 특성이 있으므로 시료로부터 함께 추출되는 비극성 불순물에 의한 간섭이 상대적으로 적을 것으로 판단되어 fluazinam을 분석하기 위한 최적 칼럼은 DB-17으로 선정하였다(Fig. 2). Fluazinam의 머무름 시간은 180°C 등온조건에서 약 6.2분이었으며, 분리능과 감도를 증대시키기 위하여 온도구배법을 사 용할 수도 있으나, 이 경우 재현성이 등온조건에 비하여 열등한 단점이 있으므로, 본 분석법의 개발 목적이 시료 주입 후 단시 간 내에 분석 작업이 수행될 수 있는 일상적 공정 잔류분석에 적용 가능한 분석법의 확립이므로 분석결과의 재현성 및 안정성 측면에서 보다 유리한 등온조건을 선정하였다.
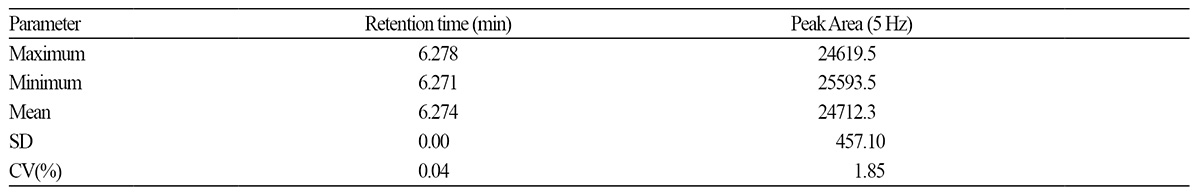
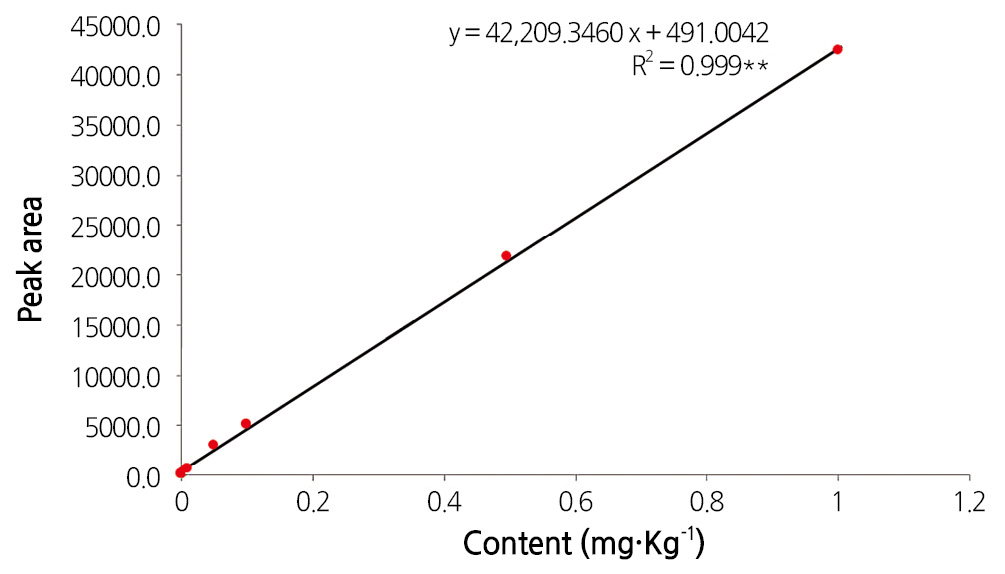
분석기기의 정량한계는 크로마토그램에서 peak로써 나타난 대상 성분의 분석 결과를 신뢰성 있게 수치화할 수 있는 한계농 도로써, 크로마토그램 상에서 검출된 peak의 S/N(signal/ noise)의 비가 최소 10 이상을 나타내는 성분의 농도를 의미한다(Fong et al., 1999; Miller, 2005). Table 1의 GC-ECD 조건에서 fluazinam 표준용액을 분석하여 S/N비를 계산한 결과 기기상의 정량 한계 (S/N ≥ 10)는 0.01ng 수준이었다. 한편, 기기분석의 안정성 평가를 위해 0.5mgㆍL-1농도의 표준품을 15번 반복 주입 분석 하여 피크의 유지시간 및 peak 면적의 변이계수(CV, %)를 조사하여 재현성 평가를 실시한 결과 두 크로마토그래피 척도 모두에서 최대 1.85% 미만의 오차를 나타내어 기기 분석 시 안정적이고 재현성 있는 분석을 수행할 수 있음을 확인하였다(Table 3). Fluazinam의 농도별 표준용액(0.001-1mgㆍL-1) 1μL를 GC-ECD에 주입, 분석하여 얻은 검량선의 방정식은 y = 42,209.3460x + 491.0042(R2 = 0.999**)로 우수한 직선 패턴을 나타내었다(Fig. 3). 즉, fluazinam은 기기 정량한계의 1/10 수 준인 0.001ng에서부터 그 1,000배인 1ng까지의 표준검량선에 대한 회귀계수가 R2 = 0.999** 이상으로 정량의 직선성이 검정 되었으므로 매우 광범위한 농도 범위의 시료 중 잔류량을 비례적으로 산출하는 것이 가능하였다.
| |
Fig. 2. GC-ECD chromatograms of fluazinam using typical capillary columns (1 μL of 0.1 mgㆍL-1 in n-hexane): DB-17 capillary column (A) and DB-1 capillary column (B). | |
시료 추출 및 분배과정의 확립
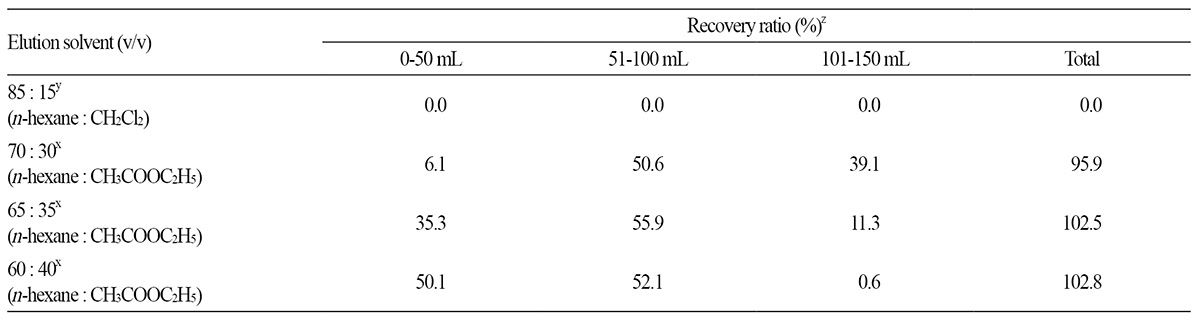
대표적 원예작물 시료로부터 fluazinam 성분을 추출하기 위한 용매로는 acetone을 사용하였다. Acetone은 US FDA법이나 AOAC법에서 대상 성분과 유사한 물리화학적 특성을 나타내는 농약 잔류분을 추출하는데 보편적으로 사용되는 표준적 용매 로써 이미 많은 연구자들에 의하여 농약 추출에 그 효율과 재현성이 인정된 바 있다(Lee et al., 2010; Lee et al., 2011). 시료 추 출액으로부터 대상 농약 성분과 함께 추출되는 방해물질을 1차적으로 제거하기 위한 조정제법으로는 액-액 분배법을 사용하 였다. 즉, 수용성 유기용매 추출액을 다량의 포화식염수/증류수로 희석한 후 직접 비극성 용매로 분배 추출하는 방법을 사용하 였는데, 이는 US FDA법이나 AOAC법에서 중간-비극성 농약 성분에 대하여 보편적으로 사용되며(AOAC, 2000; Lee et al., 2008), 번거로운 추출액의 농축과정을 생략할 수 있는 장점이 있다. 분배용매로 n-hexane, n-hexane/dichloromethane 혼합 액, dichloromethane 등 4종을 공시, 대상 성분의 분배효율을 조사하였다(Table 4). 대상 성분의 액-액 분배조건에 따른 분배효 율을 조사한 결과 n-hexane 용액 100mL로 분획하였을 때 fluazinam의 회수율은 94.6% 수준이었으며, n-hexane/ dichloromethane 혼합액(80/20, v/v) 100mL로 분획하였을 때 회수율은 92.9% 수준, n-hexane/dichloromethane 혼합액 (20/80, v/v) 100mL로 분획하였을 때는 89.0%, dichloromethane 50mL로 2회 반복한 분획은 88.6%를 나타내어 회수율 및 작 업의 편이성 등을 고려할 때 가장 우수한 분배용매Ⅰ의 액-액 분배조건을flu azinam의 분배용매로 선정하였다.
Florisil 흡착 크로마토그래피 정제조건의 최적화
대표 원예작물에 함유된 fluazinam의 분석 시 상기 액-액 분배과정을 통해 상당량의 불순물 및 비극성 간섭물질들이 제거되 었을 것으로 판단되나, 시료에 따라 원 시료로부터 유래되는 다양한 기타 불순물이 존재하므로, 기기분석에 앞서 추가적인 정 제과정이 필요할 것으로 판단되어 흡착크로마토그래피에 의한 정제법을 검토하였다. 흡착크로마토그래피는 잔류농약 분석 시 가장 많이 이용하는 방법이며, 흡착제로는 silica gel, florisil 및 alumina 등이 많이 사용되고 있는데, 이 중 florisil 은 색소와 유지의 제거가 뛰어나 미국의 FDA(1999)나 AOAC(2000) 등에서 보편적으로 사용하는 방법이다. 본 연구에서도 fluazinam의 극성을 고려하여 florisil을 흡착제로 선정 하였으며, 용매의 극성 조절을 위해 n-hexane/dichloromethane 및 n-hexane/ethyl acetate의 혼합 용매체계를 사용하여 최적화하고자 하였다(Table 5).
Florisil 흡착크로마토그래피용 용매의 다양한 극성 조절을 이용하여 fluazinam의 회수율을 조사한 결과, n-hexane/ dichloromethane 혼합액(85/15, v/v) 100mL로 pre-washing한 후, n-hexane/ethyl acetate 혼합액(65/35, v/v) 150mL로 용출 할 경우 fluazinam 성분의 회수율이 102.5%였으며, ethyl acetate의 비율을 높여 용출용매의 강도를 높여도 회수율의 개선 정 도가 미미하였다. 따라서 florisil 흡착크로마토그래피법을 이용하여 간섭물질의 제거를 위한 추가적인 정제법은 검토된 용매 체계 중 가장 우수한 회수율 나타낸 상기의 방법을 적용하였다 .
대표 원예작물에 대한 fluazinam의 분석 정량한계 및 회수율
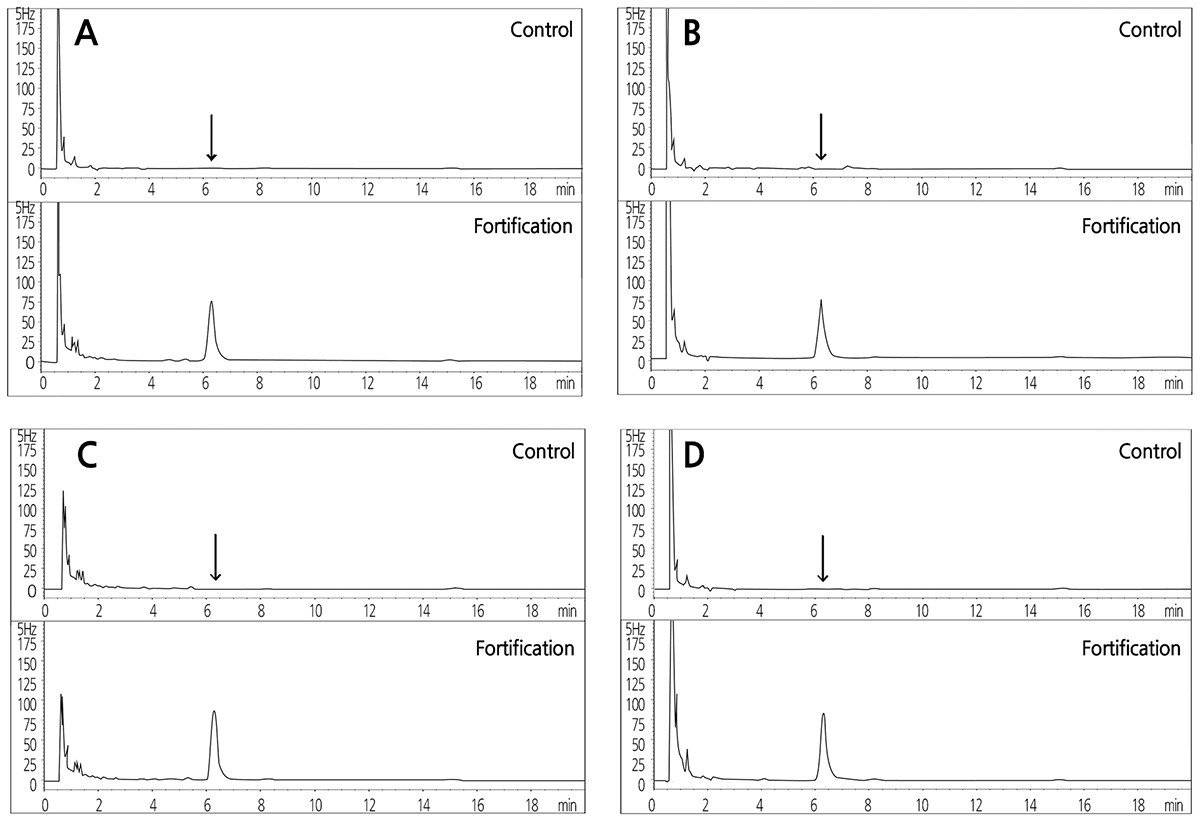
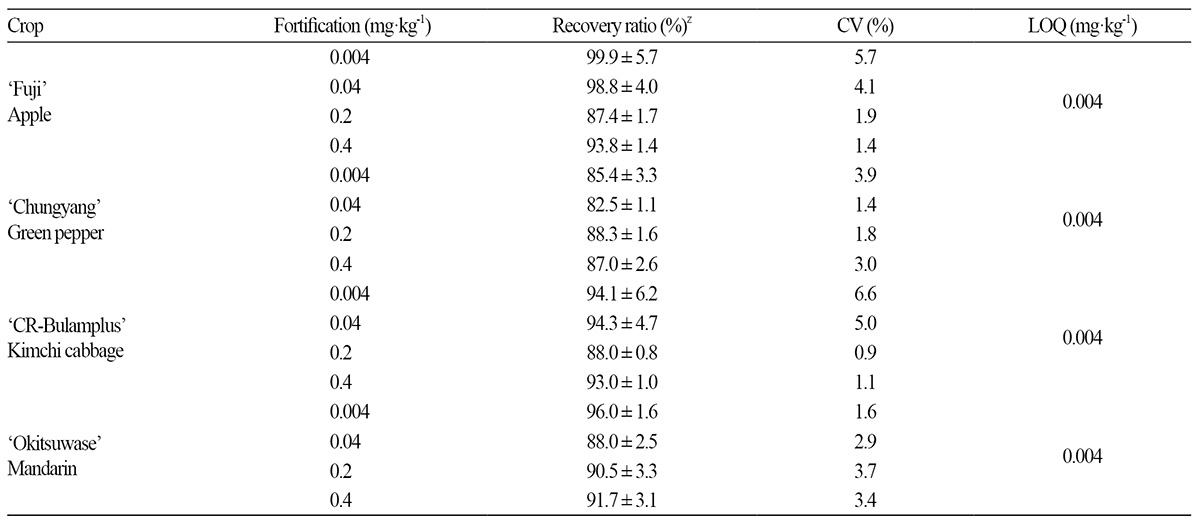
본 연구에서 확립한 시료 추출 및 정제, 그리고 기기분석 과정을 각 대표적 무농약 원예작물 시료에 적용한 결과는 Fig. 4와 같다. 무농약 작물의 최종 시료용액에서 대상농약과 동일한 머무름 시간에 간섭물질이 존재하지 않음을 확인하였고, 분석기기 의 정량한계(LOQ)와 시료량, 그리고 분석과정 중의 농축배율을 계산하여 분석법의 정량한계를 산출하였다. 본 연구에서 무농약 시료에서 간섭물질이 존재하지 않음을 확인한 후 산출된 fluazinam의 정량한계는 0.004mgㆍkg-1이었으며, 국제기준인 Codex(2003) 및 식품공전 잔류농약분석법 실무 해설서(Lee, 2012)에서 권장하는 잔류농약분석법 기준인 0.05mgㆍkg-1 이하 또는 허용기준의 1/2 이하의 정량한계 기준에 적합하였다. 각각의 무농약 시료에 fluazinam 표준용액을 LOQ, LOQ의 10배, 50배 및 100배의 농도가 되도록 첨가하고, 상기 확립된 분석방법에 의하여 대표 원예작물에 4수준 3반복으로 분석하여 회수 율을 조사한 결과, LOQ 수준에서는 85.4-99.9%, LOQ 10배 수준에서는 82.5-98.8%, LOQ 50배 수준 및 LOQ 100배 수준에 서는 각각 87.4-90.5%, 87.0-93.8%의 양호한 회수율을 나타내었으며, 재현성도 양호하여 분석오차는 최대 6.6%로 조사되었 다. 따라서, 처리수준 및 시료 종류에 관계없이 잔류분석기준인 회수율 70-120% 범위와 분석오차 10% 이내를 만족하였다 (Table 6). 이상의 결과에서 볼 때, 본 연구에서 확립된 살균제 fluazinam의 분석법은 국내ㆍ외 원예작물의 잔류농약 분석 및 검 사에 충분히 적용 가능함을 확인하였다
Table 6. Recovery ratio of fluazinam in different crop samples.
| |
zMean values of triplicate samples with standard deviations. | |
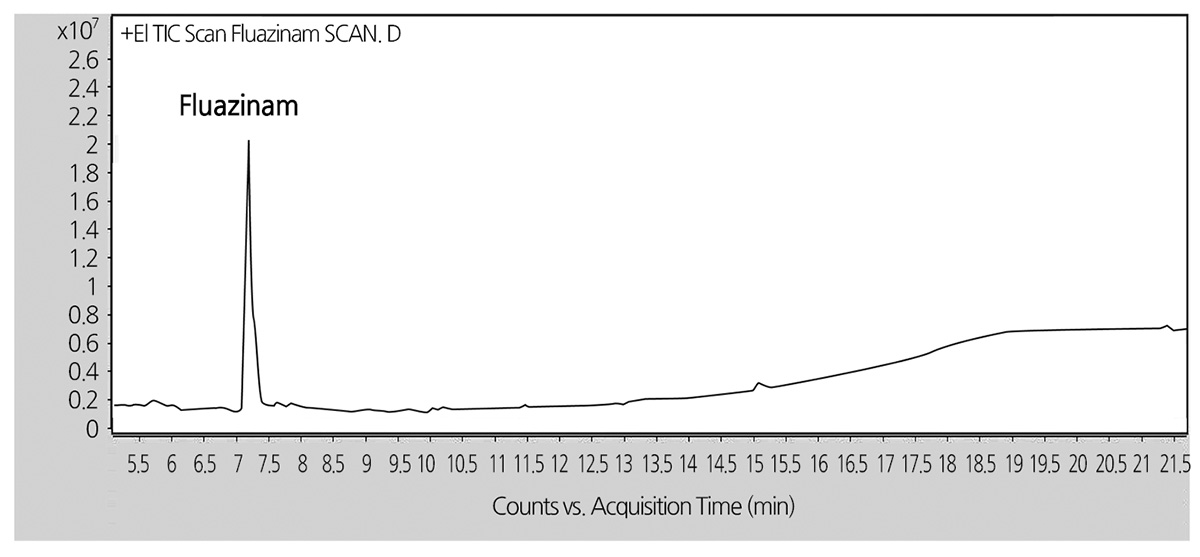
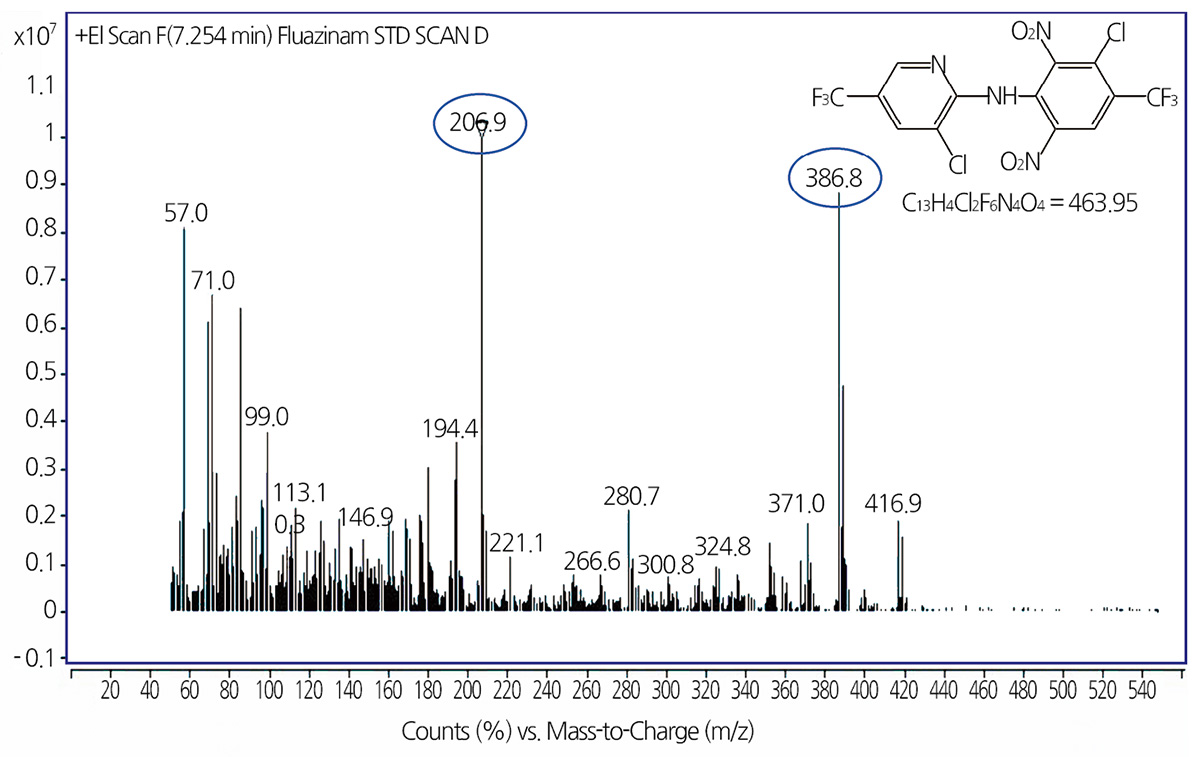
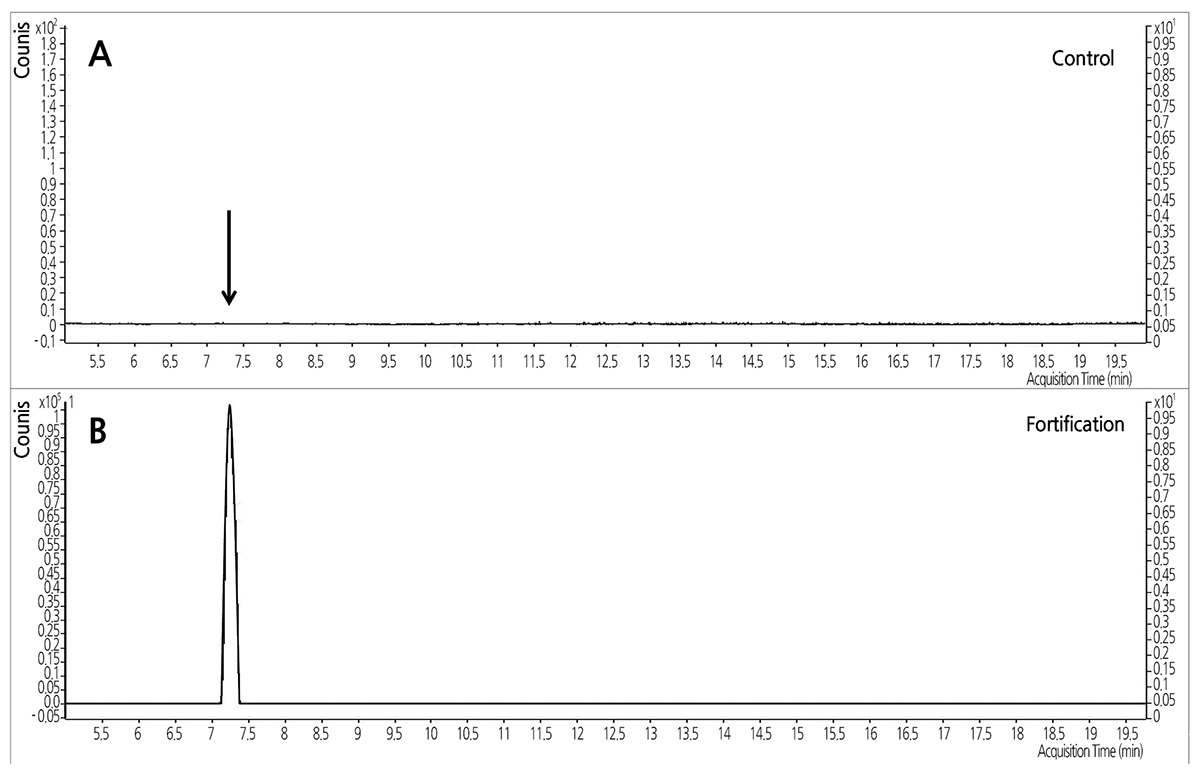
GC/MS를 이용한 잔류분의 재확인
개발된 분석법의 신뢰성을 확보하기 위해 GC/MS에 의한 재확인 과정을 추가하였다. Table 2의 GC-MS 분석조건에서 표준용액을 분석하여 TIC(total-ion chromatogram) 및 MS spectrum을 얻었으며, m/z 206.9와 386.8을 selected-ion monitoring(SIM)용 ion으로 설정하였다(Fig. 5 and 6). Fig. 7은 본 실험에 사용된 대표적 원예작물 시료 중 고추를 대상으로 살 균제 fluazinam의 잔류분을 재확인한 selected-ion monitoring(SIM) chromatogram이며, 본 실험에서 사용된 모든 무농약 시 료에서는 대상 농약성분의 peak가 전혀 관찰되지 않았고, 인위 첨가된 시료에서는 동일한 머무름 시간대에 정확하게 fluazinam의 잔류분만을 확인할 수 있었다. 따라서 본 연구에서 사용한 GC/MS의 SIM 조건을 이용할 경우에도 GC-ECD를 이용한 정 량법과 더불어 살균제 fluazinam 잔류분의 추가적 정성분석법으로 사용할 수 있을 것으로 판단된다.