서 언
재료 및 방법
선발 미생물의 chitinase, cellulose 및 siderophore 활성 검정
선발 길항미생물의 배양 조건
결과 및 고찰
선발 미생물의 한국잔디 갈색퍼짐병 길항작용
선발 길항미생물의 배양 특성
배지 종류
배양 온도
3) 배지의 pH
배양시간
탄소원의 영향
질소원의 영향
무기화합물의 영향
서 언
현재 잔디에는 약 60여종의 진균병이 발생하고 있으며 이에 관여하는 병원균은 90여종 이상으로 이중 다핵성인 Rhizoctonia spp.에 의한 병해가 가장 심각한 것으로 알려져 있다(Couch, 1985). 이 병원균은 한국잔디 등 난지형 잔디의 엽신, 엽초, 관부에 침입하여 마름증상을 보이다가 회백색의 병징으로 변한 뒤 잎집이 쉽게 뽑히는 갈색퍼짐병을 유발한다(Tredway and Burpee, 2001). 특히 이 병은 한국잔디에서 연속적으로 발생하고, 발생력과 부생능력이 크며 생존이 불리한 조건에서 내구체인 균핵을 형성하므로 방제가 어렵고 많은 양의 농약을 계속적으로 투여하게 된다(Shim and Kim, 2000).
지속적인 고품질 잔디의 유지, 생태계 보존 및 관리비용의 절감과 사용자 안전성 극대화를 위해서는 농약과 비료를 최소한으로 관리 사용하여 방제하는 기술의 개발이 중요하다. 미생물을 이용한 생물학적 방제는 자연생태계 내에서 서로 다른 종간에 일어날 수 있는 경쟁(competition), 기생(mycoparasitism), 용균(lysis), 항생(antibiosis)작용 등의 상호작용을 인위적으로 조절하여 이용하는 방법이다(Chet, 1990; Hoy and Herzog, 1985). 이러한 길항미생물을 이용한 잔디병의 생물적 방제는 1980년대부터 fairy rings(Smith, 1980), brown patch(Burpee and Goulty, 1984; Giesler and Yuen, 1998), snow mold(Lawton and Burpee, 1990), dollar spot (Goodman and Burpee, 1991; Nelson and Craft, 1991), 그리고 gray leaf spot(blast)(Viji et al., 2003) 등에 적용되어져 왔다.
본 연구실에서는 한국잔디 갈색퍼짐병원균의 균사 생육을 억제하는 작용을 가진 3 종의 세균(2종 Bacillus속과 1 종의 Pseudomonas 속)을 분리하여 기내 및 생물검정을 실시하여 그 중 효과가 제일 탁월한 CNU- BA-2 (FRIN-001-1) 균주를 특허 출원하였다(국내 특허번호 10-1323177). 이 세균은 갈색퍼짐병 병원균 R. solani AG2-2(IV)의 균체 생장을 기내조건에서는 63%, 한국잔디 화분 생육조건에서는 43%까지 억제하는 효과를 보인 바 있다(Ma et al., 2013). 이러한 분리 균주를 활용한 미생물 제제의 제조와 처리 환경에 따른 효과의 변이를 보이는 단점을 보완하고 장점을 극대화하기 위해서는 길항기작, 처리방법, 길항효과, 지속성 방안 등 유효 미생물을 활용할 수 있는 적극적인 기술 개발이 필요할 것으로 판단된다. 또한 미생물 제제의 대량생산을 위한 최적 배양조건에 관한 연구가 필수적이라 할 수 있다.
따라서 본 연구는 앞서서 보고한 선발 길항 미생물의 생리 및 생화학적 길항 기작을 구명하고 이들 분리 미생물들의 대량 증식에 필요한 여러 배양 요인을 조사하여 생물학적 방제를 위한 선발 길항 세균의 대량생산 조건을 알아보기 위하여 수행되었다.
재료 및 방법
선발 미생물의 chitinase, cellulose 및 siderophore 활성 검정
길항미생물의 chitinase 생산과 활성을 확인하고자 0.02% 쇠고기추출물, 0.01% NaCl, 0.02% peptone, 0.01% 이스트추출물이 첨가된 배지에 1%(v/v) colloidal chitin을 첨가한 고체 배지를 사용하였다(Hsu and Lockwood, 1975). Chitin (Sigma, USA) 40 g에 진한 염산 40mL를 가하여 50°C에서 교반시킨 다음 4°C의 증류수 1 L를 첨가한 후 침전물을 pH 5가 될 때까지 증류수로 여러 번 세척하여 사용하였다. 분리 선발한 길항미생물을 colloidal chitin 평판배지에 접종한 후 32°C로 48시간 배양시킨 후 균체 주위에 생성된 투명 환의 유무로서 chitinase 생산능력을 확인하였다.
Cellulase의 활성은 검정용 DCAB(detecting cellulolytic activity of bacteria) 배지(0.1% NaNO3, 0.1% K2HPO4, 0.05% KCl, 0.05% MgSO4・7H2O, 0.005% 효모추출물, 0.5% carboxylmethyl cellulose, 1.1% agar)에 선발 길항 균주를 접종하여 실시하였다. 접종 후 32°C에서 48시간 배양시킨 후 Congo red 0.1%를 배양 배지가 잠길 정도로 처리하고 30분간 정치 후 congo red를 제거한 뒤 1 M NaCl을 15분간 처리하면서 colony 주위에 황색의 환(halo)의 형성 유무로 확인하였다(Bhat and Maheshwari, 1987).
항진균성 siderophore 생성 여부를 조사하기 위하여 sidero-phore 생산 균주의 분리배지인 CAS(chrome azurol S) blue agar 배지를 제조하여 사용하였다(Lee et al., 1999; Shivanna et al., 1994). 갈색퍼짐병원균 R. solani AG2-2(IV)에 대해 길항능력을 나타냈던 선발 균주 3종을 접종하여 32°C에서 48시간 배양시키면서 오렌지 색의 둥근 환의 생성 유무를 관찰하면서 siderophore 생성 여부를 확인하였다.
선발 길항미생물의 배양 조건
선발 길항미생물의 대량 생산을 위해서는 최적 배양조건을 확립할 필요가 있다. 이를 위해서 배지의 종류, 배양 온도, pH, 배양시간, 탄소원, 질소원, 무기화합물 등의 영향을 조사하였다. 각각의 실험조건에서 길항미생물의 생장속도는 분광광도계를 이용하여 600nm에서 균탁도를 측정하였다.
선발 길항미생물 생육 최적배지를 알아보기 위해서 LBB (Luria Bertani broth), TSB(tryptic soy broth), PDB(potato dextrose broth), NB(nutrient broth), NYB(nutrient yeast extract broth) 5가지 배지를 사용하였다(Table 1). 5종의 배지를 10mL씩 시험관에 분주하고 고압 멸균한 뒤, 길항 미생물이 포함된 배양액을 1%(v/v)씩 접종하였다. 접종 후 32°C에서 190rpm으로 24시간 진탕 배양한 후 균탁도를 측정하였다.
생육 최적온도를 조사하기 위해 길항 미생물 배양액을 배지의 생육이 제일 양호했던 최적 배지에 1%(v/v)씩 접종한 뒤 10, 20, 30, 35, 40, 50, 그리고 60°C 온도조건에서 190rpm으로 24시간 진탕 배양 후 같은 방법으로 균탁도를 측정하였다.
선발 길항미생물의 생육에 필요한 최적의 pH를 알아보기 위해 생육이 가장 좋았던 LBB를 기본배지로 하고 HCl과 NaOH를 이용하여 pH 3.0에서 10.0으로 조절하고 동일한 방법으로 전 배양액 1%(v/v)를 접종하였다. 그 후 32°C에서 190rpm으로 24시간 진탕 배양 후 균탁도를 측정하였다.
배양 시간에 따른 길항 미생물의 생육차이를 확인하고자 전 배양액을 생육이 가장 좋았던 LBB 배지에 1%(v/v)로 접종하고, 32°C에서 190rpm에서 96시간 진탕 배양하면서 4시간 간격으로 배양액을 회수하여 위와 같은 방법으로 균탁도를 측정하였다.
M9 기본배지(0.0015% CaCl2, 0.6% Na2HPO4, 0.3% KH2PO4, 0.05% NaCl, 0.1% NH4Cl, 0.05% MgSO4, 0.2% Glucose)에 mannitol, lactose, fructose, galactose, sorbitol, sucrose등 총 6종의 탄소원을 1%씩 첨가하고, 길항미생물이 포함된 배양액을 접종한 후 32°C에서 24시간, 190rpm으로 진탕 배양한 후 배양액의 균탁도를 조사하였다. 비슷한 방법으로 질소원의 영향은 최적의 탄소원이 1% 첨가된 M9 기본 배지에 NH4Cl을 제외한 배지를 제조하여 쇠고기추출물, 맥아추출물, 펩톤, 효모추출물, 트립톤, 요소, 염화암모늄 등을 각 0.5%(w/v)씩 첨가한 후, 앞의 방법과 동일한 조건에서 진탕 배양하고 배양액의 균탁도를 조사하였다.
최적의 탄소원과 질소원이 각 1%(w/v)와 0.5%(w/v) 첨가된 M9 기본 배지에 K2HPO4, NaH2PO4, CaCO3, KCl등 4종의 무기화합물을 각 0.1%(w/v)씩 첨가하여 동일한 조건에서 진탕 배양한 다음 배양액의 균탁도를 조사하였다.
결과 및 고찰
선발 미생물의 한국잔디 갈색퍼짐병 길항작용
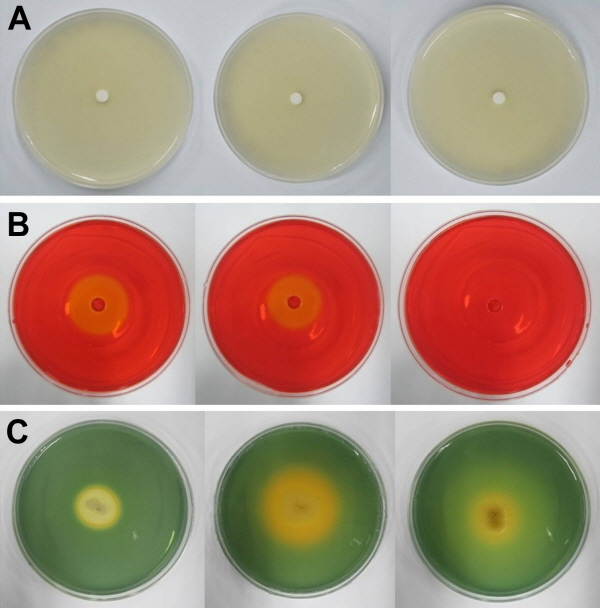
선발 길항미생물 I-009, FRIN-001-1 및 YPIN-022의 chitinase 활성을 확인한 결과 세 균주 모두 clear zone을 형성하지 않아 chitinase분비능이 없는 것을 확인하였다(Fig. 2A). Chitin은 진균류의 세포벽 구성성분이고, 이를 기질로 chinase 효소는 진균류에서는 세포벽 형성 및 균류 외형의 발달을 위해 존재하지만, chitin을 가지고 있지 않은 식물 또는 토양 세균 역시 chitin 분해물을 먹이로 활용하거나 방어기작의 하나로 chitinase를 분비한다(Robert and Selitrennikoff, 1988). 그러나 상업적으로 이용 가능한 chitin 분해효소는 대부분 미생물로부터 얻을 수 있는데 미생물 기원의 chitinase생산 균주로는 Streptomyces, Serratia, Aeromonas, Bacillus, Enterobactor, Trichoderma등이 있지만, chitin 분해효소 생산에 적합한 미생물로는 곰팡이보다는 통기 및 교반이 용이한 세균이 유리한 것으로 알려졌다(Kang et al., 1998).
|
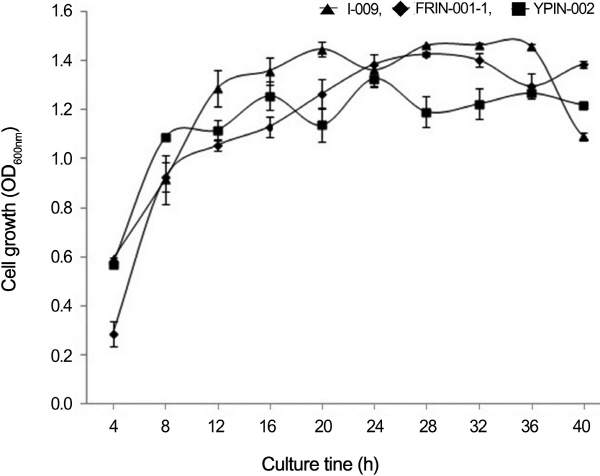
Fig. 2. Effect of culture time on the growth of three bacterial strains antagonistic against the large patch pathogen Rhizoctonia. Error bars indicated standard deviation of three replications. |
Chitinase 유전자를 형질전환시킨 담배에서 뿌리에 발생하는 Rhizoctonia solani 병원균에 내성을 보이고, 토마토에서도 Class I형의 유전자가 Fusarium 병원균에 부분 내성을 보인다는 결과가 보고되었다(Broglie et al., 1991; Melchers et al., 1993). 기대와는 달리 갈색퍼짐 병원균에 대한 선발 토양 세균들의 chinase를 통한 길항작용은 나타나지 않았다. 이는 항균작용을 보이는 chitinase 생성 유전자의 차이 또는 기질(예, β-1,3-glucan) 특이 효소작용의 차이로 선발 세균들의 항균활성이 다르게 나타난 것으로 추정된다(Robert and Selitrennikoff, 1988; Sela-Buurlage et al., 1993).
선발 길항미생물의 cellulase의 생산능 판단을 위해 Detecting Cellulolytic Activity of Bacteria(DCAB)배지를 이용한 Congo red test를 실시하게 되면 cellulase를 세포 밖으로 분비하는 미생물이 접종되면 주위의 기질이 변하여 노란색을 보이게 된다. 배지에 carboxylmethyl cellulose 기질을 포함하여 선발균을 접종한 결과 I-009와 FRIN-001-1에서는 cellulose 분비능력이 있음을 확인하였으나, YPIN-002균주는 cellulase를 분비하지 않았다(Fig. 2B).진균 세포의 세포벽을 이루는 물질인 chitin, β-glucan 및 cellulose등의 다당류는 이들의 합성이 저해될 경우 진균의 생장을 선택적으로 방해할 수 있어 항균 미생물 탐색의 좋은 대상으로 인식되고 있다.
본 연구 결과에서와 같이 Bacillus 속의 선발균은 cellulose 분해효소를 분비하여 갈색퍼짐병원균의 생장을 억제할 수 있을 것으로 보이나, Pseudomonas 속의 선발균은 다른 항균 기작을 보일 것으로 여겨진다. 보고에 의하면 Pseudomonas 속 세균의 경우 토양 병원균의 억제 기작으로 세포벽 구성 성분의 하나인 β-1,3-glucan 분해효소를 분비하는 것으로 알려졌다(Fridlender et al., 1993). 한편 Bacillus 속의 2개 선발균의 항균작용을 극대화하기 위해서는 cellulose 결합을 촉진하는 물질(예, cellulose-binding gene product) 등에 대한 연구가 필요할 것으로 보인다(Limon et al., 2004).
선발된 길항미생물의 siderophore생산능을 Chrome Azurol S(CAS) blue agar 배지에서 조사한 결과, I-009, FRIN-001-1 및 YPIN-022균주 접종부위에 오렌지색의 환이 형성되는 점으로 보아 선발 길항미생물 모두에서 siderophore가 분비됨을 알 수 있었다(Fig. 2C). Siderophore는 철 이온(Fe3+)과 친화성이 높은 가용성이며 저분자(1.0kDa 미만)인 2차 대사산물로 많은 미생물들이 이 물질을 생산한 후 철수송계(high- affinity iron-transport system)를 통해 토양 내 철 이온을 흡수하여 생육에 이용한다(Payne, 1994). 철 이온의 흡수 경쟁에서 우위를 선점하기 위해 경쟁적으로 높은siderophore를 생산하면 병원성 진균의 철 이온 흡수를 방해함으로써 식물병원성 진균을 고사시키는 작용을 하게된다(Compant et al., 2005).
선발 길항미생물의 배양 특성
배지 종류
선발 길항미생물 생육의 최적배지를 조사하기 위해 5종류의 배지를 사용하여 배양한 결과 I-009, FRIN-001-1 및 YPIN-022균주 모두 LBB배지에서 균체의 생장이 가장 높게 나타났다(Table 2). 배지의 종류에 따라 균사의 생장 속도, 미생물의 세포벽 구성물질의 차이는 포함된 기질의 종류, 배지와 세포간의 삼투압 차이 등으로 배양 속도가 다르게 나타나는 것으로 알려졌다(Lopez et al., 1998).
배양 온도
최적 LBB배지에 선발 길항미생물을 접종한 뒤 10-60°C의 온도범위에서 균체의 생육을 확인하였다(Table 3). Bacillus 속인 I-009와 FRIN-001-1균주는 35°C와 30°C에서 각각 균체의 생장이 가장 높았으며, 최적 온도를 벗어나 40°C의 온도 범위까지는 생장이 완만하게 낮아졌고, 반면에 Pseudomonas 속인 YPIN-022균주는 30°C 이하의 비교적 낮은 온도에서도 생육이 양호했고 35°C에서 균체의 생장이 가장 높았다. 그러나 40°C에서 급격히 균체의 생장이 낮아졌다(Table 3). Shim et al.(1994)은 Rhizoctonia solani AG2-2(IV)의 균사생육은 10°C부터 그 생육이 시작되어 점차 증가하여 25-30°C에서 가장 왕성하다고 하였다. FRIN-001-1균주는 30°C범위가 생육 최적온도로 조사되었는데 이는 길항균과 병원균 생육 적온이 비슷하여 병원균이 생장이 활성화될 때 길항균 또한 최적의 상태로 증식할 수 있음을 의미하므로 효과적인 길항균으로 작용할 수 있다고 판단된다. In vitro 및 in vivo 실험 결과에서도 FRIN-001-1균주의 길항 작용이 가장 우수한 것으로 나타난 이유 중의 하나는 병원균과 길항 세균의 생육적온 범위가 유사하기 때문으로 보인다(Ma et al., 2013).
3) 배지의 pH
길항 미생물의 배양에 필요한 배지의 최적 pH를 알아보기 위해 pH 3-10범위에서 배양한 결과 I-009와 FRIN-001-1균주는 pH 5부터 약알칼리인 pH 8까지의 넓은 범위 내에서 생육이 높게 나타났다. 반면에 YPIN-002균주는 약산성인 pH 5부터 알칼리인 pH 9범위까지 생육이 높게 나타났다(Table 4). 선발 길항미생물 3종의 생육 pH 범위를 확인한 결과 이는 우리나라 경작지 대부분이 약산성인 점을 고려할 때 토양 내 pH 환경에 적응 가능하여 병해 예방에 적용이 가능할 것으로 판단된다. 또한 YPIN-002균주는 골프장에서 바다 모래를 이용한 배토관리 시에도 알칼리성 토양 환경에 적응이 가능하여 병원균에 대한 길항력을 유지할 수 있을 것으로 판단된다. 특히, 갈색퍼짐병의 기주인 난지형 들잔디는 주로 골프장의 페어웨이에 식재되어 있고(Choi et al., 2012), 페어웨이의 일반적인 토양 pH 는 7.06로 알려져 있어 선발된 3종의 균주는 골프장에 적용 시 생육이 가능할 것으로 판단된다(Kim et al., 2012).
배양시간
최적의 배양 시간을 조사하기 위해 선발 길항미생물을 40시간 이상 배양하면서 매 4시간 간격으로 균탁도를 측정하여 균체 생장을 조사하였다(Fig. 3). 세 가지 길항 미생물 모두 배양 후 8시간부터 급격히 증가하였으며, I-009균주는 배양 후 32시간부터 최대 균체 생장에 도달하였다. FRIN-001-1균주는 배양 후 28시간 경과 후 최대 균체 생장을 보였고, YPIN-002균주는 배양 후 24시간 경과 후에 균체 생장이 가장 높았다. 일반적으로 항균물질은 균의 생장이 정지기를 지나면서부터 증가하는 것으로 알려져 있다. 따라서 항균 작용은 균이 사멸하기 시작하면서 배양액 내에 단백질 분해효소가 증가되어 나타나는 작용으로 보고되고 있다(Martínez- Cuesta et al. 2002). 이러한 결과로 비추어 볼 때 I-009균주는 32시간, FRIN-001-01균주는 28시간, YPIN-002균주는 24시간 이후에도 높은 길항력을 나타낼 것으로 여겨진다.
탄소원의 영향
선발 길항미생물의 균체 증식에 영향을 주는 탄소원을 조사하기 위해 mannitol, lactose, fructose, galactose, sorbitol, sucrose 등 총 6종의 탄소원을 첨가하여 배양한 결과, I-009균주는 sucrose에서 균체의 생장이 높았고, FRIN-001-1균주는 mannitol에서 높게 나타났다. YPIN-002균주는 전체 탄소원 모두에서 비교적 균체 생육이 높았으며, 그 중에서도 sucrose에서 가장 높게 나타났다(Table 5). 이는 같은 속의 미생물이라 하더라도 미생물의 종류와 생육조건에 따라 배지의 최적 탄소원의 종류가 다양하기 때문으로 보인다(Mulders et al., 1991). 토양에서 식물병원균과 항진균은 이용하는 탄소원의 종류가 서로 다르므로 식물병원균은 이용할 수 없고, 항진균만 이용할 수 있는 탄소원을 선택적으로 토양에 처리하여 항진균만을 증식시키고 병원균의 증식은 억제시킬 수 있어 식물병의 방제에 효과적으로 활용할 수도 있을 것이다(Kim and Lee, 2009; Lounes et al., 1996).
질소원의 영향
앞서 확인된 최적의 탄소원을 첨가(I-009, sucrose; FRIN- 001-1, mannitol; YPIN-022, sucrose)한 배지에 쇠고기추출물, malt extract, peptone, 효모추출물, tryptone, urea, NH4Cl 등 7종의 질소원을 추가로 첨가하여 배양시킨 후 길항미생물 균체의 생육을 확인한 결과 세 균주 모두 효모추출물을 첨가한 배지에서 균체의 생육이 가장 높게 나타났다(Table 6). 항균물질을 생산하는 항진균성 미생물은 무기질소원보다는 효모추출물과 같은 유기질소원이 효과적이라고 알려져 있어 본 연구결과와 동일한 결과를 나타내었다(Chun et al., 2000; Shomura et al., 1983). 효모추출물을 첨가한 배지에서 균체 생육이 높게 나타난 점으로 볼 때 배지 종류별 조사 결과에서 LBB배지가 균체 생육에 가장 효과적이었던 것은 배지 조성분 중 하나인 효모추출물의 영향이 있었던 것으로 판단된다.
무기화합물의 영향
최적의 탄소원과 질소원(0.5% 효모추출물)을 첨가한 배지에 K2HPO4, NaH2PO4, CaCO3, KCl등 4종의 무기화합물을 각 0.1%(w/v)씩 첨가하여 배양 후 균체의 생육을 조사한 결과 I-009균주와 YPIN-022균주는 potassium chloride가 첨가된 배지에서 균체의 생육이 높았고, FRIN-001-1균주는 potassium phosphate dibasic이 첨가된 배지에서 균체의 생육이 높게 나타났다(Table 7).