서 언
재료 및 방법
식물 재배
뿌리혹병균 균주 및 접종원 준비
접종 및 병 발생 조사
결과 및 고찰
국내 시판 양배추 품종들에서 뿌리혹병 발생
다양한 뿌리혹병균에 대한 CR 양배추들의 저항성
CR 양배추 F3 계통의 뿌리혹병 저항성
서 언
양배추(Brassica oleracea ssp. capitata)에는 항산화 및 항암 효능을 나타내는 다양한 생리활성 물질이 함유되어 있다(Fenwick et al., 1983; van Poppel et al., 1999). 그리고 양배추는 우리나라뿐만 아니라 중국과 일본 등에서 널리 재배되는 작물이다. 양배추에 발생하는 주요 병해로는 검은썩음병, 시들음병 및 뿌리혹병 등이 알려져 있는데(KSPP, 2009), 특히 Plasmodiophora brassicae Woron.에 의한 뿌리혹병(clubroot)은 B. rapa, B. napus, B. oleracea 등의 Brassica 채소에 발생하여 작물의 생산량과 질을 저하시켜 경제적으로 심각한 손실을 일으키는 병해이다(Hirai, 2006).
뿌리혹병균(P. brassicae)은 휴면 포자로 토양에 존재하며, 환경이 적합하면 수 년 동안 생존이 가능하여 뿌리혹병이 발생한 재배 포장에서는 병원균이 오랫동안 남아 있다. 이 병원균에 감염된 식물체를 뽑아서 뿌리를 살펴보면 잔뿌리가 없어지고 주근에 혹이 생성되어 수분과 양분의 흡수가 억제되어 생육이 저해되며 한낮의 무더운 시간에는 시들음 증상을 보이다가 밤에는 회복되기를 반복하다 결국 고사하게 된다(Voorrips, 1995).
뿌리혹병을 방제하기 위하여 토양의 pH를 조절하거나 배추과 작물 이외 작물과의 윤작을 하는 등의 경종적 방제와 fluazinam, flusulfamide 및 cyazofamid 등의 살균제를 이용한 화학적 방제 방법이 널리 이용되고 있다(Komyoji et al., 1995; Mitani et al., 2003). 오늘날에는 안전한 농산물에 대한 관심이 높아지면서 길항 미생물을 이용한 생물학적 방제와 내병성 품종을 이용한 재배 등의 방제 방법이 주목 받고 있다(Cheah et al., 2000; Jang et al., 2001; Lahlali et al., 2012).
B. rapa에 속하는 배추의 경우에는 European fodder turnip인 ‘Gelia R’, ‘Siloga’, ‘Debra’ 및 ‘Milan White’로부터 CR(clubroot resistance) 유전자를 도입하여 뿌리혹병에 대한 저항성 품종을 개발하였고(Hirai, 2006; Piao et al., 2009), 배추의 뿌리혹병 저항성은 단인자 우성인 것으로 알려져 있다(James and Williams, 1980; Yoshikawa, 1993; Kuginuki et al., 1999). 이와 달리 브로콜리, 양배추, 케일 등을 포함하는 B. oleracea 작물은 뿌리혹병 저항성이 질적 형질이라는 견해도 있으나(Chiang and Crete, 1970; Yoshikawa, 1983), 많은 연구자들은 QTL(quantitative trait loci) 분석을 통하여 B. oleracea의 CR이 양적 형질, 즉 하나 혹은 두 개의 주동 QTLs와 일부 미동 QTLs에 의해 지배된다고 하였다(Landry et al., 1992; Figdore et al., 1993; Grandclement and Thomas, 1996; Voorrips et al., 1997; Moriguchi et al., 1999; Rocherieux et al., 2004; Nomura et al., 2005). 그러나 이들을 검정할 수 있는 특이적인 프라이머와 RFLP(restriction fragment length polymorphism) 마커 등의 정보 부족, 다인자에 의한 복잡한 CR 유전 및 저항성 유전 자원 부족 등으로 양배추의 CR 품종 개발은 많은 어려움을 겪고 있다(Hirai, 2006).
일본에서는 CR 양배추 품종이 일부 개발되어 판매되고 있으나, 국내에서는 아직 시판되고 있지 않다. 최근에는 우리 정부에서도 종자산업의 중요성을 인지하여 Golden Seed 프로젝트를 통하여 생명공학기술개발, 우수한 품종 육성 및 종자 생산 등에 많은 지원을 하고 있으며, 양배추, 배추 및 무 등의 CR 품종을 개발하기 위한 연구도 활발히 진행되고 있다. 뿌리혹병 저항성 양배추 품종을 효과적으로 개발하기 위해서는 반드시 양배추의 뿌리혹병 저항성에 대한 뿌리혹병균의 레이스 분화 연구가 필요하다. 하지만 양배추의 뿌리혹병 저항성에 대한 뿌리혹병균의 레이스 분화에 대해서는 거의 보고된 바 없다.
본 연구에서는 CR 양배추 품종 개발을 위한 효율적인 양배추 뿌리혹병 병리검정 체계 확립의 일환으로 양배추의 저항성에 대한 뿌리혹병균의 레이스 분화를 조사하기 위하여 연구하였다. 이를 위해 우리나라에서 시판 중인 양배추 16종에서 뿌리혹병균 4균주의 뿌리혹병 발생 정도를 조사하여 실험한 뿌리혹병균들의 병원력 차이를 조사하였다. 그리고 종자회사로부터 분양 받은 CR 양배추 계통 ‘YCR478’과 일본에서 구입한 CR 양배추 2품종의 12개 뿌리혹병균에 대한 저항성 정도를 확인하였으며, ‘YCR478’과 뿌리혹병 감수성 계통(‘C1176’)을 교배하여 F3 107종을 확보하고 병원력이 서로 다른 뿌리혹병균 3개 균주에 대한 이들의 저항성 차이를 조사하였다.
재료 및 방법
식물 재배
국내에서 시판 중인 양배추 품종 16개(‘오가네’, ‘YR온누리’, ‘대박나’, ‘YR호남’, ‘YR옴파로스’, ‘중생루비아’, ‘YR호걸’, ‘레드마트’, ‘YR에코플러스’, ‘아시아볼’, ‘꼬꼬마’, ‘CMS레드선’, ‘그랜드마트’, ‘루비아’, ‘그린핫’, ‘오조라’)와 일본에서 판매중인 CR 양배추 2품종(‘YCR GEKKO’, NORIN사; ‘YCR TAE’, NORIN사)을 구입하여 실험에 사용하였다. 그리고 양배추 저항성 계통인 ‘YCR478’ 그리고 이 계통을 감수성 품종(‘C1176’)과 교배하여 얻은 F3 107계통은 조은종묘로부터 분양 받아서 실험에 사용하였다. 모든 실험에는 뿌리혹병 발생 정도를 확인하기 위하여 대조 품종으로 배추인 ‘노랑김장’(몬산토코리아)을 함께 실험하였다.
양배추 품종들은 5 × 8 연결 포트(80mL/pot, 범농사)에 원예용상토 5호(부농)를 넣고 양배추 종자를 포트당 1립씩 그리고 품종당 10립씩을 파종하여 온실(25 ± 5°C)에서 14일 동안 재배하였다. 배추도 양배추와 동일한 방법으로 파종하여 10일 동안 재배한 유묘를 실험에 사용하였다.
뿌리혹병균 균주 및 접종원 준비
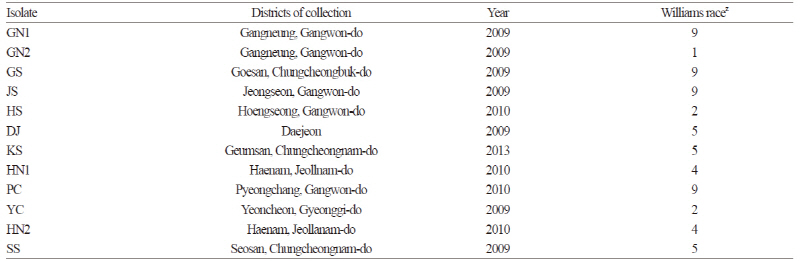
2009년부터 2013년까지 대전광역시(DJ), 충청남도 서산시(SS)와 금산군(KS), 충청북도 괴산군(GS), 경기도 연천군(YC), 전라남도 해남군(HN1, HN2) 그리고 강원도 강릉시(GN1, GN2), 정선군(JS), 횡성군(HS) 및 평창군(PC)에서 전형적인 뿌리혹병을 나타내는 뿌리를 채집하여 -80°C 초저온냉동고에 보관하였다(Table 1). 각 지역에서 수집한 뿌리혹 1g을 취하여 포자 현탁액을 만들고 이를 배추(‘노랑김장’, 몬산토코리아) 100포기에 접종하고 온실(20 ± 5°C)에서 60일 동안 재배하여 증식하였다. 이들 배추의 뿌리혹을 수확하여 깨끗하게 씻고 -80°C 초저온냉동고에 보관하면서 실험에 사용하였다.
뿌리혹병균 접종원을 준비하기 위해서는 -80°C 초저온냉동고에 보관 중인 뿌리혹병균 균주를 꺼내어 증류수로 깨끗하게 씻어서 뿌리 표면에 붙은 이물질을 제거하였다. 이를 Waring blender에 넣고 멸균수를 첨가하여 마쇄하고, 4겹의 가제로 여과하여 식물 조직을 제거한 포자 현탁액을 만들었다. 그리고 광학현미경 하(300배)에서 hemocytometer를 이용하여 휴면 포자의 농도를 조정하였는데, 뿌리혹병균 4균주에 대한 양배추 일반 품종 16종의 뿌리혹병 발생 실험에서는 4.0 × 107spores · mL-1으로, 12종 뿌리혹병균에 대한 CR 양배추 계통 ‘YCR478’과 CR 양배추 2품종은 4.0 × 107spores · mL-1으로, 뿌리혹병균 3종에 대한 F3 계통 107점의 실험은 1.0 × 108spores · mL-1로 준비하였다.
Table 1. Twelve isolates of Plasmodiophora brassicae used in this study.
| |
zSource from Jo et al., 2011. | |
접종 및 병 발생 조사
온실에서 재배한 양배추 유묘에 준비한 포자 현탁액을 포트당 5mL씩 토양 관주하여 접종하였다. 뿌리혹병 발생을 위하여 접종한 유묘를 20°C 생육실로 옮긴 후 하루에 14시간씩 광을 조사하면서 7일 동안 배양한 후에 온실(20 ± 5°C)로 이동하여 재배하였다. 뿌리혹병 발생 정도를 확인하기 위한 대조구인 배추(‘노랑김장’) 유묘도 동일한 방법으로 접종하고 관리하였다. 접종 6주 후에 대조품종 배추에 뿌리혹병이 충분하게 발생한 것을 확인하고 양배추 식물체의 뿌리를 뽑아서 흙을 털어내고 수돗물로 깨끗이 씻은 뒤에 병 발생 정도를 아래와 같은 기준에 따라 조사하였다.
병 발생 조사 기준은 0 = 뿌리혹병 발생이 없음, 1 = 측근에 혹이 착생되어 비대 정도가 적고 서로 독립하여 존재, 2 = 측근에 혹이 착생되며 비대 정도가 비교적 큼, 3 = 주근에 혹이 착생되며 서로 접합되고 비대 정도가 큼, 4 = 주근에 혹이 착생되며 서로 접합되고 비대 정도가 매우 큼 등의 5단계로 하였다. 평균 발병도가 1.0 이하인 경우에는 저항성, 1.1 이상에서 2.0 이하는 중도저항성 그리고 2.1 이상은 감수성으로 판정하였다.
‘YCR478’ × ‘C1176’의 F3 계통의 양배추 뿌리혹병 저항성 실험을 제외한 모든 실험은 10반복으로 2회 수행하였다. 그리고 SAS(SAS Institute, Inc., 1989, Cary, NC) 프로그램을 이용하여 ANOVA 분석을 하였으며, 처리 평균간 비교를 위하여 Duncan’s multiple range tast (p < 0.05)를 실시하였다.
결과 및 고찰
국내 시판 양배추 품종들에서 뿌리혹병 발생
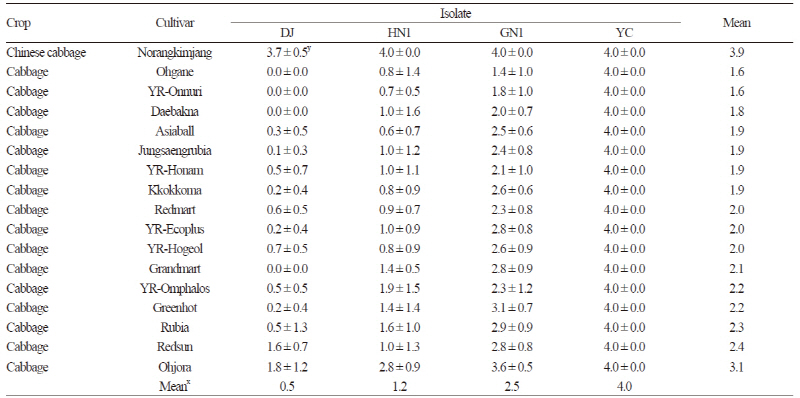
뿌리혹병 균주들의 양배추에서의 병원력 차이를 조사하기 위하여 뿌리혹병 저항성이 아닌 일반 양배추 품종 16종에 4개의 뿌리혹병균 균주(DJ, HN1, GN1 및 YC 균주)를 접종하고 이들의 뿌리혹병 발생을 조사한 결과, 뿌리혹병균 4개 균주에 의한 뿌리혹병 발생은 균주에 따라 차이가 있었다(Table 2).
배추에서 뿌리혹병균 DJ, HN1, GN1 및 YC 균주에 의한 뿌리혹병 발병도는 각각 3.7, 4.0, 4.0, 4.0으로 균주 간에 거의 차이가 없었으나, 실험한 양배추 품종들의 뿌리혹병 평균 발병도는 각각 0.5, 1.2, 2.5 및 4.0으로 뿌리혹병균 균주 간에 차이가 있었다(Table 2). 따라서 양배추에 대해서는 뿌리혹병균 간의 병원력에 차이가 있었으며, 실험한 균주 중 병원력이 가장 강한 균주는 YC이었으며 그 다음은 GN1, HN1, DJ순이었다.
병원력이 가장 강한 YC 균주는 실험한 모든 양배추 품종에서 발병도 4.0을 나타냈으나, 병원력이 가장 낮은 DJ 균주는 14개 품종에서 1.0 이하의 발병도를 보였다(Table 2). 그리고 다음으로 병원력이 낮은 HN1 균주의 경우에는 11개 품종이 1.0 이하의 발병도를 보였으며, GN1 균주는 1.0 이하의 발병도를 나타내는 품종은 없었으며 모든 품종에서 1.4 이상의 발병도를 보였다.
뿌리혹병균은 기주의 종 및 계통에 따라서 다양한 병원성 반응을 나타낸다고 알려져 있다(Williams, 1966; Buczacki et al., 1975). 배추의 경우에는 품종과 뿌리혹병균 균주 간에 특이적인 레이스 분화가 존재하나(Kuginuki et al., 1999; Hatakeyama et al., 2004; Jo et al., 2011), 감수성 품종에서의 뿌리혹병 발생은 거의 차이가 없다고 하였다(Jo et al., 2011). 본 연구에서도 배추에서의 뿌리혹병균의 병원력은 Jo et al.(2011)과 마찬가지로 거의 차이가 없었으나, 양배추에서는 뿌리혹병균 균주 간의 병원력 차이는 뚜렷하였다(Table 2).
다양한 뿌리혹병균에 대한 CR 양배추들의 저항성
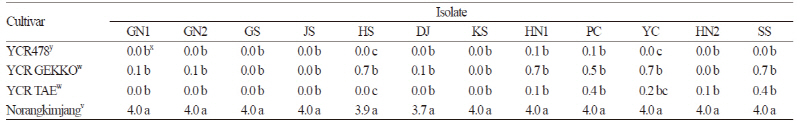
조은종묘로부터 분양 받은 CR 양배추 계통 ‘YCR478’과 일본에서 구입한 CR 양배추 2품종 ‘YCR GEKKO’, ‘YCR TAE’의 다양한 Williams race(race 1, 2, 4, 5, 9)의 뿌리혹병균 12개 균주(Table 1)에 대한 저항성 차이를 조사한 결과(Jo et al., 2011), CR 계통인 ‘YCR478’은 실험한 모든 뿌리혹병 균주에 의해 뿌리혹병이 거의 발생하지 않았다. 그리고 CR 품종인 ‘YCR GEKKO’와 ‘YCR TAE’도 뿌리혹병균 12균주에 대한 저항성은 거의 차이가 없었으며, 모두 0.7 이하의 낮은 발병도를 보였다(Table 3). 따라서 ‘YCR478’, ‘YCR GEKKO’ 및 ‘YCR TAE’는 실험한 모든 뿌리혹병균에 대하여 고도의 저항성임을 알 수 있었다.
배추(B. rapa subsp. pekinensis)의 뿌리혹병 저항성(CR) 품종은 1984년에 일본에서 처음 판매되기 시작하여 이후에 많은 저항성 품종들이 개발되었는데, 이들의 저항성은 European turnip(B. rapa)인 ‘Siloga’, ‘Gelria R’, ‘Milan White’, ‘Debra’로부터 도입되었으며, 이들 배추 품종의 저항성은 단인자 우성 유전을 한다고 보고되었다(James and Williams, 1980; Yoshikawa, 1993; Kuginuki et al., 1999). 그리고 이후 일본의 CR 배추 품종들 대부분은 포장에서 저항성이 무너졌다고 보고되었다(Tanaka et al., 1998; Kuginuki et al., 1999). 한편, 2005년에 배추(B. rapa cv. Parkin)로부터 뿌리혹병 저항성이 도입된 일부 양배추 품종(‘Kilaton’, ‘Tekila’)이 출시되었는데, 배추(‘Parkin’)에서와 마찬가지로 독일, 폴란드, 프랑스 등의 일부 지역에서 저항성이 무너졌다(Diederichsen et al., 2009).
이와 달리 양배추의 저항성 유전에 대해서는 다양한 의견이 존재하는데, 소수의 열성 유전자가 지배한다는 보고 즉 질적 저항성이라는 보고도 있으나, 2개 이상의 유전자가 관여하는 양적 저항성이라는 것이 지배적이다. 뿌리혹병에 대한 B. oleracea의 저항성 유전자는 지금까지 약 22개의 QTLs이 있다고 알려져 있다(Piao et al., 2009). 스웨덴 순무 ‘Wilhelmsburger’에서 뿌리혹병균 race 2에 저항성을 보이는 2개의 QTLs, CR2a와 CR2b(Landry et al., 1992), 브로콜리에서 race 7에 저항성을 보이는 3개의 QTLs(Figdore et al., 1993), ‘Bindsachsener’에서 찾은 2개의 주동 QTLs과 1개의 미동 QTLs 등이 있다(Voorrips et al., 1997). 따라서 B. oleracea의 뿌리혹병 저항성은 2개 이상의 다인자에 의해 결정되는 QTL 저항성이므로, 질적 저항성인 배추 CR 품종에서와 같이 저항성이 무너지는 현상 즉 뿌리혹병 저항성에 대한 병원균의 레이스 분화는 일어나지 않아서 실험한 12개 뿌리혹병균에 대한 저항성 차이는 없는 것으로 생각되었다.
CR 양배추 F3 계통의 뿌리혹병 저항성
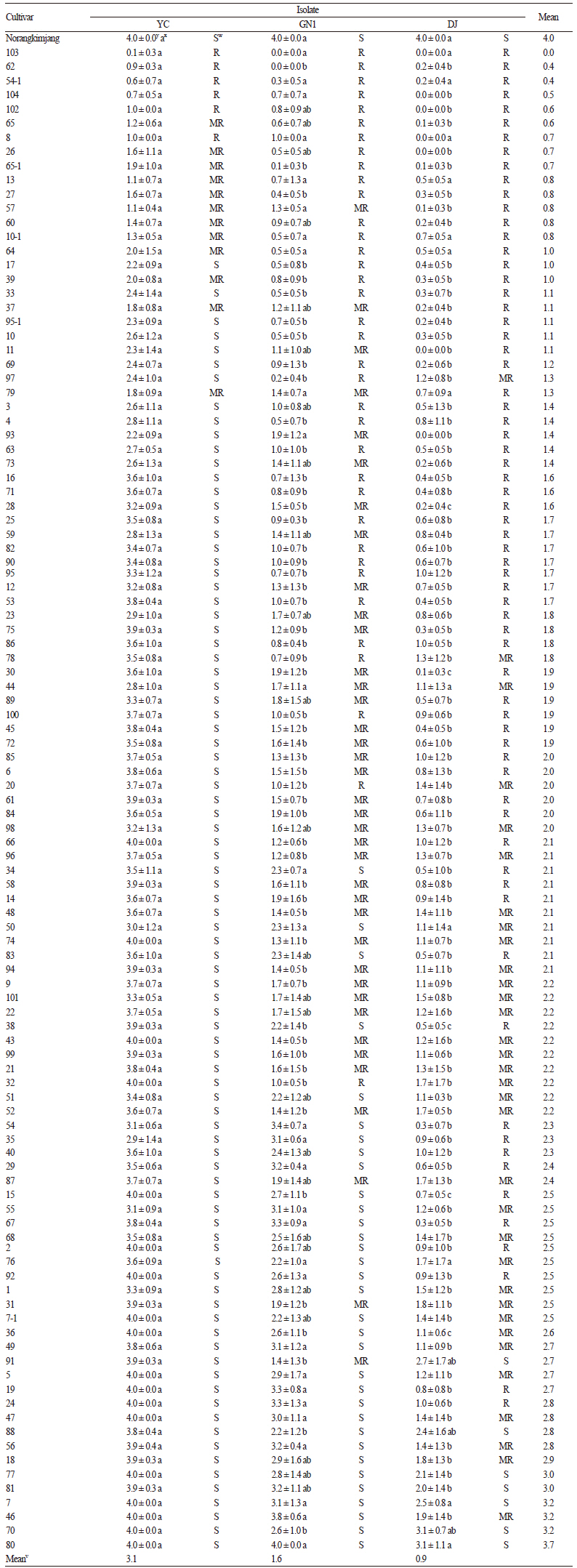
뿌리혹병 저항성 양배추 계통 ‘YCR478’과 감수성 계통 ‘C1176’을 교배하여 만든 F3 계통 107점의 뿌리혹병 저항성을 병원력 정도가 서로 다른 3개 균주에 대하여 조사한 결과, YC, GN1 및 DJ 균주에 의한 양배추 F3 107계통의 평균 발병도는 각각 3.1, 1.6 및 0.9이었다(Table 4). 따라서 양배추 일반 품종 16종에서의 뿌리혹병 발생에서와 마찬가지로 F3 107종에 대해서도 병원력이 가장 강한 YC 균주는 가장 높은 발병도를 그리고 병원력이 가장 낮은 DJ 균주는 가장 낮은 발병도를 나타냈다(Table 4).
이들 3개 P. brassicae 균주들에 대한 ‘YCR478’ × ‘C1176’ 교배의 107개 F3 계통의 저항성은 이들 균주의 병원력(virulence)에 따라 다른 결과를 나타내었다(Table 4). 즉 병원력이 가장 강한 YC 균주에 대하여 저항성을 나타내는 F3는 6개로 3균주 중 가장 적었으며, 중도저항성과 감수성을 보이는 F3는 각각 12개와 89개이었다. 이와 달리 병원력이 가장 낮은 DJ 균주에 대해서는 저항성 F3가 67개로 가장 많았으며, 중도저항성과 감수성 반응을 보이는 F3는 각각 34개와 6개이었다. 중간 정도의 병원력을 지니는 GN1 균주에 대해서는 저항성이 36개, 중도저항성이 38개, 감수성이 33개로 저항성 F3의 수가 중간이었다.
그리고 실험한 ‘YCR478’ × ‘C1176’ 교배의 F3 107계통의 3가지 뿌리혹병균에 대한 저항성 차이를 조사하기 위하여 Table 4에서와 같이 병원력이 높은 균주순 즉 YC, GN1, DJ 균주 순서로 이들 균주에 의한 뿌리혹병 발병도를 정리하면, 실험한 F3 중 102계통은 균주의 병원력이 증가할 수록 저항성이 감소하였다(Table 4). 그리고 나머지 5개 F3(20, 32, 78, 91, 97)만이 GN1 균주와 DJ 균주 간에 대한 반응이 앞에서와 달리 상대적으로 병원력이 강한 GN1 균주에는 발병도가 낮게, 병원력이 낮은 DJ 균주에는 발병도가 높게 나왔다. 하지만 이들 F3에서의 두 균주에 의한 뿌리혹병 발병도는 차이가 크지 않으므로 이들이 두 균주에 대하여 특이적으로 저항성 반응을 나타낸 것으로 생각되지는 않았다.
Jo et al.(2014)은 고추의 역병 저항성은 양적 저항성이고, 고추 품종들의 역병균에 대한 저항성은 P. capsici 균주와 고추 품종 간에 특이적인 저항성 반응이 존재하지 않고, 고추 품종에 우수한 역병 저항성 유전자를 얼마나 많이 도입하였느냐에 따라 균주의 병원력에 반비례하여 고추 품종들의 역병에 대한 저항성에 차이를 보인다고 하였다.
배추의 뿌리혹병균에 대한 저항성과 같이 질적 저항성을 나타내며 특이적인 race 분화가 존재하는 것과 달리, 양배추의 뿌리혹병 저항성은 고추의 역병 저항성과 마찬가지로 양적 저항성(QTL) 유전을 하고 P. brassicae 균주의 병원력과 반대로 ‘YCR478’ × ‘C1176’의 F3에 저항성 유전자가 많이 집적되어 있는 F3 계통은 병원력이 더 강한 균주에도 저항성을 나타내고, 저항성 유전자가 적게 들어 있는 F3 계통은 병원력이 약한 균주에만 저항성을 보이는 것으로 생각되었다.
따라서 뿌리혹병 저항성 양배추 품종을 개발하기 위한 병리 검정 전략은 고도의 저항성 품종을 육종하기 위해서는 YC 균주와 같이 병원력이 강한 균주를 사용하여 뿌리혹병 저항성을 선발하는 것이 필요하고, 보통의 저항성 품종을 위해서는 GN1 균주와 같이 중간 정도의 병원력을 가지는 뿌리혹병균을 사용하여 병리 검정을 수행하는 것이 바람직할 것으로 생각되었다.