서 언
고형배지를 사용하는 수경재배에서는 근권부의 염류 집적과 이에 따른 양분 균형 변화 등이 나타날 수 있으며 이를 교정하기 위해서는 일정 비율의 배액을 필요로 한다(Schon and Compton, 1997). 이 과정에서 질산태 질소와 같은 양분이 고농도로 용탈되며, 이는 지하수 오염원으로 작용한다(McAvoy, 1994). 따라서 배액을 재사용하는 순환식 수경재배 방식을 적용하여 양수분의 이용효율을 증가시키고(Ahn et al., 2010; Ko et al., 2013), 환경오염원을 감소시킬 필요가 있지만(Van Os, 1999), 비순환식에 비해 투입비용의 증가(Van Os, 1991), 양분 불균형 발생(Zekki et al., 1996), 유기산의 집적(Lee et al., 2006) 등이 우려된다. 이는 농가의 순환식 수경재배 방식의 적용에 대해 불안 요인으로 작용하며, 기술적인 안정화가 필요한 부분이다.
수경재배는 외부와 토양으로부터 격리된 시설재배환경에서 이루어지기 때문에, 토경재배에 비해 미생물의 개체수와 종류를 비교적 낮은 수준에서 유지시킬 수 있지만 발병 시에는 토경재배에 비해 더 심한 수준으로 진행될 수 있으며, 이러한 온실 내 병원균은 물, 토양, 공기 등의 경로를 통해서 전파될 수 있다(Agrios, 2005). 따라서 온실 내부의 미생물의 개체수 증가는 병이 전파될 수 있는 경로와 전염 가능성을 증가시키는 원인이 될 수 있다. 또한 온습도와 같은 환경조건(Etchellis et al., 1973)과, 영양조건(Chang et al., 2007) 등은 미생물의 개체수 증가에 영향을 미칠 수 있다.
비순환식 온실의 경우는 순환식 수경재배에 비하여 배액의 적극적인 집수과정이 없으며 일부는 온실 내 잔류하거나 외부로 방류된다. 특히, 대부분의 비순환식 온실에서는 관수 시 배액은 온실 내부로 방출되어 증발된다. 순환식과 비순환식 수경재배 시스템의 구조적 차이는 온실 내 미세 환경조건과 영양조건 등에 변화를 발생시킬 수 있으며, 이는 병원균의 개체 증식에 영향을 줄 수 있는 요인이다. 따라서 순환식 수경재배 방식의 적용 시 온실 내 배액의 폐쇄적 순환 구조로 인해 배액을 온실 내외부로 방류하는 비순환식 수경재배 시스템에 비해 상대적으로 병발생 억제에 유리한 조건을 갖출 수 있을 것으로 생각된다. 이에 대한 연구를 통해 수경재배 시스템에 따른 미생물 집락수 변화의 차이를 확인할 수 있다면 순환식 수경재배 시스템의 적용 효과인 자원절약 및 환경부하 감소와 더불어 온실 내 위생조건의 향상 측면을 고려할 수 있게 하여, 적용에 따른 불안요인을 감소시키고 순환식 수경재배 시스템의 보급확대에 기여할 수 있을 것으로 기대된다. 본 연구는 순환식과 비순환식 수경재배를 채택하고 있는 상업용 농가에서 병원균의 집락형성단위(CFU) 수준을 조사 분석하여 순환식 수경재배 시스템의 배액 수집에 따른 온실 내 미생물의 개체수 변화를 분석하고자 수행하였다.
재료 및 방법
수경재배 온실 조건
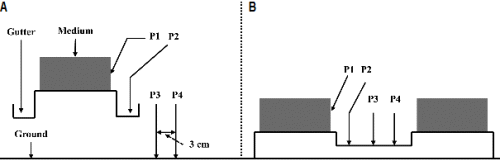
본 연구는 파프리카를 재배하는 1ha 이상의 복합환경제어 시스템을 갖춘 상업용 벤로형 유리온실을 대상으로 조사하였다. 비순환식과 순환식 수경재배 농가 중 코이어와 암면을 배지로 사용하는 2개 농가를 각각 선정하여 2012년 10월 24일에서 26일 사이에 시료를 채취하였다. 모든 농가는 일사비례제어 점적 관수 방식이 적용되어 있었으며, 매일 공급 양액의 30% 정도의 양액이 배액되도록 관리되었다. 순환식 수경재배의 배액은 UV 살균방식이 적용되었으며, 발생된 배액이 행잉 거터(hanging gutter)의 배수로를 통해 1차 집수탱크로 저장되었다(Fig. 1A). 비순환식 수경재배 농가에서 발생된 배액은 2열의 배지 사이에 위치한 스티로폼 베드의 배수로를 통해서 온실 내 배수탱크로 이송되거나 온실 내 정체되는 구조였다(Fig. 1B). 모든 농가의 통로를 제외한 바닥면은 피복자재로 피복되어 있었으며, 모두 약 2주 전에 살균제 살포가 이루어졌다.
미생물 시료 채취 및 배양
시료는 배지의 피복재와 거터, 온실 바닥 면을 대상으로 하여 각각 채취되었으며, 멸균된 1회용 면봉(3M quick swab, 3M, USA)을 이용하여 표면에 대해 약 30°의 기울기를 유지하며 지그재그로 3회 반복 이동하여 접촉하여 채취하였다. 수집에 사용된 면봉은 수집액에 담아 밀봉하였으며, 아이스 박스에 냉장 보관하여 이동하였다. 배지의 피복재를 기준으로 25cm2의 정사각형 면적에 대해서 3cm 간격으로 4개의 지점에서 시료를 채취 하였으며(Fig. 1), 이러한 수집 작업을 각 온실별 무작위로 장소를 선정하여 3회 반복 채취하였다. 시료는 10, 100, 1000배의 배율로 멸균 증류수를 이용하여 희석하였다. 희석 배율 중 30-300개의 집락을 형성한 배지를 집락수 계산에 사용하였으며, 최대 희석 배율에서도 300개 이상의 집락이 존재할 경우에는 단위 면적당 평균 집락수를 계산한 후 배양면적을 곱하여 집락수를 계산하였다. 미생물 시료의 배양에는 3M 건조필름 배지를 사용하였으며, 일반 호기성 세균배지(3M Petrifilm aerobic count plate, 3M, USA)와 진균류 배지(3M Petrifilm yeast and mold count plate, 3M, USA)를 이용하여 선택적으로 배양하였다. 일반 세균은 35°C에서 48시간 동안 배양하였으며, 진균류는 25°C에서 72시간 동안 배양하였다. 배양 종료 후 단위면적당 집락형성단위(CFU)를 다음과 같이 계산하였다.
미생물 CFU의 조건별 평균의 비교는 분산분석을 통해 유의성 검정을 하였으며, 미생물의 개체수의 수준과 이에 대한 온실 내 시료 수집 지점의 영향력을 평가하기 위해 주성분분석(principal component analysis)을 이용하였다. 상기의 통계분석을 위해서는 SAS 9.3(SAS Institute, Cary, NC, USA)을 이용하였다.
결과 및 고찰
각 온실의 채취지점에서 수집한 미생물 시료를 배양한 후 조사 농가의 수경재배 조건에 대해서 분석한 결과, 진균류의 경우의 CFU 값은 순환식 농가가 비순환식 농가에 비해 유의적으로 낮게 나타났다(Table 2). 세균류의 경우 유의차는 없었지만, 코이어 배지를 사용하는 순환식 수경재배 온실이 3.65 log CFU/cm2로 비순환식 온실의 3.78 log CFU/cm2의낮은 경향을 나타냈고, 암면의 경우에도 순환식 온실이 2.66 log CFU/cm2로 3.18 log CFU/cm2의 비순환식 온실보다 낮은 경향을 나타냈다. 외부와 차단된 수경재배 온실 내 미생물의 개체수 증가는 배액의 수집 방식에 따른 환경조건의 차이에 의한 영향이 비교적 클 수 있으며, 미생물에 대해서 일종의 배지로 작용할 수 있는 배액의 성분에 따른 영향이 있을 수 있다. 본 조사에 포함된 온실은 각각 암면과 코이어를 배지로 사용하였으나 각각은 무기배지와 유기배지로써 배액의 성분에 차이가 있을 수 있다. 조사한 온실 내 CFU를 배지에 대해서 분석한 결과, 진균류에서 암면배지를 사용하는 순환식 수경재배 온실에서 유의적으로 가장 낮은 수준의 CFU 값을 나타냈다. 그러나 코이어를 배지로 사용하는 순환식 수경재배 온실은 암면 배지를 사용하는 비순환식 온실과 유사한 수준으로 나타났다. 진균류에서 가장 높은 CFU 값은 코이어를 배지로 사용하는 비순환식 온실로 나타났다. 세균류에서는 코이어 배지가 사용된 순환식과 비순환식 수경재배 온실에서 높은 값이 관찰되었다.
코이어 배지는 코코넛 섬유로 이루어져 있으며 배액으로 유기물질이 유출될 수 있다(Domeño et al., 2009). 또한 유기물의 함량 차이는 미생물의 활동 및 개체수 증가에 영향을 줄 수 있다(Chang et al., 2007). 배지에 따른 상기의 결과는 배액의 질적인 차이에 따른 간섭으로 판단된다. 비순환식 수경재배 온실은 순환식 수경재배 온실에 비해 배액이 거쳐 가는 면적이 상대적으로 넓으며, 이로 인해 미생물의 개체수 증가를 최소화 하는데 상대적으로 불리한 조건에 있는 것으로 판단된다. 이와 같은 결과들은 통제된 실험 시설이 아닌 실제 상업농가 현장에서 조사가 이루어진 본 연구의 제약상 조사의 기준인 순환식과 비순환식 배액 수집 시설의 차이에 따른 영향 외에도 농가의 살균제 살포와 같은 요인의 영향을 배제할 수는 없다. 그러나 Rowe and Farely(1978)는 토마토 재배 온실 내 살균된 토양에 미생물을 투입한 결과 2-3주 안에 재집락이 형성됨을 보고한 바 있으며, 조사한 농가는 모두 약 2주 전에 살균제 살포가 이루어진 상태였기 때문에 조사 결과에 대한 간섭 효과는 최소화되었을 것으로 판단된다.
순환식과 비순환식 농가의 시료 채취 구역은 Fig. 1의 P1와 P2 구역의 경우 각각 배지와 배액 집수 부분으로 유사하지만 비순환식의 P3와 P4구역(Fig. 1B)은 배액 집수부에, 순환식의 경우 온실 바닥면에 해당하여 기능적인 차이가 있다. 비순환식 수경재배 시설의 경우 배액의 적극적인 집수과정을 필요로 하지 않으므로 일부는 온실 외부로 방류되거나 배지 근처에서 정체되어 있게 된다. 이로 인해 순환식 수경재배 온실의 P3와 P4 구역(Fig. 1A)의 표면은 비순환식 온실의 동일 구역에 비해 미생물의 생육에 있어서 습도, 무기염류 등에서 다른 수준의 환경을 제공하게 된다. 미생물 개체수의 증가 속도는 초기 집락수와 온도, 습도와 같은 환경 조건, 무기양분 등에 의해서 결정될 수 있다(Etchellis et al., 1973; Sridhar and Bärlocher, 2000; van Maanen and Xu, 2003). 본 연구에서 조사 농가의 수경재배 조건의 차이에 따라 나타난 미생물 집락수의 차이는 시료 채취 표면의 환경조건이 미생물의 번식에 직간접적으로 영향을 미친 결과로 판단된다.
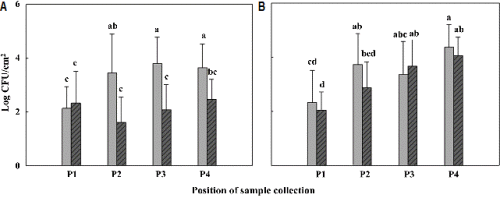
온실 내 시료를 채취한 구역별 CFU 값을 비교한 결과는 Fig. 2와 같다. 비순환식 온실에서 진균류의 경우 P2-P4 구역이 가장 높은 수준으로 나타났으나, P1 구역은 순환식 온실의 동일 구역과 함께 유의적으로 가장 낮은 것으로 조사되었다. 세균류의 경우는 각 구역에 대해 명확한 유의차가 관찰되지 않았지만, 비순환식과 순환식 수경재배 온실의 P1 구역의 CFU가 가장 낮은 경향을 나타냈다. P1 구역은 비순환식 온실과 순환식 온실 모두 배지의 피복 부위로써 유사한 환경조건을 가지고 있으며, 비순환식 온실이라도 위치 별로 다른 환경조건에 노출되어 있었기 때문에 나타난 차이로 볼 수 있다. 진균류의 순환식 수경재배 온실의 CFU는 모든 구역에서 비순환식 온실에 비해 전체적으로 가장 낮은 수준을 나타내었으며, 세균류의 경우는 순환식 온실의 전 구역에서 유의하지는 않지만 비순환식에 비해 낮은 경향의 CFU가 관찰되었다. 따라서 본 조사에서 나타난 결과가 다른 요인들의 간섭보다는 비순환식 또는 순환식 시스템의 적용에 따른 환경조건의 차이가 미생물의 개체수 증가에 미친 영향이 컸던 것으로 추정할 수 있다.
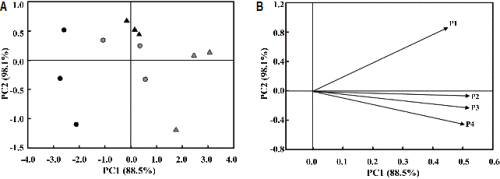
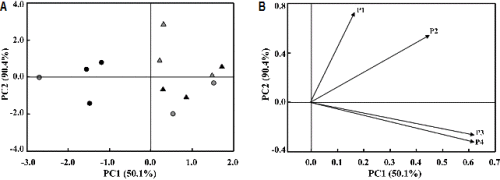
각 온실 내 시료의 수집 지점을 설명변수로 하고 미생물의 개체수 수준을 목적변수로 설정한 주성분 분석결과 진균류의 경우 제1주성분에서 코이어를 사용하는 비순환식 온실의 주성분 점수가 가장 높게 나타났으며, 그 다음으로 암면을 사용하는 비순환식 온실, 코이어 이용 순환식 온실, 암면 이용 순환식 온실 순으로 나타났다(Fig. 3). 제1주성분의 결과에는 P2 구역이 가장 크게 기여하였지만 P3와 P4 구역도 유사한 수준으로 나타났으며, P1 구역이 가장 낮게 나타났다. 세균류의 경우는 전반적으로 비순환식 수경재배 온실이 높은 수준의 주성분 점수를 나타냈으나 코이어를 사용하는 순환식 수경재배 온실도 이와 유사한 수준의 점수를 나타냈다(Fig. 4). 그러나, 세균류의 경우도 암면을 사용하는 순환식 수경재배 온실이 주로 낮은 수준의 주성분 점수를 나타냈다. 세균류의 주성분 분석 결과에는 P4 구역이 가장 크게 기여하였으며, 비슷한 수준으로 P3 구역이 기여하는 것으로 나타났다. 세균류의 경우도 P1 구역이 가장 낮은 수준으로 기여하는 것으로 관찰됐다. 이는 온실 내 환경의 차이로 작용했던 배액 이동 경로 상에 있는 P2 - P4 구역이 온실 내 미생물 개체수의 변화에 영향력이 있는 변수로 작용하고 있다는 것을 의미하며, 배지의 피복부분에 해당하여 상대적으로 배액의 발생에 대한 환경적인 영향을 적게 받는 P1 구역의 영향력이 작았음을 의미한다.
발병을 구성하는 3요소는 발병력과 밀도 등의 총합으로 나타낼 수 있는 병원체와 환경, 기주식물로 구성될 수 있으며 이 요소 간의 상호관계를 병삼각형으로 나타낼 수 있다(Agrios, 2005). 온실의 경우 단일 작물로 구성되어 기주식물의 개체수 측면에서 병 발생에 유리하게 작용할 수 있는 조건을 갖추고 있으며, 비순환식 온실의 경우 환경, 병원체의 요소에 대해 순환식 온실보다 더 높은 수준에 있는 것으로 생각된다. 본 연구에서는 미생물의 전체적인 개체수만을 조사하였기 때문에 이 집단을 구성하는 미생물이 병원성 또는 비병원성 여부를 알 수 없다. 그러나, 한 공간에서 특정 식물의 개체수가 증가할 경우 해당식물을 기주식물로 하는 병원체의 개체수는 함께 증가하는 경향을 가지고 있다(Flory and Clay, 2013). 비순환식 수경재배 시스템을 적용한 온실이 병삼각형의 3요소를 상대적으로 더 높은 수준에서 만족시키고 있으며, 따라서 잠재적인 병발생의 측면에서 비순환식 수경재배는 순환식 수경재배 온실보다 더 높은 가능성을 나타내고 있는 것으로 판단된다.
순환식 수경재배는 배액의 재사용에 따른 배액 내 병원성 미생물의 집적이 우려되는 측면이 있지만 비순환식 수경재배 온실은 배액의 수집에 대한 기술적인 필요성이 낮음에 따라 발생하는 온실 내 미세 환경의 변화와 그에 따른 잠재적 병발생 가능성의 증가를 고려할 필요가 있다. 조사대상인 고형배지를 사용하는 국내 순환식 수경재배 온실의 수가 극단적으로 적은 본 연구의 특성상, 충분한 표본을 확보하지 못하는 한계로 인해 조사 결과에 그에 따른 영향이 있을 수 있다. 그러나, 전반적으로 비순환식 수경재배 온실의 배액 내부 방류에 따른 온실 내 미생물 개체수 증가 현상이 관찰된 것으로 판단된다. 따라서 적절한 배액 살균 기술의 적용과 함께 순환식 수경재배를 위한 배액 수집 방식을 적용할 경우, 잠재적인 병 발생 억제 측면에서 상대적으로 유리한 온실 조건을 조성할 수 있을 것으로 기대된다.